髄液シャント術
対象:頭痛が顕著な場合に好まれる。VPS(脳室腹腔)またはLPS(腰椎腹腔)。
特徴:頭痛改善に優れる。即時成功率はONSFと同等。
注意点:長期再手術率50%超。シャント不全・感染・転位のリスクあり。

特発性頭蓋内圧亢進症(idiopathic intracranial hypertension; IIH)は、明らかな原因なく頭蓋内圧が上昇する疾患である。劇症型特発性頭蓋内圧亢進症(fulminant idiopathic intracranial hypertension; FIH)はその亜型であり、症状発現から4週間未満で重度かつ急速に進行する視力障害を特徴とする。
疫学:IIHの年間発生率は約1.15/10万人(米国)と推定される9)。IIHは主に生殖年齢の肥満女性に好発するが、FIHは男性・小児・非肥満者でも報告されている3)。FIHはIIH患者の2〜3%に発生する。
診断の規模:Thambisettyらによる16例シリーズは現時点で最大のFIH症例集積報告であり1)、平均視力低下発現から16日(7〜28日)で高度視力障害に至った。CSF開放圧の平均は541 mmH2O(29〜70 cm H2O)と極めて高値であった。
定義の議論:FIHを「4週間以内」という時間基準で定義することへの異論もある。視力を脅かす進行速度を基準とすべきとの提案もなされており8)、定義の統一に向けた議論が継続している。
FIHはIIHの亜型であり、症状発現から4週間以内に急速かつ重度な視力障害をきたす点が通常のIIHと異なる。IIH患者の2〜3%に発生する。通常のIIHが比較的緩徐に進行するのに対し、FIHは数日単位で視力が悪化し、迅速な介入なしには不可逆的な失明に至りうる。
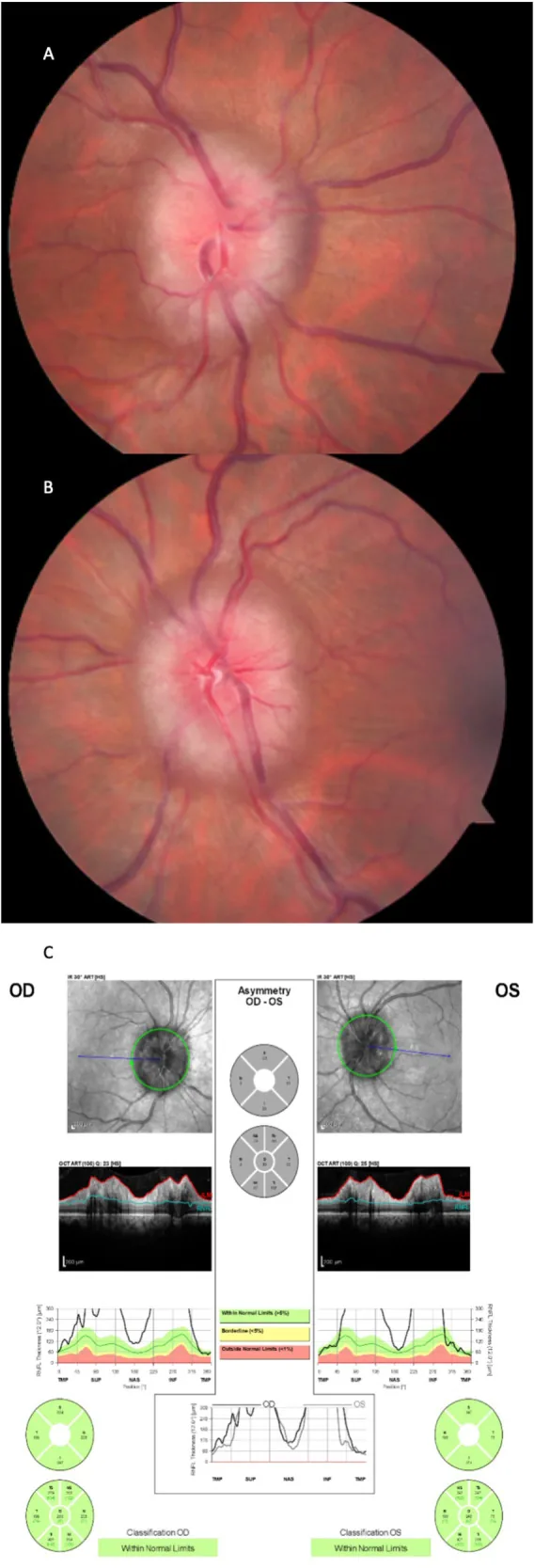
FIHの自覚症状は通常のIIHと共通するが、進行速度が著しく速い点が特徴である。
初期の網膜神経線維層厚が高いほど長期的な視力予後が不良とされる8)。また、ベースラインのHumphrey視野検査(VF)平均偏差が-7 dBを下回る場合には視力回復が困難との報告がある8)。診断の遅延(Aldhahwaniらの報告では平均3.2ヶ月)も不良予後に直結する3)。
特発性頭蓋内圧亢進症・劇症型特発性頭蓋内圧亢進症の主なリスク因子を以下に示す。
FIHの診断には以下の3要件をすべて満たす必要がある。
改訂Dandy基準の要点:
FIHの診断において鑑別が必要な主要疾患を以下に示す3)8)。
| 疾患 | 鑑別のポイント |
|---|---|
| 悪性高血圧性視神経症 | 血圧測定・眼底所見(火炎状出血・綿花状白斑) |
| 髄膜炎 | CSF細胞数増多・発熱・髄膜刺激症状 |
| 脳静脈洞血栓症 | MRV所見・凝固異常 |
| 視神経炎(MOG・NMOSD・サルコイドーシス・梅毒) | 血清抗体・CSF所見・全身症状 |
| 視神経浸潤(悪性腫瘍) | MRI造影所見・全身精査 |
FIH患者は入院管理を原則とし、積極的な内科的・外科的治療を行う。
日本では、特発性頭蓋内圧亢進症に対して以下が基本的な治療である。
主要な薬剤の特徴を以下に示す。
| 薬剤 | 用量 | 備考 |
|---|---|---|
| アセタゾラミド | 1日2〜4 g | 第一選択薬。RCTで有効性が証明された唯一の薬剤 |
| トピラマート | 適宜 | アセタゾラミド不耐時の代替。催奇形性あり(妊婦禁忌) |
| フロセミド | 適宜 | 代替薬。RCTでの有効性は証明されていない |
アセタゾラミドが使用不可の場合、トピラマートまたはフロセミドが代替薬となる。ただしRCTで有効性が確立されているのはアセタゾラミドのみである10)。
メチルプレドニゾロン静注:FIHに限り一時的措置として使用されることがある。北米では特に小児例で用いられる慣行があるが、英国では成人FIHへの通常使用は行わない8)。
Srivastava & Micieli(2022)は、36歳男性(体格指数 47.3、脳脊髄液開放圧45 cm H2O)に対してアセタゾラミド最大4 g/日を単独投与した。手術を拒否したにもかかわらず、4ヶ月で乳頭浮腫消失、6ヶ月で両眼視力20/20まで回復した。視野平均偏差は右-18.88→-2.21 dB、左-11.57→-3.19 dBまで改善した4)。
外科的介入の選択は患者の主症状・全身状態・施設の経験により個別に判断する。
髄液シャント術
対象:頭痛が顕著な場合に好まれる。VPS(脳室腹腔)またはLPS(腰椎腹腔)。
特徴:頭痛改善に優れる。即時成功率はONSFと同等。
注意点:長期再手術率50%超。シャント不全・感染・転位のリスクあり。
視神経鞘切開術(ONSF)
対象:視力障害が主な問題の場合に選択。
特徴:視力安定化に有効。頭痛改善効果は低い。
注意点:全体合併症リスク10〜15%(CRAO/CRVOによる視力喪失1〜2%含む)。視力安定後の再悪化率は1年で34%、3年で45%8)。
静脈洞ステント留置(VSS)
対象:横静脈洞狭窄がある場合。
特徴:頭蓋内圧の迅速な正常化が期待できる。
注意点:術後6ヶ月間の抗血小板療法が必要7)。妊婦における良好な成績が報告されている。
妊娠中のFIH管理:妊婦では体重管理が不可能であり、トピラマートは催奇形性のため禁忌である。アセタゾラミドとCSFドレナージを組み合わせた管理、または緊急VSSが選択肢となる6)7)。
Regev ら(2025)は、横静脈洞ステント留置を妊娠中の緊急FIIH 2例に施行した。症例1(23歳、体格指数 33.5、LPOP 360 mmH2O)では1ヶ月で乳頭浮腫が消失し視野が完全回復した。症例2(29歳、体格指数 39.5、LPOP 400 mmH2O)では右眼は完全回復、左眼に残存視野欠損を認めた7)。
アセタゾラミド最大4 g/日の単独投与でFIHが回復した報告がある4)。ただし、これは厳密な入院管理下で経過観察を継続した例であり、視力が悪化傾向にある場合は早急に外科的治療の検討が必要である。薬物療法のみで経過を見る場合は頻回の視力・視野検査が不可欠である。
妊娠中は体重減量が不可能であり、トピラマートは催奇形性のため禁忌となる6)。アセタゾラミドとCSFドレナージ(腰椎穿刺・ドレナージ)による管理が基本となる。静脈洞狭窄が確認された場合は緊急静脈洞ステント留置術(VSS)も選択肢に挙がり7)、良好な成績が報告されている。
特発性頭蓋内圧亢進症・劇症型の病態生理は完全には解明されていない。現在考えられている主な機序を以下に示す。
頭蓋内圧上昇の機序:頭蓋内は占拠性病変・CSF流出障害・静脈洞狭窄などにより圧が上昇する。圧-容積曲線はS字型を示し、脳脊髄液が約30 cm³増加するまではICPの変化は微小であるが、それを超えると急激に上昇する9)。
静脈洞狭窄との関係:IIH患者の90%以上に横静脈洞狭窄が同定されるが、これが原因なのか結果なのかは依然として議論の余地がある7)。静脈洞狭窄→静脈圧上昇→CSF吸収障害→ICP上昇という悪循環が提唱されている。
ホルモン・代謝的因子:アンドロゲン調節異常の関与が示唆されている8)。肥満に伴うインスリン抵抗性や副腎皮質ホルモンの代謝変化もCSF産生増加に寄与すると考えられる。
グリア神経血管界面の関与:近年、glia-neuro-vascular interface(グリア神経血管界面)の機能異常がIIH発症に関与している可能性が示唆されている9)。
FIH固有の病態:FIHの病態がIIHと異なるかどうかは依然として不明である。病態の違いが急速な進行を説明するのか、単に頭蓋内圧の絶対値や個体の感受性の差異によるものかは明らかになっていない。
FIHの定義を「4週間以内」という時間基準ではなく「視力脅威性(vision-threatening)」で定義すべきとの提案がなされている8)。時間基準では急速な進行にもかかわらず診断から漏れる症例が存在する可能性があり、定義の見直しが議論されている。
英国においてVSS(静脈洞ステント留置術)とVPS(脳室腹腔シャント術)を直接比較するランダム化比較試験(RCT)が進行中である8)。現時点では両術式の優劣は確立されておらず、施設の経験と個々の患者の特性に基づいて選択されている。
Aldhahwani ら(2024)はFIHと悪性高血圧が合併した4例を報告した3)。3/4例が男性、BMIは19.5〜36と幅広く、非肥満例を含んでいた。診断の遅延が平均3.2ヶ月に達し、最終視力は20/400〜光覚弁と極めて不良であった。迅速な診断の重要性と非典型例の存在を示す報告として注目される。
Selvaraj ら(2021)は中絶後の急性出血性貧血(Hb 4.9 g/dL)を契機に発症したFIHの1例を報告した5)。CSF開放圧は840 mmH2Oと極めて高く、輸血・メチルプレドニゾロン・アセタゾラミド・連続腰椎穿刺の併用により、右眼6/24・左眼(ONSF施行後)2/60まで視力が回復した。急性貧血がFIIHの誘因となりうることを示した稀な症例である。
11β-HSD1(11β-ヒドロキシステロイド脱水素酵素1型)阻害薬やオクトレオチドなど、特発性頭蓋内圧亢進症/劇症型の病態に関わる新規治療標的についての研究が進行中である6)。これらは標準治療としては確立されていない。