
フィンゴリモド関連黄斑浮腫
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. フィンゴリモド関連黄斑浮腫とは
Section titled “1. フィンゴリモド関連黄斑浮腫とは”フィンゴリモド(イムセラ/ジレニア)は、再発寛解型多発性硬化症(RRMS)に対する初の経口疾患修飾療法(DMT)である。スフィンゴシン-1-リン酸(S1P)受容体を調節し、リンパ球のリンパ節からの放出を阻止することで中枢神経系の自己免疫性脱髄を抑制する1)。
黄斑浮腫(ME)は本剤の重大な眼副作用であり、フィンゴリモド関連黄斑浮腫(FAME)と呼ばれる2)。日本では2011年に発売され、長期投与時の使用経験が少ないことから全例調査が承認条件として義務付けられている。海外臨床試験での黄斑浮腫発現率は0.5 mg/日で0.2%、1.25 mg/日で1.4%であった。一方、国内臨床試験では黄斑浮腫は認められなかった。
同クラスのより新しいS1P受容体モジュレーター(シポニモドなど)では、臨床試験において同様の黄斑浮腫リスクは報告されていない。
承認用量(0.5 mg/日)での発現率は海外臨床試験で0〜0.5%と低い。高用量(1.25 mg/日)では1〜1.6%に上昇する。国内臨床試験では未発現であった。詳細は「原因とリスク要因」の項を参照。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”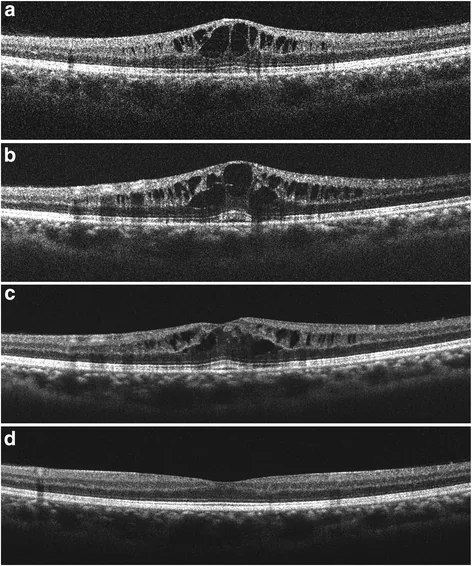
FAME患者が訴える主な症状は以下の通りである8)。
- 中心視力の低下・かすみ:最も多い訴えである。
- 色覚変化:色の見え方の異常を自覚する。
- 変視症:物が歪んで見える。
- 小視症:物が小さく見える。
- 暗点:相対的または絶対的な暗点を認める。
海外臨床試験で発現した黄斑浮腫例の多くは無症候性であった。投与開始3〜4か月後の定期検査で初めて発見される場合がある。
臨床所見(医師が診察で確認する所見)
Section titled “臨床所見(医師が診察で確認する所見)”- 視力低下:Snellenチャート等で測定する。
- コントラスト感度低下:Pelli-Robsonチャートなどで評価する。
- 色覚異常:色覚検査で検出する。
- 変視症:アムスラーチャートで確認する。
- 散瞳眼底検査所見:網膜肥厚、網膜内嚢胞、黄斑の色調変化を認める。緑色光で明瞭化することがある。
中等度〜重度ME(中心窩厚 >300 μm)は細隙灯顕微鏡検査で確認できる場合がある4)。軽度ME(中心窩厚 201〜300 μm)はOCTによる検出が必要である4)。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”FAMEの発症にはフィンゴリモドの用量・投与期間、患者の年齢・併存疾患が関与する。
主要な臨床試験における黄斑浮腫発現率を以下に示す。
| 試験・対象 | 0.5 mg群 | 高用量群 |
|---|---|---|
| FREEDOMS/TRANSFORMS試験(MS) | 0〜0.5% | 1〜1.6%(1.25 mg) |
| 腎移植試験(+シクロスポリン) | — | 1.3%(2.5 mg)/ 2.2%(5.0 mg) |
発現率は用量依存的であり、承認用量(0.5 mg/日)では低い10)11)12)。
発症時期は治療開始後3〜4か月以内が最多であるが、12か月以上経過後の発症も報告されている13)。2週間や2年という事例もある。
リスク因子は以下の通りである13)14)。
- 41歳超の年齢
- 糖尿病:腎移植試験では糖尿病患者の発現率30%に対し、非糖尿病患者では4%であった。
- 糖尿病網膜症
- ぶどう膜炎既往:MS臨床試験で未既往例0.6%に対し、既往例では約20%と著明に高率であった。
- 眼科手術の既往
- 網膜血管疾患
41歳超の高齢者、糖尿病(特に糖尿病網膜症を有する場合)、ぶどう膜炎の既往歴がある患者はリスクが高い。ぶどう膜炎既往例では発現率が約20%に達する。眼科手術歴や網膜血管疾患も危険因子である。
4. 診断と検査方法
Section titled “4. 診断と検査方法”薬剤誘発性黄斑浮腫の早期発見のため、投与開始3〜4か月後に眼底検査を含む眼科的検査が必須とされている。患者が視覚障害を訴えた場合にも検査が必要である。
- 光干渉断層計(OCT):非侵襲的で網膜の高解像度断層画像を提供する。網膜下液分布の定量的評価が可能であり、特に軽度MEにおいて細隙灯顕微鏡検査よりも感度が高い。スペクトラルドメインOCT(SD-OCT)による中心窩網膜厚測定が推奨される。
- 蛍光眼底造影(IVFA):早期相で中心窩周囲毛細血管拡張を認める。後期相では血管外へのフルオレセイン漏出を認め、血管透過性亢進を示す9)。OCTとIVFAはMEの検出に高い感度を有し、病因の特定にも有用である。
視覚障害を呈するMS患者では、視神経炎(ON)との鑑別が重要である4)。両者の鑑別点を以下に示す。
| 所見 | 黄斑浮腫(ME) | 視神経炎(ON) |
|---|---|---|
| 痛み | なし | 眼球運動時に増悪 |
| 変視症 | あり | 稀 |
| RAPD | なし | 一般的 |
| OCT | 黄斑肥厚 | 乳頭周囲網膜神経線維層(RNFL)肥厚→菲薄化 |
| IVFA | 黄斑部漏出 | 視神経乳頭漏出 |
| MRI | 正常 | 視神経の造影増強 |
5. 標準的な治療法
Section titled “5. 標準的な治療法”FAMEの管理は、フィンゴリモドの中止が第一選択である。通常、中止後6か月以内に消失する10)11)。早期発見が予後改善の鍵となる。
投与中止で多くの症例は改善する。ただし、改善しない症例も存在する。中止後の多発性硬化症の再燃リスク、2週間以上中止した場合の再導入時リスクにも留意が必要である。疾患修飾療法の中止・変更にあたっては、脱髄疾患悪化のリスクとの天秤が求められる。
フィンゴリモド中止以外に、FAMEの管理に関するコンセンサスは確立していない。消失促進に使用される薬剤は以下の通りである。
- 局所NSAIDs点眼:ネパフェナク、ブロムフェナク、ケトロラクなど。
- ステロイド:プレドニゾロン、デキサメタゾン、ジフルプレドナート、トリアムシノロン(点眼・結膜下・硝子体内投与)。
- 炭酸脱水酵素阻害薬:アセタゾラミド。
- 抗VEGF薬:ラニビズマブの硝子体内注射。
これらの多くはフィンゴリモド中止と併用されるが、中止せずに奏効した症例報告もある。ただし、FAME発生率が低いため、いずれの治療レジメンについても質の高いエビデンスは不足している。
モニタリング
Section titled “モニタリング”FDAは以下のモニタリングスケジュールを推奨している4)。
- 治療開始前:ベースライン眼科検査(視力・眼圧・散瞳眼底検査・OCT)
- 3〜4か月後:再検査
- 6か月後:再検査
- 以降:年1回
ぶどう膜炎・糖尿病の既往がある患者や、MEに関連する他の薬剤を使用している患者は、より綿密なモニタリングが必要である。
多くの症例は中止後6か月以内に消失する。しかし、改善しない難治例も存在し、局所NSAIDs・ステロイド・抗VEGF薬などの追加治療が必要となる場合がある。詳細は「標準的な治療法」の項を参照。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”黄斑浮腫は、網膜の外網状層および内顆粒層における液体蓄積を特徴とする。血液網膜関門(BRB)の破綻により、網膜組織へタンパク質が通過し、浸透圧の上昇から水分が貯留する3)。
BRBは2つの構成要素から成る。内BRBは網膜血管内皮細胞間の密着結合(TJ)が維持する。外BRBは網膜色素上皮(RPE)細胞間のTJが担う3)。BRB破綻の原因には、網膜血管不全、炎症、病的膜による牽引、網膜色素上皮障害、薬剤がある4)。
フィンゴリモドはS1Pの構造類似体である4)。活性代謝物フィンゴリモドリン酸がS1P1受容体およびS1P受容体に結合し、受容体の内在化・分解を介して機能的拮抗薬として作用する5)。治療効果はS1P1受容体への結合を通じたリンパ節でのT細胞貯留による。
FAMEの正確な機序は不明であるが、S1P1受容体拮抗がペリサイト(毛細血管周細胞)および内皮細胞間のTJを減少させ、BRBの血管透過性を亢進させることが推定されている4)6)。
Coplandら(2012)は、マウスぶどう膜炎モデルにおいてフィンゴリモド治療量投与が網膜炎症を速やかに抑制し、マクロファージおよびCD4+ T細胞の浸潤を減少させ、血液眼関門を維持することを報告した7)。この結果はフィンゴリモドが眼内炎症を抑制する側面を持つ一方で、S1P受容体への作用を介してBRB破綻を惹起しうるという二面性を示唆するものである。
フィンゴリモドの活性代謝物がS1P1受容体に拮抗し、血管内皮細胞間の密着結合(TJ)を減少させる。これにより血液網膜関門の透過性が亢進し、網膜に液体が蓄積して黄斑浮腫が生じると考えられている。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”FAMEの発生率が低いため、治療レジメンに関する質の高いエビデンスは不足している。現時点で確立されたコンセンサスはない。
フィンゴリモドを中止せずにNSAIDs点眼やステロイドで黄斑浮腫を管理できた症例報告が散見される。MS治療の継続が不可欠な患者において、薬剤継続下でのFAME管理戦略は今後の重要な検討課題である。
シポニモドなど新世代のS1P受容体モジュレーターでは、臨床試験で同様の黄斑浮腫リスクが報告されていない。受容体選択性の違いがMEリスクに与える影響の解明は今後の研究課題である。
8. 参考文献
Section titled “8. 参考文献”- Chun J, Hartung HP. Mechanism of action of oral fingolimod (FTY720) in multiple sclerosis. Clin Neuropharmacol. 2010;33(2):91-101.
- Zarbin MA, Jampol LM, Jager RD, et al. Ophthalmic evaluations in clinical studies of fingolimod (FTY720) in multiple sclerosis. Ophthalmology. 2013;120(7):1432-1439.
- Tranos PG, Wickremasinghe SS, Stangos NT, et al. Macular edema. Surv Ophthalmol. 2004;49(5):470-490.
- Jain N, Bhatti MT. Fingolimod-associated macular edema: incidence, detection, and management. Neurology. 2012;78(9):672-680.
- Brinkmann V, Billich A, Baumruker T, et al. Fingolimod (FTY720): discovery and development of an oral drug to treat multiple sclerosis. Nat Rev Drug Discov. 2010;9(11):883-897.
- Tomkins-Netzer O, Lightman S, Engel BC, et al. Blood-retinal barrier disruption in inflammation and malignancy. Prog Retin Eye Res. 2024;99:101245.
- Copland DA, Liu J, Schewitz-Bowers LP, et al. Therapeutic dosing of fingolimod (FTY720) prevents cell infiltration, rapidly suppresses ocular inflammation, and maintains the blood-ocular barrier. Am J Pathol. 2012;180(2):672-681.
- Afshar AR, Fernandes JK, Engorn HM, et al. Fingolimod-associated macular edema resolved with corticosteroid and cyclosporine. Mult Scler Relat Disord. 2013;2(2):155-158.
- Saab G, Bhatti MT, Katz BJ, et al. Fluorescein angiography and optical coherence tomography imaging of fingolimod-associated macular edema. Retin Cases Brief Rep. 2014;8(4):287-291.
- Kappos L, Radue EW, O’Connor P, et al. A placebo-controlled trial of oral fingolimod in relapsing multiple sclerosis (FREEDOMS). N Engl J Med. 2010;362(5):387-401.
- Cohen JA, Barkhof F, Comi G, et al. Oral fingolimod or intramuscular interferon for relapsing multiple sclerosis (TRANSFORMS). N Engl J Med. 2010;362(5):402-415.
- Tedesco-Silva H, Mourad G, Kahan BD, et al. FTY720, a novel immunomodulator: efficacy and safety results from the first phase 2A study in de novo renal transplantation. Transplantation. 2004;77(12):1826-1833.
- Nolan R, Gelfand JM, Green AJ. Fingolimod treatment in multiple sclerosis leads to increased macular volume. Neurology. 2013;80(2):139-144.
- Minuk A, Belliveau MJ, Bhargava R, et al. Fingolimod-associated macular edema: resolution by sub-tenon injection of triamcinolone with continued fingolimod use. JAMA Ophthalmol. 2013;131(6):802-804.
