脂肪増殖型
別名:タイプI、adipogenic型
特徴:主に脂肪の拡大と上眼瞼挙筋の瘢痕化を呈する。TED患者の約2/3を占める。
DONとの関連:重度の眼球突出による視神経伸展が生じない限り、DONに至ることは稀である。

甲状腺視神経症(dysthyroid optic neuropathy: DON)は、甲状腺眼症(thyroid eye disease: TED)に伴う視神経機能障害である。TEDはバセドウ眼症(Graves orbitopathy: GO)とも呼ばれる自己免疫疾患で、外眼筋および眼窩内脂肪の腫大により眼窩内圧が上昇し、視神経が圧迫されることで生じる。TEDの中で最も重篤な合併症の一つであり、未治療で放置すると永久的な視力喪失に至る可能性がある。
TED全症例の0.9〜8.6%にDONが発症し1)、約70%が両眼性に生じる。半数以上は矯正視力0.5以上を保つが、最悪の場合は失明に至ることもある。適切な治療を行えば視機能の回復が期待できるため、早期診断が極めて重要である。
DONを発症するのはTED全症例の3〜8%程度であり、大多数のTED患者ではDONに至らない。ただし筋腫大型の表現型や喫煙・高齢などのリスク要因がある場合は注意が必要である。詳細は「原因とリスク要因」の項を参照。
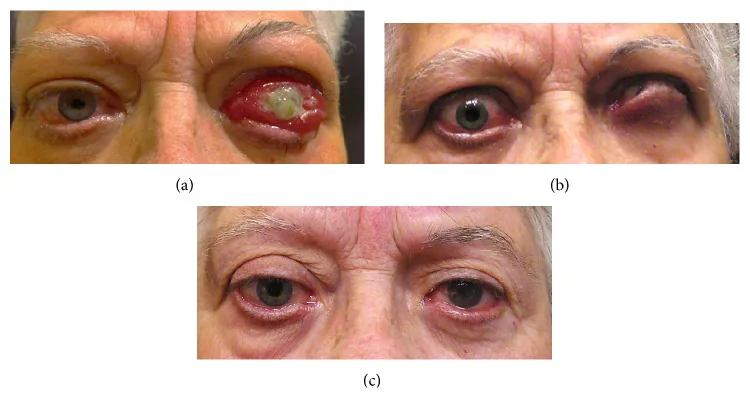
DONの初発症状は、中心視力のぼやけと色の鮮やかさの低下(彩度低下)である。視力低下の程度は軽微なものから光覚消失まで多様であるが、半数以上は視力0.5以上を保つ。
主な自覚症状を以下に示す。
DONの主な臨床所見とその出現頻度を以下に示す。
| 臨床所見 | 出現頻度 |
|---|---|
| 視力低下 | 約80% |
| 色覚低下 | 約77% |
| 視野欠損 | 約71% |
| 眼球運動制限 | 約70% |
| 視神経乳頭浮腫 | 約20% |
その他の重要な臨床所見を以下に列挙する。
DON症例の76%は両側性であり、乳頭腫脹は約半数で認められない。乳頭に異常を認めない場合でもDONは生じうるため、視機能検査と画像診断の組み合わせが不可欠である。
TEDは、眼窩線維芽細胞の表面にあるTSH受容体およびIGF-1受容体に対する自己抗体が原因で生じる自己免疫疾患である。抗体結合により脂肪分化、Tリンパ球活性化、サイトカイン放出が生じ、眼窩脂肪・筋肉にグリコサミノグリカン(GAG)が沈着する。
TEDは2つの表現型に大別される。
脂肪増殖型
別名:タイプI、adipogenic型
特徴:主に脂肪の拡大と上眼瞼挙筋の瘢痕化を呈する。TED患者の約2/3を占める。
DONとの関連:重度の眼球突出による視神経伸展が生じない限り、DONに至ることは稀である。
筋腫大型
別名:タイプII、myopathic型
特徴:外眼筋の肥大を伴い、うっ血性軟部組織徴候や眼球運動障害を呈する。TED患者の約1/3を占める。
DONとの関連:眼窩尖端部での視神経圧迫が生じやすく、DONの主要な原因となる。
TED自体は女性に多く(男女比1:4)、DONは高齢の男性に多い傾向がある。主なリスク要因を以下に示す。
甲状腺機能異常はTEDの重症度と相関するが、DONの発症や重症度との間には明確な相関がないとされている。また、甲状腺自己抗体がすべて陰性であってもDONは発症しうる。
喫煙はTEDの進行およびDON発症の最も重要なリスク要因とされる。放射性ヨウ素治療後のTED悪化リスクも喫煙者で高い。禁煙によりTEDの治療抵抗性も低下することが知られている。
DONの診断は、TED患者における視神経機能障害の確認と、画像診断による眼窩尖端部の圧迫所見に基づく。
DONの確定診断および手術計画において画像診断は必須である。
| 検査 | 主な利点 |
|---|---|
| CT | 骨の描出に優れる。手術計画に最適 |
| MRI(STIR) | 炎症活動性の評価に有用 |
最近DONを発症した患者の96%が高力価の甲状腺刺激免疫グロブリン(TSI)を有していたとの報告がある。ただし、自己抗体がすべて陰性でもDONは発症しうるため、血清学的検査のみでの除外診断はできない。
CTは骨の描出に優れ、迅速・安価に撮影でき、手術計画にも適するため第一選択となることが多い。一方、MRIのSTIRシーケンスは炎症活動性の評価に優れる。両者は相補的であり、状況に応じて使い分ける。
DONの第一選択治療はステロイドパルス療法(またはハーフパルス療法)である。
EUGOGOガイドライン(2021年)では、1日最大1 gを3日間投与し、改善傾向があれば必要に応じて毎週繰り返す高用量投与を推奨している。
外部放射線照射療法(EBRT)はリンパ球と線維芽細胞を標的として炎症を抑制する。即効性がないため急性期治療として単独で用いることはなく、ステロイド療法の補助として位置づけられる。ステロイドとの併用により、DON発症予防効果が報告されている。
ステロイドパルス療法開始後2週間以内に視神経機能の改善が見られない場合は、緊急眼窩減圧術が検討される。日本ではDON患者の22〜38%が眼窩減圧術を施行されている1)。
手術アプローチには以下がある。
眼窩尖端部の容積拡大により視神経の減圧を図り、内側壁・眼窩底・深い外側壁を対象とする。術前のCT計画および術中ナビゲーションが有用である。
放射性ヨウ素(RAI)治療は、既存のTED患者の最大20%で症状を悪化させる可能性がある。RAI前の経口プレドニゾンによる予防投与が推奨される。RAI後のTED悪化に関連する因子として、喫煙、治療前のT3高値、治療後の甲状腺機能低下症、筋腫大型疾患が挙げられる。
適切な治療を行えば、約70%以上の患者で視機能の回復が得られる。外科的減圧術を行った場合の方が、完全な視力回復の確率はより高い。
パルス療法開始後2週間以内に視神経機能の改善が見られない場合は、緊急眼窩減圧術が検討される。日本ではDON患者の22〜38%が眼窩減圧術を施行されている1)。
DONの発症には複数のメカニズムが関与する。
TEDの根本的な病態としては、眼窩の多分化能を有する線維芽細胞のTSH受容体およびIGF-1受容体に自己抗体が結合することにより、以下のカスケードが生じる。
これらの過程の結果、眼窩内の容積が増大し、骨性眼窩の制約のもとで視神経の圧迫または伸展が生じる。
テプロツムマブはIGF-1受容体(IGF-1R)の細胞外領域に特異的に結合し、TEDにおける免疫反応を阻害するモノクローナル抗体である。
Congら(2024)は5件のRCT(計411例)を対象としたメタ解析で、テプロツムマブがプラセボと比較して眼球突出の有意な減少、臨床活動スコア(CAS)の改善、および複視の改善をもたらすことを報告した。有害事象および重篤な有害事象のリスクはプラセボ群と有意差がなかった2)。
DONに対しても、ステロイド・放射線治療・手術に抵抗性であった症例でテプロツムマブが有効であったとする観察研究が複数報告されている。日本人患者におけるテプロツムマブの有効性については、今後の研究が期待される1)。
いずれもDONに対する有効性のエビデンスは限定的であり、さらなる研究が必要である。
Mizuochiら(2025)は、甲状腺機能低下症からバセドウ病へ移行しDONを発症した55歳女性の症例を報告した。3クールの1 gパルス療法後にDONへ進行したが、追加パルス療法で視力は回復した。しかし疾患活動性は4年以上持続し、計5回の増悪を経験した。外来での0.5 g週1回パルス療法を繰り返し、メチルプレドニゾロンの累積投与量は59.5 gに達したが重篤な副作用は認めなかった1)。
この報告は、DONの長期管理における慎重なモニタリング(CAS・TSAb・眼窩MRI)の重要性を示唆している。
現時点でテプロツムマブはDONに対する標準治療としては確立されていない。しかし、ステロイドや放射線治療に抵抗性のDON症例で有効であった観察研究が複数報告されており、今後の研究が期待される。