ポートワイン血管腫の分布とリスク
V1領域のみ:緑内障リスク6.7%
V2領域のみ:緑内障リスクはほぼなし
V1+V2領域:緑内障リスク31.8%と大幅に上昇
V1+V2+V3領域:神経症状リスクが4倍に増加

スタージ・ウェーバー症候群(Sturge-Weber Syndrome: SWS)は、脳三叉神経血管腫症(encephalotrigeminal angiomatosis)とも呼ばれる先天性の神経皮膚症候群(母斑症)である。三叉神経領域の顔面ポートワイン血管腫(火炎状母斑)、同側の脳軟膜血管腫、眼の血管腫を三主徴とする。
発生頻度は出生50,000人に1人とまれな疾患であり、人種・性別による偏りはない5)7)。ほとんどが孤発例である。GNAQ遺伝子の体細胞モザイク変異が原因であり、胎生期の交感神経障害による血管発生異常と考えられている4)5)。
| 分類(Roach) | 特徴 |
|---|---|
| I型(古典型) | PWS+神経症状+緑内障 |
| II型 | PWS+緑内障(神経病変なし) |
| III型(最稀) | 髄膜血管腫のみ |
緑内障は母斑症の中でSWSにおいて最も高い発症率を示す2)。
三叉神経領域の顔面ポートワイン血管腫、同側の脳軟膜血管腫、眼血管腫を三主徴とする先天性の神経皮膚症候群である。GNAQ遺伝子の体細胞モザイク変異が原因であり、遺伝性ではなくほとんどが孤発例である4)。てんかん(約80%)、知的障害、片麻痺などの神経症状と、緑内障(30〜70%)が主要な合併症である。三主徴が揃わない不完全例も存在する。
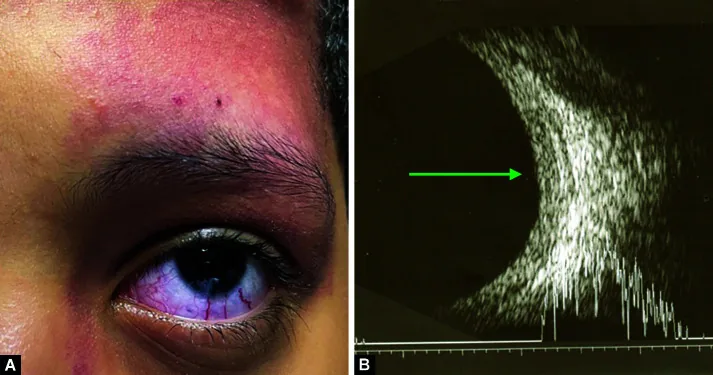
先天性の早期発症型では流涙・羞明・眼瞼けいれんが初発症状となる。角膜径増大や角膜混濁による視力障害を呈する。晩期発症型は原発開放隅角緑内障と類似し、初期には自覚症状に乏しい。
眼所見:緑内障が最も重要な眼合併症であり、眼瞼に血管腫が及んでいる場合に30〜70%の高頻度で発症する1)。約60%が生直後〜4歳までの早期発症型で、残りは幼児期以降の晩期発症型である。結膜・上強膜の血管拡張と蛇行、脈絡膜血管腫(約60%に合併)、網膜血管の蛇行がみられる。
全身所見:出生時より顔面の三叉神経第1枝・第2枝領域にポートワイン血管腫(火炎状母斑)が存在する。通常片側性であるが両側性もある7)。3歳までに高頻度(75〜90%)にてんかん発作を生じ、精神発達遅滞、片麻痺、同名半盲をきたすことがある。髄膜血管腫により大脳皮質の萎縮・石灰化が生じる。
55歳で初回てんかん発作を呈した成人発症例も報告されており、顔面外のポートワイン血管腫を伴う非典型例では診断が遅れることがある5)。
SWSはGNAQ遺伝子の体細胞モザイク変異(post-zygotic mutation)が原因である4)5)。この変異により内皮細胞の無制御な増殖と血管奇形が生じる。遺伝性ではないため、分子診断には罹患組織(通常は皮膚)の生検が必要である4)。
ポートワイン血管腫の分布とリスク
V1領域のみ:緑内障リスク6.7%
V2領域のみ:緑内障リスクはほぼなし
V1+V2領域:緑内障リスク31.8%と大幅に上昇
V1+V2+V3領域:神経症状リスクが4倍に増加
発症時期と病因の違い
早期発症型(約60%):隅角の発育異常が主因。牛眼・角膜径増大を呈する1)
晩期発症型(約40%):上強膜静脈圧の上昇と脈絡膜血管腫の関与が主因1)
眼瞼侵襲:血管腫が眼瞼に及ぶ場合、緑内障発症率が著明に上昇する
両側性PWS:片側性と比較してSWSである可能性が高い7)
SWSに伴う緑内障の診断には精密な眼圧検査と前眼部・隅角・眼底検査が重要である。小児では全身麻酔下検査が必須となる場合が多い。
眼圧測定:小児ではGoldmann眼圧計が使用困難な場合が多く、反跳式眼圧計が有用である。角膜浮腫や角膜菲薄化により測定値の解釈に注意を要する。
隅角検査:病型診断と治療法の選択に不可欠である。早期発症型では隅角形成不全(虹彩根部が正常より高位に付着)がみられる。晩期発症型では隅角内に血液が観察されることがあり、上強膜静脈圧上昇を示唆する。
脈絡膜血管腫の診断:蛍光眼底造影が有用であり、早期に大型の脈絡膜血管パターンが見られ、後期に腫瘍部分全体が過蛍光を示す。びまん性脈絡膜血管腫は通常の眼底検査では同定困難な場合がある。
全身検査:頭部CTで脳皮質内の石灰化を検出する。石灰化のない段階でも造影MRIやSPECTにより脳病変は検出可能である。
顔面ポートワイン血管腫を認める患者では眼圧測定を含む定期的な眼科検査が不可欠である。小児では反跳式眼圧計による眼圧測定、前眼部検査(角膜径・角膜混濁・Haab線の有無)、隅角検査(隅角形成異常の評価)、眼底検査(乳頭陥凹の評価)を行う。小児では全身麻酔下検査が必要となることが多い。晩期発症型では隅角内の血液の有無や上強膜の血管拡張が鑑別に有用である。
先天性や乳幼児期発症の緑内障には手術治療が必要である1)。線維柱帯切開術や隅角切開術を第一選択とする1)。ただし成功率は原発先天緑内障より低く、追加手術が必要になることが多い。
年長者では上強膜静脈圧が上昇しているため、薬物治療が第一選択となる1)。房水産生抑制薬が最も有効とされる。プロスタグランジン関連薬の反応は一貫していない。
濾過手術・チューブシャント
濾過手術:薬物治療や流出路再建術が奏功しない場合に考慮する1)。代謝拮抗薬併用で成績が向上しうる
チューブシャント手術:Ahmedデバイスで24ヶ月時成功率79%。2段階Baerveldtデバイスでは全例で21 mmHg未満を達成した報告がある
2段階法の利点:チューブ挿入前にプレートに被膜を形成させることで低眼圧リスクを軽減できる
術中・術後合併症への対策
脈絡膜出血・滲出:脈絡膜血管腫を伴う場合、手術による眼圧下降で脈絡膜剥離・出血のリスクが高い1)
予防措置:術前の高浸透圧薬による眼圧下降、後部強膜切開術、強膜弁縫合の事前配置または強固な追加縫合
毛様体光凝固術:難治性緑内障や手術合併症の高リスク例で考慮する。62.5%で合併症なく眼圧コントロールが得られた報告がある
流出路再建術(線維柱帯切開術)がステロイド緑内障に有効であるように、SWSの隅角形成異常に対しても隅角手術が有効な場合がある1)。
最も重要な注意点は脈絡膜血管腫に関連する手術合併症である。SWSでは脈絡膜血管腫の合併が約60%に見られ、緑内障手術による急激な眼圧下降が脈絡膜滲出・出血・網膜剥離を引き起こすリスクがある1)。予防策として術前の高浸透圧薬投与、後部強膜切開術の施行、強膜弁の強固な縫合、バルブ付きまたは2段階式ドレナージデバイスの使用が推奨される。また小児では交感神経α2受容体作動薬が2歳未満で禁忌であることにも注意を要する1)。
SWSの早期発症型緑内障は前房隅角の先天性形成異常に起因する。摘出眼の組織学的検討では、広いぶどう膜線維柱帯、線維柱帯に直接付着した毛様体筋、未発達の強膜突起、前方付着した虹彩根部が確認されている。これらの所見は原発先天緑内障で見られるものと類似する。
晩期発症型では上強膜静脈圧の上昇が主要な眼圧上昇機序である1)。眼表面および眼窩内の血管腫により静脈還流が障害され、房水流出に対する抵抗が増大する。隅角鏡検査では隅角異常は最小限であるが、隅角内の血液が観察されることが多い。
両者は緑内障の発症機序が根本的に異なるためである。早期発症型は隅角の先天性形成異常が主因であり、線維柱帯や隅角構造自体に問題があるため、流出路を物理的に開放する隅角手術(線維柱帯切開術・隅角切開術)が有効である1)。一方、晩期発症型は上強膜静脈圧の上昇が主因であり、隅角構造自体は比較的正常に近い。上強膜静脈圧が高い状態では房水産生抑制薬が最も有効であり、薬物治療が第一選択となる1)。薬物治療が無効な場合は、上強膜静脈系をバイパスできる濾過手術を考慮する。
SWSに伴う緑内障の管理は以下の点で今後の進展が期待される。
- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm, Savona. 2020.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
- Patel A, Hayward JD, Taez V, et al. Genetic Basis of Childhood Glaucoma. Ophthalmology. 2022;129(7):P819-P834.
- Yadav PS, Adhikari P, Mehta B, et al. Unmasking Sturge-Weber Syndrome in Adulthood: A Case with Extrafacial Port-Wine Stain and Delayed Neurological Symptoms. Ann Med Surg. 2024;86:3679-3682.
- Ainuz BY, Wolfe EM, Wolfe SA. Surgical Management of Facial Port-Wine Stain in Sturge Weber Syndrome. Cureus. 2021;13(1):e12637.
- Pathak BD, Sharma S, Adhikari A, et al. Sturge-Weber Syndrome with Bilateral Port-Wine Stain. Case Rep Pediatr. 2022;2022:2191465.