急性発作時の所見
眼圧:40 mmHgを超え、80 mmHgに達することもある1)2)
角膜:実質浮腫と微小嚢胞状浮腫を認める2)
瞳孔:中等度散瞳で対光反射が減弱・消失する2)3)
前房:中心部はある程度の深さを保つが周辺部が浅い。前房内炎症を伴う2)
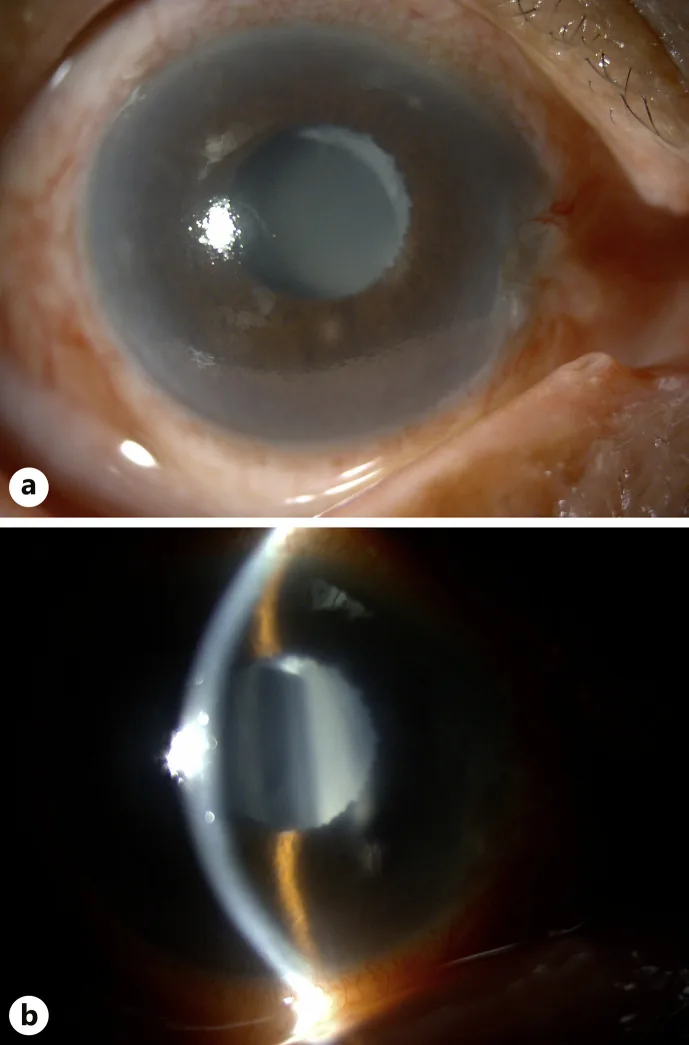
緑内障斑:水晶体前嚢下の壊死。過去の発作を示唆する所見である2)
隅角:広範な虹彩線維柱帯接触を認める2)3)

閉塞隅角緑内障(ACG)は前房隅角の並置閉塞または癒着閉塞により房水流出が障害され、眼圧上昇と視神経障害を生じる疾患群である1)2)。原発性と続発性のいずれも急性発作と慢性経過の両方をとりうる。
原発閉塞隅角疾患(PACD)は以下のように段階的に分類される1)。
40歳以上で有病率が増加する1)4)。多治見スタディではPACGの有病率は0.6%、久米島スタディでは2.2%と地域差が認められる。東アジア系・イヌイット系で特に有病率が高い4)。女性に好発する4)。
原発閉塞隅角緑内障の有病率は人種・民族間で大きく異なる4)。東アジア系やイヌイット系で最も高い有病率が報告されている4)。これは眼軸長・前房深度・水晶体厚・角膜曲率など解剖学的特徴の人種差に起因すると考えられている。日本国内でも地域差があり、多治見(0.6%)と久米島(2.2%)で約3.7倍の差がある。
解剖学的狭隅角のみの場合や慢性閉塞隅角の場合は通常無症状である。末期になって初めて視力低下や視野欠損を自覚する。
急性閉塞隅角発作では劇的な症状を呈する1)2)。視力低下・霧視・虹視症(光の周りのハロー)が出現する1)2)。激しい眼痛と頭痛を伴い、悪心・嘔吐などの迷走神経症状を生じることがある1)2)。
急性発作時の所見
眼圧:40 mmHgを超え、80 mmHgに達することもある1)2)
角膜:実質浮腫と微小嚢胞状浮腫を認める2)
瞳孔:中等度散瞳で対光反射が減弱・消失する2)3)
前房:中心部はある程度の深さを保つが周辺部が浅い。前房内炎症を伴う2)
緑内障斑:水晶体前嚢下の壊死。過去の発作を示唆する所見である2)
隅角:広範な虹彩線維柱帯接触を認める2)3)
続発性ACGの鑑別所見
| リスク因子 | 概要 |
|---|---|
| 遠視 | 短眼軸による浅前房4) |
| 加齢 | 水晶体厚の増加1)4) |
| 女性 | 男性より好発4) |
| アジア系・イヌイット系 | 解剖学的特徴4) |
| 家族歴 | 眼軸長や屈折の遺伝4) |
| 浅前房・短眼軸・厚い水晶体 | 解剖学的素因4) |
続発性の原因は多岐にわたる1)2)。虹彩を後方から前方に押し出す機序(膨隆水晶体・水晶体脱臼・毛様体脈絡膜滲出・房水流向異常・後眼部腫瘍など)と、虹彩を引き寄せて線維柱帯に接触させる機序(炎症性膜の収縮・ICE症候群・線維性増殖など)に大別される。
薬剤誘発性ACGではトピラマートなどスルホンアミド系薬剤が毛様体脈絡膜滲出を引き起こし、毛様体の前方回旋と虹彩-水晶体隔壁の前方移動により隅角閉塞を生じる6)7)8)。アセタゾラミドも同様の特異的反応を引き起こしうることが報告されている10)。
トピラマートは毛様体脈絡膜滲出を引き起こし、毛様体の前方回旋と虹彩-水晶体隔壁の前方移動により両眼性の急性隅角閉塞を生じる6)7)8)。投与開始後2週間以内に発症することが多いが、中止後にも発症しうる6)。UBMで毛様体の前方回旋と脈絡膜滲出が確認される8)。治療はトピラマートの中止、アトロピン点眼、ステロイド点眼、眼圧下降薬の投与である6)7)。レーザー虹彩切開術は無効であり、縮瞳薬は病態を悪化させるため禁忌である。
隅角鏡検査はACG診断のゴールドスタンダードである1)2)。圧迫隅角鏡を用いて並置閉塞と癒着閉塞を鑑別する。原発性では上方にPASが形成されやすく、炎症性の続発性では下方にPASが形成されやすい傾向がある。
UBM(超音波生体顕微鏡)は毛様体の形態・位置、脈絡膜滲出の有無を評価でき、続発性の原因検索に有用である8)10)。前眼部OCTは隅角構造の客観的定量評価に用いられる。
van Herick法による前房深度評価は簡便な狭隅角スクリーニング法である1)。角膜厚と周辺部前房深度の比が1/4未満であれば隅角鏡検査を行うべきである1)。
薬剤誘発性が疑われる場合はUBMとBスキャンで毛様体脈絡膜滲出を確認する6)8)10)。網膜色素変性の合併が疑われる場合は全視野網膜電図を施行する5)。ARB(常染色体劣性ベストロフィノパチー)ではEOGで特徴的な光上昇の消失を認める9)。
急性原発閉塞隅角の治療は以下の順で行う1)。
LPIは瞳孔ブロックの解消に有効な第一選択である1)2)。角膜が十分に透明な状態で施行する1)。不透明な角膜を通してのレーザー照射は水疱性角膜症のリスクがある1)。片眼に原発閉塞隅角緑内障/原発閉塞隅角症が認められた場合、僚眼にも予防的LPIを行う1)。
水晶体摘出は瞳孔ブロックを根本的に解消する1)。隅角開大効果と眼圧下降効果が得られる1)。PASが広範囲の場合は眼圧下降効果が限定的である1)。
プラトー虹彩にはLPIのみでは不十分であり、レーザー隅角形成術(レーザー周辺虹彩形成術)により虹彩根部を収縮させる1)。水晶体摘出による隅角開大も有効である1)。
| 治療法 | 適応 |
|---|---|
| LPI | 瞳孔ブロック1) |
| 水晶体摘出 | 瞳孔ブロック・水晶体因子1) |
| ALPI | プラトー虹彩1) |
| 隅角癒着解離術 | 広範PAS(50%以上)1) |
続発性では原因疾患の治療が最優先である1)2)。薬剤誘発性では原因薬の中止が最も重要であり、アトロピン点眼による毛様体弛緩とステロイドによる消炎を行う6)7)8)。縮瞳薬は水晶体前方移動を助長するため禁忌である。悪性緑内障ではアトロピン点眼と硝子体切除術が治療の中心となる1)。
水晶体摘出は瞳孔ブロックの根本的解消に有効である1)。水晶体を除去することで前房が深くなり隅角が開大する。白内障手術適応のある症例では一石二鳥の効果が期待できる。ただしPASが広範囲に形成されている場合は眼圧下降効果が限定的であり、隅角癒着解離術の併用が推奨される1)。急性期の水晶体摘出は合併症リスクが高いため熟練した術者が行うべきである1)。
原発閉塞隅角緑内障の大部分は相対的瞳孔ブロックによる1)2)3)。後房から前房への房水流出抵抗の増大により虹彩が前方膨隆し、線維柱帯を閉塞する1)。瞳孔ブロックのリスクは中等度散瞳時に最大となる3)。
原発閉塞隅角の成因には複数のメカニズムが複合的に関与する1)。(1)相対的瞳孔ブロック、(2)プラトー虹彩、(3)水晶体因子(加齢による水晶体厚の増加)、(4)水晶体後方因子(毛様体・脈絡膜・硝子体)である1)。
プラトー虹彩配置では前方に位置する毛様突起が虹彩基部を前方に押し出し、中心前房深度は正常であるにもかかわらず隅角閉塞を生じる1)。
押し出し機序
瞳孔ブロック型:膨隆水晶体、水晶体脱臼、小球状水晶体による虹彩の前方押し出し2)3)。虹彩後癒着による絶対的瞳孔ブロック2)
毛様体脈絡膜型:薬剤(トピラマート)による毛様体脈絡膜滲出と毛様体の前方回旋6)7)8)。後眼部腫瘍や漿液性網膜剥離による押し出し
房水流向異常型:硝子体の前方偏位により前房が全体的に浅くなる。悪性緑内障とも呼ばれる1)
引き寄せ機序
炎症性膜の収縮:ぶどう膜炎に伴うPAS形成。虹彩新生血管による線維血管膜の収縮2)
ICE症候群:角膜内皮の異常増殖による線維柱帯閉塞1)
外傷・手術関連:上皮増殖、線維性増殖、虹彩の創部への嵌入2)
Luらは若年の網膜色素変性(RP)患者3例にPACGが合併した症例を報告した5)。RP患者では一般集団と比較してACG発症リスクが3.64倍高いとされる5)。短眼軸、水晶体厚の増加、チン小帯の脆弱性がACGの解剖学的素因となる5)。ZNF408遺伝子の新規変異がRP合併PACG患者で同定された5)。RP患者には定期的な隅角鏡検査と眼圧モニタリングが推奨される5)。
トピラマート誘発性ACGの複数の症例報告が集積されている6)7)8)。典型例では投与開始後1〜2週間で両眼性に発症し、毛様体脈絡膜滲出とそれに続く毛様体の前方回旋が機序である8)。Tyagiらは前房蓄膿を伴うぶどう膜炎と脈絡膜剥離を呈した2例を報告し、トピラマートが重篤な眼内炎症を引き起こしうることを示した7)。中止後にも発症しうることが報告されている6)。
Kaisariらの文献レビューでは1956年以降23例のアセタゾラミド誘発性近視化が報告されている10)。中央値500 mg投与後中央値24時間で発症し、約1/3が隅角閉塞を合併する10)。この反応は用量非依存性の特異的反応であり、初回投与でも発生する10)。薬剤中止と毛様体麻痺薬により中央値5日で完全回復する10)。
常染色体劣性ベストロフィノパチー(ARB)の50%以上に閉塞隅角緑内障が合併するとされる9)。Rajaらは38歳女性のARB合併ACGで進行した視神経障害を報告し、LPIのみでは眼圧コントロールが困難であったためマイクロパルス経強膜毛様体光凝固術を施行した9)。
- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. Br J Ophthalmol. 2021.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
- American Academy of Ophthalmology. Primary Angle-Closure Disease Preferred Practice Pattern®. 2020.
- Lu Z, Wang L, Ying X, et al. Bilateral angle closure glaucoma with retinitis pigmentosa in young patients: case series. BMC Ophthalmology. 2023;23:458.
- Alzendi NA, Badawi AH, Alhazzaa B, et al. Topiramate-induced angle closure glaucoma: two unique case reports. Saudi J Ophthalmol. 2020;34:202-204.
- Tyagi M, Behera S, Senthil S, et al. Topiramate induced bilateral hypopyon uveitis and choroidal detachment: a report of two cases and review of literature. BMC Ophthalmology. 2021;21:287.
- AlNaqeeb O, Aljohani S, Alshehri A. Topiramate-induced acute bilateral angle closure glaucoma confirmed by ultrasound biomicroscopy. Saudi J Ophthalmol. 2020;34:316-318.
- Raja V, Manthravadi SK, Anjanamurthy R. Angle-closure glaucoma associated with autosomal recessive bestrophinopathy. Indian J Ophthalmol. 2022;70:2657-2658.
- Kaisari E, Abouzeid H, Magnin L, et al. Acute myopic shift after a single dose of acetazolamide: a case report and review of the literature. Klin Monatsbl Augenheilkd. 2024;241:554-558.