超音波生体顕微鏡(UBM)
原理:50〜100 MHzの高周波超音波を用いたBモード超音波で前眼部の断層像を得る3)。接触式検査であり点眼麻酔が必要である
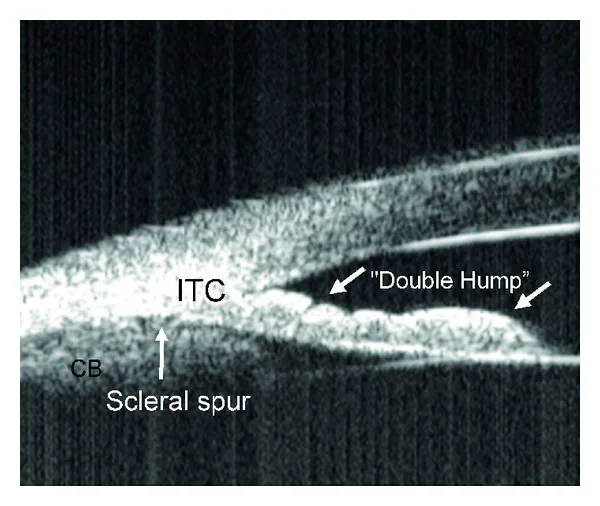
利点:光を使用しないため暗室散瞳状態での隅角撮影が可能。虹彩裏面・毛様体まで描出でき、プラトー虹彩や毛様体腫瘍の診断に有用3)
定量パラメータ:隅角開放距離(AOD)、線維柱帯虹彩角(TIA)、線維柱帯毛様体突起間距離(TCPD)
限界:接触式であり検者の習熟を要する。解像度はAS-OCTに劣る。照明条件や調節が画質に影響する

緑内障は世界における不可逆的な視力障害の主要な原因である。眼圧(IOP)の上昇は緑内障の最も重要なリスク因子であり、房水の流出障害がその主因となる4)。
房水は毛様体で産生され、主流出路(線維柱帯→シュレム管→集合管→房水静脈→上強膜静脈)と副流出路(ぶどう膜強膜流出路)から排出される。主流出路が総流出量の80%以上を担う4)。傍シュレム管結合組織(JCT)とシュレム管が房水流出抵抗の主要部位である1)4)。
近年のMIGSの台頭に伴い、房水流出路の画像診断への関心が高まっている。流出路の術前評価により最適な治療標的の特定が可能となり、個別化された術式選択に寄与する可能性がある。
隅角鏡検査(gonioscopy)は前房隅角評価のゴールドスタンダードである2)。これを補完する画像診断法として超音波生体顕微鏡・AS-OCT・隅角写真撮影がある。
超音波生体顕微鏡(UBM)
原理:50〜100 MHzの高周波超音波を用いたBモード超音波で前眼部の断層像を得る3)。接触式検査であり点眼麻酔が必要である
利点:光を使用しないため暗室散瞳状態での隅角撮影が可能。虹彩裏面・毛様体まで描出でき、プラトー虹彩や毛様体腫瘍の診断に有用3)
定量パラメータ:隅角開放距離(AOD)、線維柱帯虹彩角(TIA)、線維柱帯毛様体突起間距離(TCPD)
限界:接触式であり検者の習熟を要する。解像度はAS-OCTに劣る。照明条件や調節が画質に影響する
前眼部OCT(AS-OCT)
原理:低コヒーレンス干渉法を用いて前眼部構造の高解像度断層像を得る3)。非接触・非侵襲で短時間の撮影が可能
利点:解像度・定量性に優れ、4象限を一度にスキャンできる。SS-OCTでは360度評価と隅角閉塞範囲の定量が可能
定量パラメータ:AOD、線維柱帯虹彩空間面積(TISA)、虹彩線維柱帯接触(ITC)指数。AOD750が0.1 mm減少するごとに隅角閉塞のオッズは3.27倍増加する
限界:色素・新生血管の評価はできない3)。器質的隅角閉塞の鑑別が困難。強膜岬の同定が15〜28%で不可能
AS-OCTは隅角鏡検査より多くの隅角閉塞を検出する傾向がある2)。Nolanらの342眼の研究ではAS-OCTで66.7%、隅角鏡検査で44.4%が閉塞と診断された。これはAS-OCTが赤外線を使用し、隅角鏡検査中の不注意な圧迫による隅角開大の影響を受けないためと考えられる。ただしAS-OCTは隅角鏡検査を代替するものではなく、補完的に使用すべきである2)。
| モダリティ | 接触 | 毛様体描出 | 定量性 | 色素評価 |
|---|---|---|---|---|
| 超音波生体顕微鏡 | 要 | 可 | 可 | 不可 |
| AS-OCT | 不要 | 不可 | 優 | 不可 |
| 隅角鏡検査 | 要 | 不可 | 限定的 | 可 |
EyeCam(Clarity Medical Systems社)は接触型ハンドヘルドデバイスで、98%以上の患者で鮮明な隅角画像を取得できる。隅角鏡検査との一致度は良好(κ=0.72〜0.76)であるが、隅角閉塞の検出率は隅角鏡検査(13.8%)よりEyeCam(27%)が高い。圧迫(indentation)が行えないことが欠点である。
NGS-1自動隅角鏡は360度全体の隅角画像を提供する。複数焦点の高解像度写真を撮影するが、22.5%で低画質であり隅角鏡検査より感度が低いと報告されている。
両者は相補的であり一概には比較できない。AS-OCTは非接触で解像度・定量性に優れ、日常診療での使用が容易である3)。一方超音波生体顕微鏡は虹彩裏面・毛様体を描出でき、プラトー虹彩や毛様体腫瘍の診断では超音波生体顕微鏡が必須である3)。狭隅角検出における両者の平均値・再現性・感度・特異度は同様であると報告されている。
シュレム管(SC)の評価
超音波生体顕微鏡による評価:原発開放隅角緑内障眼では正常眼と比較してSC経線方向径・冠状方向径・TM厚がいずれも有意に小さい。小児緑内障でも非緑内障眼(142 μm)に比べ緑内障眼(64.9 μm)でSC径が有意に小さい
AS-OCTによる評価:SC断面積(CSA)の定量が可能。原発開放隅角緑内障眼のSC面積(11,332 μm²)は正常眼(13,991 μm²)より有意に小さい。SC面積は眼圧と有意に相関する
加齢変化:加齢に伴いSCのサイズと検出率が有意に減少する。TM厚は加齢とともに増加する
機種間差:CSAはOCT機種により異なる。SD-OCTで測定されたCSAはSS-OCTより大きい
治療によるSC変化
点眼薬:0.004%トラボプロスト点眼8時間後に平均SC面積が90%以上増加。ピロカルピンもSCを拡張させる。チモロール・ドルゾラミド配合剤ではSC変化なし
SLT後:SC断面積と体積が有意に増加。SC面積増加と眼圧下降に有意な正相関あり。若年開放隅角緑内障ではSCの特定がSLT成功の強力な予測因子である
カナロプラスティ後:SC高さ+351%、幅+144%の増加
線維柱帯切除術後:PACG眼でSC径・面積が有意に増加。SCの変化は眼圧下降率と相関する
集合管(CC)の生体内画像評価の報告は少ない。Liらは強調深度イメージングOCTを用いて、集合管の数が鼻側(5.5±1.4個)で耳側(3.3±1.1個)より有意に多いことを示した。SC断面積は集合管が多い領域で有意に大きかった(r=0.6)。
研究段階であるが臨床応用の可能性が広がっている。SC面積は眼圧と相関し、点眼薬や手術に対するSCの形態変化が報告されている。特にSLT前のSC同定がSLT成功の予測因子となりうることは臨床的に重要である。ただしSCの同定率は年齢により異なり(15歳以上73.8% vs 7歳以下53.6%)、機種間でCSAが異なる点に注意が必要である。
前眼部OCTアンギオグラフィ(AS-OCTA)により結膜血管と深部の強膜内血管の評価が可能になっている。深部血管層(上強膜静脈・房水静脈に相当)では血管密度・長さ密度・直径指数・フラクタル次元が象限間で異なる。
房水静脈の観察はMIGSの効果予測に有用である可能性がある。iStent術後の眼圧下降率は房水静脈の流れのgradeと相関すると報告されている。
主流出路は前房→線維柱帯→シュレム管→集合管→房水静脈→上強膜静脈→体循環の経路をたどる。線維柱帯は前房側から線維柱帯ぶどう膜部・角強膜線維柱帯・傍シュレム管結合組織(JCT)の3部に分けられる1)。
房水流出抵抗の大部分はJCTとシュレム管内壁内皮(SCE)との間に存在する1)。SCE基底膜の微小不連続部を通じて房水が巨大空胞・細孔を経てシュレム管腔に流出する1)。房水流出は均一ではなく、高流量・低流量の領域が分節的(セグメンタル)に存在する1)。緑内障眼では低流量領域が多い1)。
緑内障眼のJCTの細胞外マトリックスは正常眼の約20倍の硬さを示す1)。線維柱帯細胞の喪失はIOPホメオスタシス応答の消失につながり、細胞の補充により応答が回復する1)。
副流出路では房水が毛様体前端部の細胞間隙から毛様体実質に入り、ぶどう膜に沿って後方へ向かい、強膜を経由して眼外に流出する。流出量は0.2〜0.4 μL/分とされる。主流出路が圧依存性であるのに対し、副流出路は圧非依存性である4)。
房水流出抵抗の大部分は傍シュレム管結合組織(JCT)の最深部、すなわちシュレム管内壁内皮(SCE)とその基底膜からなる厚さ1〜2 μmの領域に局在する1)。線維柱帯ぶどう膜部や角強膜線維柱帯の線維柱間隙では房水はほとんど抵抗を受けない。緑内障眼ではこの領域の細胞外マトリックスの硬さが正常の約20倍に増加しており、これが流出抵抗増大の一因と考えられている1)。
AS-OCT画像から隅角閉塞を自動検出するディープラーニングシステムが開発されている。Fuらのモデルでは曲線下面積(AUC)0.96、感度0.9、特異度0.92が報告された。隅角閉塞リスクの高い患者のスクリーニングへの応用が期待される。
AS-OCTAにより造影剤を使用せず前眼部の微小血管を画像化できる。深層血管の描出により集合管以降の経路(上強膜静脈・房水静脈)の評価が可能となりつつある。今後、MIGS術前の流出路評価や術後効果の予測における有用性が検討される見込みである。
OCT技術の進歩によりシュレム管の生体内計測が可能となり、薬物・レーザー・手術に対するSCの形態変化をモニタリングできるようになった。SLT成功予測やカナロプラスティの評価など臨床応用への展開が進んでいる。
- Acott TS, Vranka JA, Keller KE, Raghunathan V, Kelley MJ. Normal and glaucomatous outflow regulation. Prog Retin Eye Res. 2021;82:100897.
- European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.
- De Groef L, Bhatt DK. The role of the visual system in glaucoma. Annu Rev Vis Sci. 2024.