線維柱帯手技
ステント留置: iStent、iStent inject W、Hydrusマイクロステントにより線維柱帯をバイパスしシュレム管へ直接排出する1)5)
線維柱帯切開・切除: Kahook Dual Blade(KDB)、Trabectome、GATT、OMNIにより線維柱帯を切開・切除しシュレム管を露出する1)5)
粘弾性拡張: Ab interno canaloplasty(ABiC)により360度にわたりシュレム管を拡張し集合管の開通を図る1)

低侵襲緑内障手術(Microinvasive Glaucoma Surgery: MIGS)は、ab interno(眼内側)から行う非ブレブ形成手技である1)。線維柱帯または脈絡膜上腔の流出を増強し、正常な解剖・生理への侵襲を最小限に抑える1)。「MIGS」の用語は2009年にIqbal Ike K. Ahmed医師が提唱した。
従来、点眼薬やレーザーで眼圧コントロールが不十分な軽度〜中等度の患者には、線維柱帯切除術や緑内障ドレナージデバイスなどの濾過手術が選択肢であった。しかし濾過手術は低眼圧・脈絡膜出血などの重篤な合併症リスクがあり、軽度〜中等度の患者では先送りされることが多かった。低侵襲緑内障手術はこの「治療の空白」を埋める手技群として普及が進んでいる2)。
低侵襲緑内障手術は安全性・有効性のバランスにおいて従来手術と異なる特性をもつ2)。眼圧下降効果は従来の濾過手術より劣るが、合併症リスクは著しく低い2)3)。結膜切開を必要としないため、将来の濾過手術の成功率を損なわない2)。
低侵襲緑内障手術の5つの定義的特徴は以下のとおりである。
MIGSは眼の内側(ab interno)から小さな切開で行うため、回復が早く合併症リスクが低いのが特徴です。一方、線維柱帯切除術などの従来手術は眼圧をより大きく下げられますが、低眼圧や感染などの重篤な合併症リスクがあります。MIGSは軽度〜中等度の緑内障に適しており、進行した緑内障で低い目標眼圧が必要な場合は従来手術が選択されます。担当医と相談してください。
MIGSは作用機序と解剖学的ターゲットにより分類される1)。ブレブ形成を伴う結膜下デバイス(XEN Gel Stentなど)は安全性・有効性プロファイルが異なるため、MIGSではなくMIBS(Minimally Invasive Bleb Surgery)に分類される1)2)。
線維柱帯手技
ステント留置: iStent、iStent inject W、Hydrusマイクロステントにより線維柱帯をバイパスしシュレム管へ直接排出する1)5)
線維柱帯切開・切除: Kahook Dual Blade(KDB)、Trabectome、GATT、OMNIにより線維柱帯を切開・切除しシュレム管を露出する1)5)
粘弾性拡張: Ab interno canaloplasty(ABiC)により360度にわたりシュレム管を拡張し集合管の開通を図る1)
その他の手技
脈絡膜上腔手技: Minijectにより脈絡膜上腔へのぶどう膜強膜流出を増強する1)
房水産生抑制: 内視鏡下毛様体光凝固術(endoCPC)により毛様体を焼灼し房水産生を減少させる3)
レーザー手技: Excimer Laser Trabeculotomy(ELT)により線維柱帯にレーザーで微小孔を作成する1)
| カテゴリ | 代表的デバイス・手技 | 解剖学的ターゲット |
|---|---|---|
| ステント留置 | iStent inject W, Hydrus | TM/シュレム管 |
| 線維柱帯切開 | KDB, GATT, OMNI | TM/シュレム管 |
| 脈絡膜上腔 | Miniject | 脈絡膜上腔 |
日本ではフックやブレードを用いた流出路再建術が広く普及している。角膜小切開創から隅角鏡下に線維柱帯を切開する術式であり、白内障手術との同時施行が一般的である。原発開放隅角緑内障・正常眼圧緑内障・落屑緑内障・ステロイド緑内障などが適応となる8)。
MIGSは大きく3つに分類されます。(1)線維柱帯手技(iStentなどのステント、KDBなどの切開術、ABiCなどの粘弾性拡張)、(2)脈絡膜上腔手技、(3)房水産生抑制(内視鏡下毛様体光凝固術)です。どの手技が適切かは緑内障の病型・重症度・併存疾患などにより異なります。
低侵襲緑内障手術は主に軽度〜中等度の開放隅角緑内障または高眼圧症の患者に適応される1)3)。
以下のような状況で考慮される。
白内障手術との併用が最も一般的であるが、一部の手技は単独でも施行可能である1)2)。
低侵襲緑内障手術は全体として15〜50%の眼圧下降を達成し、薬剤使用量を0.4〜1.8剤減量させる4)。メタアナリシスでは、低侵襲緑内障手術の1年時眼圧下降効果は全サブタイプにわたり統計学的に有意であった3)。
低侵襲緑内障手術+白内障手術の併用は白内障手術単独と比較して2〜2.8 mmHg大きい眼圧下降を示す4)。単独の低侵襲緑内障手術は併用手技と比較して再手術率が高く、2年時に最大24%に達する4)。
主要デバイスの臨床成績
iStent inject: 24ヶ月時に75.8%が20%以上の眼圧下降を達成(白内障手術単独群は61.9%)5)
Hydrus: HORIZON試験で24ヶ月時に77.3%が20%以上の眼圧下降(白内障手術単独群は57.8%)6)
iStent(第1世代): 12ヶ月時に72%が薬剤なしで眼圧≦21 mmHg(白内障手術単独群は50%)5)
効果の持続性
経時的減弱: 他のすべての緑内障手術と同様に、MIGSの効果は時間とともに減弱する傾向がある2)
短〜中期: 短期〜中期の眼圧低下と薬剤負担軽減は確認されている3)
長期データ: 長期的な効果の持続性・視野進行への影響については十分なデータが蓄積されていない1)2)
白内障手術自体にも眼圧下降効果があるため、低侵襲緑内障手術の独自の効果と白内障手術の効果を分離することは困難である1)7)。
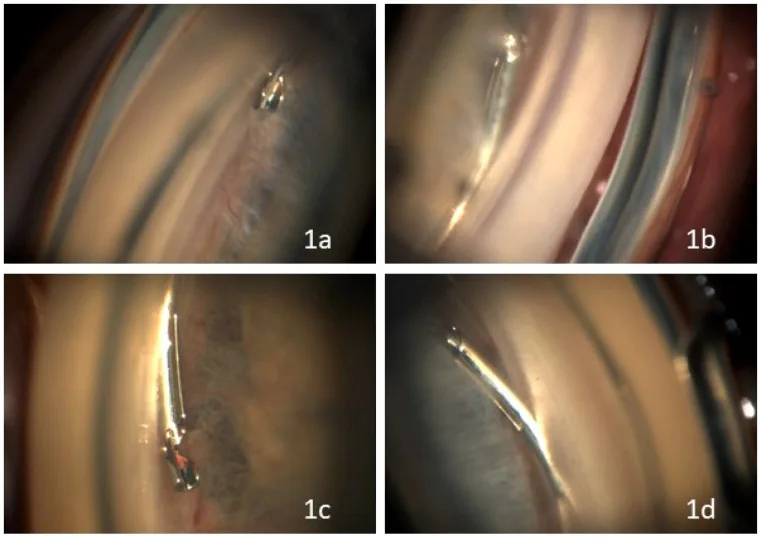
低侵襲緑内障手術は従来の緑内障手術と比較して合併症プロファイルが良好である3)。メタアナリシスでは最も多い合併症として前房出血(24.9%)、一過性眼圧上昇(4.9%)、術後炎症(3.31%)が報告されている3)。
| 合併症 | 頻度 |
|---|---|
| 前房出血 | 24.9% |
| 一過性眼圧上昇 | 4.9% |
| 術後炎症 | 3.31% |
注目すべきは、低眼圧・複視・感染といった従来手術で懸念される重篤合併症の報告がない点である3)。TVT Study(Tube Versus Trabeculectomy Study)では早期術後合併症が緑内障ドレナージデバイス 22%、線維柱帯切除術39%であり、低侵襲緑内障手術の安全性の優位性が示唆される3)。
Hydrusマイクロステントでは位置不良によりぶどう膜炎・緑内障・前房出血(UGH)症候群を生じ、摘出が必要となる症例が報告されている6)。4例の症例シリーズでは全例にUGH症候群の所見(虹彩炎3例、嚢胞様黄斑浮腫2例、前房出血1例、高眼圧4例)を認めた6)。留置後6ヶ月以上経過した症例では虹彩組織の癒着により摘出が困難となるため、早期の異常認識が重要である6)。
前房出血はHydrus(36.4%)でiStent(19.9%)やiStent inject(8.5%)より有意に高頻度であった6)。
MIGSの合併症は一般的に軽度で一過性です。前房出血が最も多いですが、通常は数日で自然に消退します。低眼圧・感染・複視などの従来手術で懸念される重篤な合併症はMIGSではほとんど報告されていません。ただし、デバイスの位置不良により追加手術が必要になる場合があります。術後は担当医の指示に従い定期的に受診してください。
近管腔線維柱帯(juxtacanalicular trabecular meshwork)が房水流出に対する最大の抵抗部位である2)。この抵抗をバイパスまたは除去することでシュレム管への流出が改善し、眼圧が低下する2)。
眼圧上昇はシュレム管の虚脱を引き起こし、管壁と線維柱帯に慢性変化をもたらす2)。粘弾性拡張(ABiC)ではシュレム管と集合管を360度にわたり拡張し、この病的変化を改善する。
iStentやHydrusなどの管腔型ステントは線維柱帯を貫通して留置される。前房から直接シュレム管へ房水を排出するバイパス経路を形成する2)。Hydrusは8 mmの長さで90度にわたりシュレム管を拡張する足場としても機能する6)。
KDB・Trabectome・GATT・OMNIなどは線維柱帯組織を切開または切除する。シュレム管の内壁を直接露出させ、房水の流出抵抗を減少させる。フックやブレードによる線維柱帯切開では、シュレム管内壁穿破に伴う前房出血は必発であるが、通常2〜3日で消退する8)。
線維柱帯MIGSの眼圧下降効果は上強膜静脈圧とシュレム管から遠位の流出抵抗によって制限される1)。そのため眼圧がmid-teens以下に低下することは稀である1)。
低侵襲緑内障手術の研究における臨床エンドポイントの報告方法は統一されておらず、異なる研究間の比較が困難である2)。世界緑内障学会(WGA)および欧州緑内障学会(EGS)は、眼圧低下率とIOPの上限値を組み合わせた成功基準を推奨している2)。
従来、閉塞隅角緑内障はMIGSの禁忌とされてきた3)。しかし、近年は多くの患者がMIGSの恩恵を受けられるとの考えから、この見解は変化しつつある3)。
現在のエビデンスでは、低侵襲緑内障手術の各手技間の優劣や従来の線維柱帯切除術との同等性を支持する十分なデータが存在しない7)。長期の安全性・費用対効果・薬剤非依存率・理想的な患者プロファイルに関するデータの蓄積が今後の課題である1)7)。
患者報告アウトカム(PRO)に関する研究は限られているが、視覚機能・生活の質・眼表面の健康の改善を示唆する予備的知見が得られている4)。
MIGSの効果は他の緑内障手術と同様に時間とともに減弱する可能性があります。単独MIGSでは2年時に最大24%で再手術が必要となったとの報告があります。MIGSは結膜を温存するため、将来的に線維柱帯切除術や緑内障ドレナージデバイスなどの追加手術が必要になった場合にもその成功率を損なわないという利点があります。
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025.
Gedde SJ, et al. Reporting Clinical Endpoints in Studies of Minimally Invasive Glaucoma Surgery. Ophthalmology. 2025;132(2):143-151.
Paik JM, et al. Outcomes and Complications of Minimally Invasive Glaucoma Surgery: A Systematic Review and Meta-Analysis. Clin Ophthalmol. 2025;19:487-503.
Singh A, et al. Minimally Invasive Glaucoma Surgery: A Review of Clinical and Patient-Reported Outcomes. Cureus. 2025;17(7):e87872.
American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern. 2020.
Sachdeva N, et al. Early to late explantation of Hydrus microstent MIGS device: A case series. Am J Ophthalmol Case Rep. 2024;36:102105.
European Glaucoma Society. Terminology and Guidelines for Glaucoma, 5th Edition. PubliComm; 2020.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126:85-177.