内科的治療
房水産生抑制薬:局所β遮断薬、α作動薬、炭酸脱水酵素阻害薬が第一選択である6)。房水流出部位を標的とする縮瞳薬より房水産生抑制薬が推奨される。
プロスタグランジン関連薬:HSVの理論的役割から、ラタノプロスト誘発性のHSV再発の懸念があり慎重に検討すべきである2)。
角膜浮腫管理:高張食塩水の点眼液・ゲルによる角膜脱水を行う。
長期予後:薬物治療は膜様組織の進行により周辺虹彩前癒着が拡大するため抵抗性となることが多い6)。

虹彩角膜内皮症候群(ICE症候群)は、異常な角膜内皮細胞が膜様組織を伴って隅角および虹彩に伸展・収縮し、線維柱帯が閉塞されて眼圧上昇をきたす疾患である。角膜内皮異常による角膜浮腫と、膜様組織の収縮による虹彩変形および周辺虹彩前癒着(PAS)を特徴とする。
ICE症候群は以下の3つの臨床型に分類される。
通常は20〜50歳の女性に片眼性に発症する2)。散発性であり、他の眼疾患や全身疾患との一貫した関連はない。ICE症候群は片眼性で散発的である点が、両眼性で遺伝性の後部多形性角膜ジストロフィ(PPMD)との最も簡単な鑑別点となる。
3型の区別は主に虹彩と角膜の臨床所見に基づく。チャンドラー症候群は角膜浮腫が主体で虹彩変化は軽微であり、眼圧が正常でも角膜浮腫を生じうる。進行性虹彩萎縮は多瞳孔症・瞳孔偏位・虹彩孔形成・ぶどう膜外反が顕著で、緑内障合併が最も多い。コーガン・リース症候群は虹彩前面の有茎性の茶色結節またはびまん性の色素性病変が特徴であり、虹彩萎縮は通常みられない。ただし、いずれの型も基本的な病態生理は共通であり、治療方針も同様である。
初期症状は片眼性の疼痛、視界のぼやけ、または虹彩外観の変化である。角膜浮腫による疼痛と、隅角閉鎖による眼圧上昇に伴う痛みが混在する。虹彩異色、瞳孔の変形に気づいて受診する場合もある。
角膜所見:角膜内皮は「叩き出しの銀」または「打ち出しの銅」のような外観を呈し、フックス角膜内皮ジストロフィの角膜滴状粉に類似する。角膜浮腫は眼圧が正常であっても微小嚢胞状になることがある。
虹彩所見:虹彩異色、ぶどう膜外反、瞳孔偏位、虹彩孔形成、虹彩萎縮が型に応じて出現する2)。コーガン・リース症候群では虹彩前面の有色素性結節が認められ、組織学的にはメラニン含有紡錘形母斑細胞からなる良性病変である4)。
隅角所見:隅角鏡検査でSchwalbe線を越えて高く伸びる周辺虹彩前癒着が認められ、これはICE症候群に病的(pathognomonic)な所見である5)。周辺虹彩前癒着は斑状で非常に前方に位置し、周辺虹彩前癒着間の線維柱帯は正常に見える5)。
| 臨床型 | 角膜浮腫 | 虹彩所見 | 緑内障頻度 |
|---|---|---|---|
| チャンドラー | 顕著 | 軽度 | 中等度 |
| 進行性虹彩萎縮 | 中等度 | 顕著 | 最多 |
| コーガン・リース | 中等度 | 結節 | 中等度 |
ICE症候群の真の病因は未解明であるが、単純ヘルペスウイルス(HSV)またはエプスタイン・バーウイルス(EBV)の潜在感染が角膜内皮レベルで低グレードの炎症を惹起し、上皮様の活性化を引き起こすとの仮説がある。PCR検査ではICE症候群患者の角膜内皮および房水からHSV DNAが高率に検出されている。Alvaradoらの報告では、ICE患者の角膜・房水サンプルの60%以上からHSV DNAが検出されている2)。
病理学的には、正常な内皮細胞が移動特性を持つ上皮様細胞に置換される。電子顕微鏡ではデスモソーム、トノフィラメント、微絨毛などの上皮的特徴が確認される。隣接する正常内皮細胞に対する毒性損傷(壊死性変化)も報告されている。
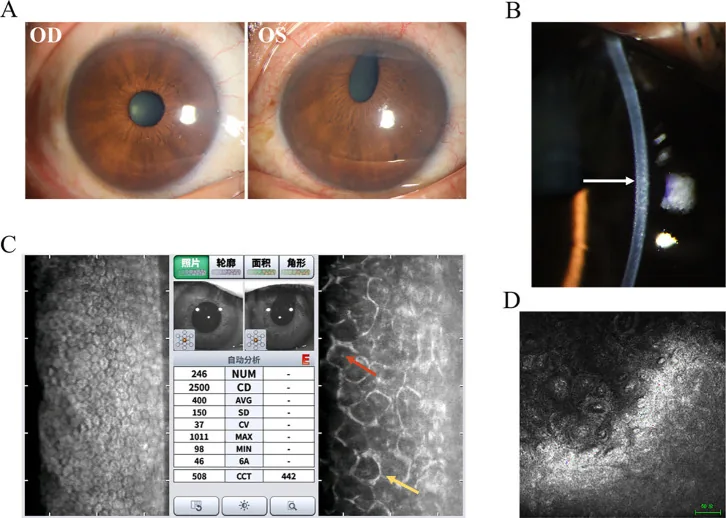
スペキュラーマイクロスコピー:最も重要な診断ツールである2)。典型的な六角形の角膜内皮形状が消失し、多形性で「明暗反転(light-dark reversal)」を示す。中央に明るい点を持つ通常より大きく暗い内皮細胞(ICE細胞)が特徴的である。角膜内皮細胞密度の著明な減少を認め、コーガン・リース症候群の1例では763 cells/mm²まで低下した報告がある3)。
In vivoコンフォーカル顕微鏡(IVCM):角膜内皮の丸石状腫脹細胞、六角形構造の消失、多形性の高輝度細胞、単核・二核の巨大内皮細胞を描出する2)。
前眼部OCT(AS-OCT):虹彩角膜角の癒着、角膜内皮層の高輝度肥厚、虹彩上の膜様組織を可視化する2)。
隅角鏡検査:周辺虹彩前癒着の評価に不可欠であり、続発閉塞隅角緑内障の診断と経過観察に用いる。
緑内障評価:眼圧測定、視神経乳頭写真、視野検査(ハンフリーまたはゴールドマン)、OCTによる網膜神経線維層評価を初期精密検査および経過観察に導入する2)。
前進する角膜内皮細胞膜が収縮を伴わずに線維柱帯を機能的に閉鎖する場合がある。この場合、隅角鏡検査で明らかな周辺虹彩前癒着が視認されないため、「機能的な」隅角閉鎖が存在するにもかかわらず開放隅角緑内障と誤認される。片眼性の緑内障を見た場合はICE症候群を鑑別に含め、スペキュラーマイクロスコピーで角膜内皮を慎重に評価すべきである。
内科的治療
房水産生抑制薬:局所β遮断薬、α作動薬、炭酸脱水酵素阻害薬が第一選択である6)。房水流出部位を標的とする縮瞳薬より房水産生抑制薬が推奨される。
プロスタグランジン関連薬:HSVの理論的役割から、ラタノプロスト誘発性のHSV再発の懸念があり慎重に検討すべきである2)。
角膜浮腫管理:高張食塩水の点眼液・ゲルによる角膜脱水を行う。
長期予後:薬物治療は膜様組織の進行により周辺虹彩前癒着が拡大するため抵抗性となることが多い6)。
外科的治療
線維柱帯切除術:抗線維化薬(MMCまたは5-FU)併用で行う6)。生存率は1年73%、3年44%、5年29%と報告されている。異常内皮による瘻孔閉塞のリスクがある。
チューブシャント手術:生存率は1年71%、3年71%、5年53%と線維柱帯切除術より長期成績が良好である5)6)。ブレートのあるチューブシャントが選択されることが多い。
角膜内皮移植:DSAEK/DSEKにより角膜機能を改善する1)。全層角膜移植(PKP)と同等の移植片生存率であるが、視覚回復が速く乱視が軽度である1)。
毛様体破壊術:難治例の最終手段としてダイオードレーザー毛様体光凝固術を行う6)。
2段階手術アプローチとして、水晶体乳化吸引術+人工虹彩挿入を先行し、6ヶ月後にDSAEKを行う方法が報告されている1)。54歳女性の症例では、術後矯正視力が20/100から20/32に改善し、角膜内皮細胞密度1,640 cells/mm²が維持された1)。
コーガン・リース症候群における嚢胞様黄斑浮腫(CME)のまれな合併が報告されている3)。局所NSAIDs(フルルビプロフェン1日3回)による治療で消退が得られたが、中止後に再発した3)。異常内皮細胞が内側血液網膜関門を障害し、HSV関連サイトカインによるプロスタグランジン産生が病態に関与すると推定されている3)。
ICE症候群の根本的な異常は角膜内皮の上皮様化生にある。正常な内皮細胞が、増殖・遊走能を持つ上皮様細胞に置換される。この過程はPPMDにも共通するが、ICEは片眼性で散発的、PPMDは両眼性で常染色体優性遺伝である点が異なる。
上皮様化生した内皮細胞は角膜裏面からSchwalbe線を越えて線維柱帯上、さらに虹彩前面へと前進する5)。この膜様組織が収縮することで以下の病態が生じる。
続発閉塞隅角緑内障:高い周辺虹彩前癒着の形成による房水流出路の閉塞が主な機序である5)。膜自体による線維柱帯の機能的閉鎖も生じうるため、明らかな周辺虹彩前癒着がなくても緑内障が発生する。
角膜浮腫:変性した内皮細胞のポンプ機能不全と、緑内障による眼圧上昇の両者が原因となる。チャンドラー症候群で最も顕著である。
虹彩変形:膜様組織の収縮により虹彩が牽引され、瞳孔偏位・虹彩孔形成・ぶどう膜外反が生じる。進行性虹彩萎縮で最も顕著であり、瞳孔偏位は周辺虹彩前癒着が多い方向に偏る。
コーガン・リース症候群の虹彩結節は組織学的に紡錘形メラニン細胞母斑様細胞からなり、Ki-67陽性率1%未満、melan-A陽性の良性病変である4)。まれに水晶体小帯脆弱性を伴い、白内障手術時にびまん性小帯離開を認めることがある4)。
最も簡便な鑑別点は、ICE症候群が散発性で片眼性であるのに対し、PPMDが常染色体優性遺伝で両眼性であることである。スペキュラーマイクロスコピーでも異なり、ICE症候群では中央にハイライトのある暗い領域(ICE細胞)を示すが、PPMDは典型的な小胞やバンド状構造を呈する。PPMDも瞳孔偏位や角膜浮腫を伴いうるが、性差がなく先天性であるため臨床経過も異なる。