バルブ型(Valved)
代表:Ahmed緑内障バルブ(AGV)
機構:最小開放圧を持つ一方向弁により即時的な房水流出を開始
利点:術後早期の眼圧コントロールが予測しやすく、低眼圧のリスクが低い
欠点:長期的な眼圧下降はノンバルブ型にやや劣る2)
材質:シリコン(FP7/FP8)またはポリプロピレン(S2/S3)

緑内障ドレナージデバイス(GDD:glaucoma drainage device)は、房水シャント(aqueous shunt)またはチューブシャントとも呼ばれ、房水を前房から赤道部後方に配置された外部プレートへ誘導するインプラントである1)。合成チューブと合成プレートからなり、プレートは線維柱帯切除術より遥かに後方に位置する1)。
術後4〜6週間でプレート周囲に線維性被膜(fibrous capsule)が形成され、これが房水流出を調節する。長期的な眼圧コントロールは通常、点眼薬の併用下で達成される1)。
最初の緑内障ドレナージデバイスであるMoltenoインプラントの導入以来40年以上にわたり、様々な改良が加えられてきた。現在では眼圧調節バルブの有無、サイズ、材質、デザインが異なる多種のデバイスが市販されている。
緑内障ドレナージデバイスの主な適応は以下の通りである1)2)。
近年では一次手術としての緑内障ドレナージデバイス使用に対する関心が高まっており、その有効性がランダム化比較試験で確認されつつある1)。米国のMedicareデータでは1994年から2012年にかけてシャント手術件数が増加し、線維柱帯切除術件数は減少している2)。
緑内障ドレナージデバイスはバルブ(弁)機構の有無により大きく2つに分類される。
バルブ型(Valved)
代表:Ahmed緑内障バルブ(AGV)
機構:最小開放圧を持つ一方向弁により即時的な房水流出を開始
利点:術後早期の眼圧コントロールが予測しやすく、低眼圧のリスクが低い
欠点:長期的な眼圧下降はノンバルブ型にやや劣る2)
材質:シリコン(FP7/FP8)またはポリプロピレン(S2/S3)
ノンバルブ型(Nonvalved)
代表:Baerveldt、Molteno
機構:弁機構なし。術後はステントまたは結紮糸で一時閉塞し、被膜形成後に開放
利点:長期的な眼圧下降に優れ、到達可能な眼圧がより低い2)
欠点:術後早期の低眼圧リスクが高く、管理がより複雑
材質:シリコン(Baerveldt、ClearPath)またはポリプロピレン(Molteno)
| デバイス | プレート面積 | 材質 | 特徴 |
|---|---|---|---|
| Ahmed FP7 | 184 mm² | シリコン | バルブ型・最も汎用 |
| Baerveldt 350 | 350 mm² | シリコン | ノンバルブ型・大面積 |
| Molteno3 GS | 175 mm² | ポリプロピレン | ノンバルブ型 |
長期的な眼圧コントロールはインプラントのプレート表面積に依存する。これが濾過胞のサイズ、組織反応、線維性被膜の厚さを決定する。ダブルプレートのMoltenoはシングルプレートより眼圧コントロールが良好であった。一方、350mm²と500mm²のBaerveldtの比較では350mm²モデルが優れていた。
プレート材質について、AGVではシリコンモデル(FP7)がポリプロピレンモデル(S2)と比較して最終的な眼圧コントロールが改善し、テノン嚢胞(Tenon’s cyst)の発生が少なかったとの報告がある。現在、市販デバイス間に明確な優劣を示すエビデンスはない1)。
術後早期の安定した眼圧コントロールを重視する場合や、術後の通院・点眼アドヒアランスに課題がある患者にはバルブ型(Ahmed)が適している。より低い最終眼圧を目標とする場合はノンバルブ型(Baerveldt)が有利であるが、術後管理がより複雑になる2)。結膜瘢痕の範囲やインプラントサイズの選択も重要な考慮事項である。
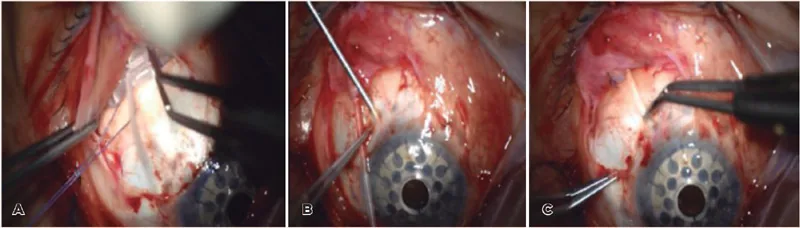
緑内障ドレナージデバイスの標準的な手術手技は以下の通りである。
チューブの挿入部位は前房が最も一般的であるが、偽水晶体眼では毛様体溝、硝子体切除眼では毛様体扁平部に配置することもある。
ノンバルブ型デバイスでは術後早期の低眼圧を防ぐため、以下の工夫が行われる。
チューブ内ステント:4-0または5-0縫合糸をチューブ内腔に挿入し、被膜形成後にスリットランプ下で除去する。
外側結紮:吸収性縫合糸(7-0または8-0バイクリル)でチューブを結紮する。ベンティングスリットを併用して早期の部分的流出を確保することもある。
二段階手術:第一段階でプレートのみ固定し、4〜6週間後に被膜形成を待ってチューブを前房に挿入する。
チューブ露出:緑内障ドレナージデバイス特有の合併症であり、結膜びらんを経てチューブが露出する8)。4.3〜14.3%の頻度で発生する7)。眼内炎のリスクがあるため早期の修復が必要である。パッチグラフト追加や強膜トンネルでの被覆が行われる。
低眼圧:特にノンバルブ型で多い1)。前房の深さが維持されていれば保存的に管理可能であるが、水晶体・角膜接触がある場合は粘弾性物質注入による前房再形成が必要となる。
テノン嚢胞(被膜化):プレート周囲の線維性被膜が肥厚し眼圧が上昇する。AGVでの頻度は40〜80%、ノンバルブ型では20〜30%とされる10)。術後3週〜3ヶ月の「高眼圧期(hypertensive phase)」として出現することが多い。
チューブ閉塞:血餅、虹彩、硝子体、線維組織などによりチューブが閉塞する6)。角膜混濁例では眼内内視鏡が原因の同定と治療に有用である6)。
角膜内皮障害:チューブが角膜内皮に近接する場合、長期的な角膜内皮細胞減少と水疱性角膜症をきたしうる1)。
巨大濾過胞:まれにプレート周囲に巨大な濾過胞が形成される5)。前方拡大型(細隙灯で観察可能、異物感・美容的問題)と後方拡大型(眼球偏位・複視、MRIで評価)に分類される5)。
Ugarte らは AGV挿入後の巨大濾過胞を前方拡大型と後方拡大型に分類し、後方拡大型はT2強調MRIでの評価が有用であると報告した5)。
TVT Studyの5年データでは、重篤な合併症の発生率はチューブ群で34%、線維柱帯切除術群で36%であった。主な合併症として前房消失(GDD 13.6%)、低眼圧(11.7%)、チューブ露出(5%前後)がある1)。多くの合併症は適切な管理により対処可能であるが、長期経過観察が不可欠である。
線維柱帯切除術が有利な点
インプラント不要:異物がなく、チューブ露出のリスクがない1)
角膜内皮:長期的な角膜内皮障害のリスクが低い
再手術の選択肢:追加の緑内障手術の選択肢がより多い
緑内障ドレナージデバイスが有利な点
濾過手術高リスク例:結膜瘢痕・続発緑内障に適する1)
術後管理:術後ケアの負担が少ない
創漏れ:術後の創漏れリスクが低い
| 研究 | 比較 | 主要結果 |
|---|---|---|
| TVT Study | Baerveldt 350 vs TLE+MMC(既手術眼) | 5年成功率: 緑内障ドレナージデバイス > TLE。眼圧低下・合併症は同等2) |
| PTVT Study | Baerveldt 350 vs TLE+MMC(初回手術眼) | 3年: 成功率は同等。TLEがより低い眼圧を達成2) |
| ABC/AVB Study | Ahmed vs Baerveldt | Baerveldtが眼圧低下に優れるが、重篤合併症はAhmedで少ない2) |
TVT Study(Tube Versus Trabeculectomy Study)は、以前に白内障手術または線維柱帯切除術の既往がある眼を対象とした多施設RCTである2)。5年の追跡でチューブ群の成功率が線維柱帯切除術群を上回ったが、眼圧低下・薬剤使用・重篤合併症・視力喪失は同等であった。
PTVT Study(Primary TVT Study)は初回手術眼を対象とした進行中のRCTであり、3年時点で成功率は両群で同等であったが、線維柱帯切除術群でより低い眼圧がより少ない薬剤数で達成された2)。
ABC Study(Ahmed Baerveldt Comparison)とAVB Study(Ahmed Versus Baerveldt)はいずれもAhmedとBaerveldtを比較した多施設RCTである2)。5年間の追跡でBaerveldt群はAhmed群と比較して眼圧低下・薬剤減少に優れていたが、ABC Studyでの重篤合併症とAVB Studyでの低眼圧関連視力障害はAhmed群で少なかった。
Stallworthらは32研究(1,221眼、885人の小児)を対象としたシステマティックレビュー・メタアナリシスで、小児緑内障ドレナージデバイスの術後12ヶ月のプール平均眼圧は16.5 mmHg、成功率は0.87(95%CI 0.83-0.91)であったと報告した3)。24ヶ月では平均眼圧17.6 mmHg、成功率は0.77であった。
小児緑内障では隅角手術が第一選択であるが、続発緑内障では効果が限定的であり、緑内障ドレナージデバイスが一次治療として使用されることがある3)。研究の90%がAhmedを使用しており、小児におけるBaerveldtのデータは限られている3)。
緑内障ドレナージデバイスにおけるマイトマイシンCの術中使用は複数のRCTで検討されたが、成功率の向上は示されなかった1)。低眼圧期の延長と合併症増加が報告されており、現在緑内障ドレナージデバイスにおいて抗線維化薬は一般的に使用されていない。
どちらが最適かは患者の状態によって異なる。初回手術の原発開放隅角緑内障ではPVTT Studyで線維柱帯切除術がより低い眼圧を達成した2)。一方、以前の手術歴がある眼や続発緑内障では緑内障ドレナージデバイスが有利である1)2)。結膜瘢痕の程度、目標眼圧、患者の通院・アドヒアランスなどを総合して選択する。
パッチグラフトを不要とする自家強膜トンネルを用いたチューブ被覆法が開発されている。
Tanitoらは1mm幅のクレセントナイフを用いてマイクロインシジョン強膜トンネル(MIST)を作成し、前房・毛様体溝・硝子体腔の3部位へのチューブ挿入に応用した4)。縫合不要で手術時間の短縮が可能であり、術後のチューブ露出も認めなかった。
Miuraらは22ゲージ針を用いた強膜トンネル作成法を報告し、最長21ヶ月の経過観察でチューブ露出を認めなかった7)。
これらの手法はパッチグラフト材料の入手困難さやウイルス感染リスクを回避する利点がある。
Kawashimaらは角膜混濁でスリットランプ観察が困難なAGV不全例において、眼内内視鏡によりチューブ先端の線維組織による閉塞を同定し、組織除去により眼圧下降を得た6)。角膜混濁を伴う症例での緑内障ドレナージデバイス不全の診断に内視鏡が有用であることが示された。
Katsevらは流出路障害と房水産生低下を合併し、点眼薬の治療域が極めて狭い症例にAGVを挿入し、コンプライアントな流出路の創出により不安定な眼圧を安定化させた9)。15ヶ月間にわたり無投薬で眼圧8〜10 mmHgを維持した。