静脈閉塞による原因

上強膜静脈圧上昇(Elevated Episcleral Venous Pressure)
1. 上強膜静脈圧上昇とは
Section titled “1. 上強膜静脈圧上昇とは”上強膜静脈圧(episcleral venous pressure: EVP)の上昇は、房水流出路の下流における静脈圧の異常上昇により眼圧が上昇し、二次性開放隅角緑内障を引き起こす病態である3)。
ゴールドマンの式によると、眼圧は「房水産生量を流出施設で除した値にEVPを加えたもの」として表される。正常EVPは8〜10mmHg程度であり、EVPが1mmHg上昇するとIOPは約0.83±0.21mmHg上昇する。EVPとIOPには線形関係が成立する。
房水の従来型流出路では、房水はSchlemm管から集合管・房水静脈を経て上強膜静脈叢に合流し、上眼静脈から海綿静脈洞、内頸静脈、上大静脈を経て右心房へ流入する。この経路のいずれかで閉塞が生じるとEVPが上昇する3)。
ほとんどの症例は基礎疾患に続発して発症するが、すべての原因が除外された場合は特発性(Radius-Maumenee症候群)と診断される1)。特発性EVP上昇は1968年にMinasとPodosにより初めて記載され、1978年にRadiusとMaumeneeが4例を報告したことから同症候群と命名された1)。文献上の報告は約60例と極めてまれである1)。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”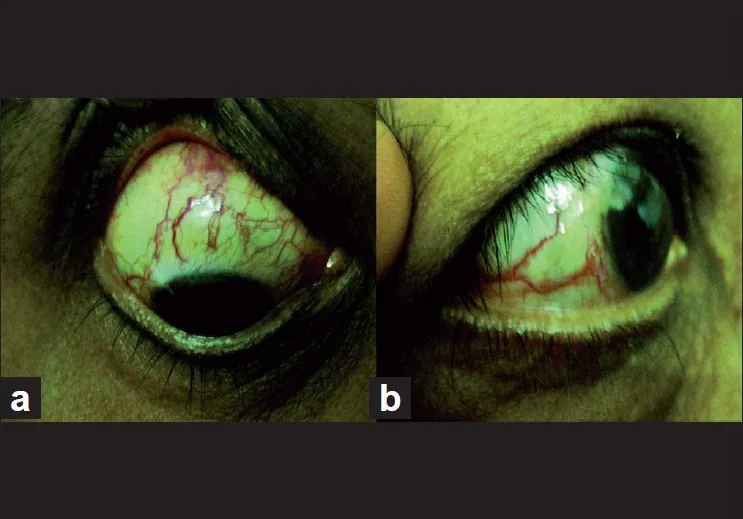
EVP上昇の患者は従来の治療に反応しない慢性の眼充血で受診することが多い。慢性結膜炎と誤診されることがしばしばある。通常、痛みや刺激感の訴えは少ない。急性の場合(頸動脈海綿静脈洞瘻など)は眼刺激症状や眼痛が出現しうる3)。
| 所見 | 特徴 |
|---|---|
| 上強膜血管 | 螺旋状(コルク抜き状)の拡張 |
| 隅角鏡 | 開放隅角+Schlemm管血液逆流 |
| 眼圧 | 上昇(慢性例で持続的) |
| 眼球突出 | 頸動脈海綿静脈洞瘻では拍動性 |
特徴的な所見は炎症を伴わない螺旋状の上強膜血管拡張であり、隅角鏡検査では開放隅角とSchlemm管への血液逆流が観察される1)2)。慢性例ではSchlemm管壁の硝子化も認められることがある。結膜浮腫や眼球突出は原因疾患に応じて出現し、頸動脈海綿静脈洞瘻(CCF)では拍動性眼球突出と眼窩血管雑音が特徴的である3)。
Radius-Maumenee症候群の症例では、片側性または両側非対称性に発症することが多い1)2)。38歳女性の症例では、3年以上持続する右眼の充血を主訴とし、びまん性に怒張した上強膜血管、IOP 22mmHg(チモロール使用下)、正常な眼底所見が認められた1)。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”EVP上昇の原因は静脈閉塞、動静脈異常、特発性の3つに大別される3)。
| 分類 | 主な疾患 |
|---|---|
| 静脈閉塞 | 上大静脈症候群、海綿静脈洞血栓症 |
| 動静脈異常 | 頸動脈海綿静脈洞瘻、硬膜瘻、Sturge-Weber |
| 特発性 | Radius-Maumenee症候群 |
動静脈異常と特発性
頸動脈海綿静脈洞瘻(CCF):EVP上昇の最も頻度の高い原因。75%は頭部外傷に起因し、25%は特発性で中年女性に多い。拍動性眼球突出と血管雑音が特徴的
硬膜瘻:低流量の動静脈シャント3)
Sturge-Weber症候群:上強膜血管腫による3)
眼窩静脈瘤:Valsalva法で増強する眼球突出が特徴
Radius-Maumenee症候群:除外診断。約60例の報告1)
頸動脈海綿静脈洞瘻では眼虚血が持続すると血管新生緑内障を発症することがあり注意を要する。強膜炎や上強膜炎では上強膜静脈への炎症の波及により房水流出障害が生じ、眼圧上昇をきたす。
大きく3つに分類されます。静脈閉塞(上大静脈症候群、海綿静脈洞血栓症、甲状腺眼症、眼窩腫瘍)、動静脈異常(頸動脈海綿静脈洞瘻[頸動脈海綿静脈洞瘻]、硬膜瘻、Sturge-Weber症候群、眼窩静脈瘤)、特発性(Radius-Maumenee症候群)です。頸動脈海綿静脈洞瘻が最も頻度の高い原因であり、75%は頭部外傷に起因します。Radius-Maumenee症候群は除外診断であり、すべての二次性原因を画像検査で除外した上で診断されます。
4. 診断と検査方法
Section titled “4. 診断と検査方法”EVP上昇の診断では原因疾患の特定が最も重要である。
隅角鏡検査は必須であり、開放隅角とSchlemm管への血液逆流を確認する1)。
画像検査として、頭蓋内MRI・MRA/MRVにより海綿静脈洞病変や頸動脈海綿静脈洞瘻を除外する1)。CT血管造影は眼窩および頭蓋内の血管異常の評価に有用である。脳血管造影は動静脈瘻検出のゴールドスタンダードであるが侵襲的であり、眼窩ドップラー超音波検査が上眼静脈拡張の非侵襲的確認に用いられる。
甲状腺機能検査はすべての症例で実施すべきである1)。
EVP測定法として直接穿刺法(最も正確)や間接法(静脈圧計、エアジェット等)が存在するが、日常臨床でのルーチン使用には至っていない2)。
Radius-Maumenee症候群の症例では、頭蓋内MRI血管造影、甲状腺機能検査、血管造影がすべて正常であったことが報告されている1)。
鑑別診断として上強膜炎、強膜炎、結膜炎、急性閉塞隅角緑内障、酒さ、真性多血症などが挙げられる。
5. 標準的な治療法
Section titled “5. 標準的な治療法”治療の基本は原因疾患の治療であり、脳神経外科など他科との連携が必要となる3)。
薬物療法
β遮断薬・炭酸脱水酵素阻害薬:房水産生抑制が主な作用。EVP上昇に対する第一選択薬3)
Rhoキナーゼ阻害薬:ネタスジル点眼後にEVPが-0.79mmHg低下。Sturge-Weber症候群6眼でも有意な眼圧低下を報告
リパスジル:点眼8時間後に上強膜静脈内房水柱幅が有意に増加し、上強膜静脈流出の増強を示唆
注意点:線維柱帯流出促進薬は効果が限定的。プロスタグランジン関連薬は上強膜血管全体を拡張させる
レーザー・手術療法
線維柱帯切除術:適切な手術選択肢だが、脈絡膜滲出のリスクが高い。術中の急速な眼圧低下を防ぐために調整縫合が推奨される2)
緑内障ドレナージデバイス:Ahmed弁やBaerveldt implantが難治例に使用される。5年成績では反復手術例においてGDDが線維柱帯切除術より良好2)
XEN45ゲルステント:低侵襲な代替法。結膜組織を温存できる利点がある2)
レーザー線維柱帯形成術:EVP上昇に対するエビデンスは乏しい2)
Radius-Maumenee症候群の3症例の長期追跡では、線維柱帯切除術、XEN45、Ahmed弁、Baerveldt implant、毛様体光凝固術が施行された2)。全症例で少なくとも1眼が線維柱帯切除術を受けたが、反復手術が必要となることが多く、脈絡膜滲出(低眼圧を伴わない)が2例で発生した2)。術中の急速な眼圧低下が毛様体・脈絡膜・上強膜静脈における圧勾配を誘発し、脈絡膜滲出の原因となると考えられている2)。
頸動脈海綿静脈洞瘻では自然治癒もみられ、多くは良好な経過をとる。難治例ではバルーン療法や放射線療法が行われることがある。
治療の第一は原因疾患の治療です。眼圧コントロールにはβ遮断薬や炭酸脱水酵素阻害薬による房水産生抑制が有効です。最近ではRhoキナーゼ阻害薬(ネタスジル、リパスジル)がEVPを低下させる作用を持つことが示されています。薬物療法で眼圧コントロールが不十分な場合は手術が検討されますが、EVP上昇眼では濾過手術後の脈絡膜滲出リスクが高いため、術中の急速な眼圧低下を避ける慎重な手技が求められます。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”房水は主経路(全流出量の80〜95%)と副経路(5〜20%)の2つの経路で眼外へ排出される4)。主経路では房水は線維柱帯→Schlemm管→集合管→房水静脈→上強膜静脈→上眼静脈→海綿静脈洞→内頸静脈→上大静脈の順に流出する。
上強膜吻合部より下流で静脈圧が上昇すると、Schlemm管から上強膜静脈への房水流出に対する抵抗が増大する3)。慢性例ではSchlemm管内への血液逆流が生じ、線維柱帯を介した房水流出が減少する。その結果、眼圧が慢性的に上昇し、緑内障性視神経障害に至る3)。
主経路の房水流出は眼圧依存性であり、眼圧の上昇とともに流出量が増加する。しかしEVPが上昇した状態では、この代償機構では眼圧正常化に不十分となる。副経路(ぶどう膜強膜路)からの流出は非眼圧依存性であり、EVP上昇の影響を受けにくいため、プロスタグランジン関連薬による副経路からの流出促進が一定の効果を持つ可能性がある。
内頸動脈海綿静脈洞瘻では上強膜静脈圧の上昇に伴い、Schlemm管内への血液流入が認められ、眼圧上昇をきたす。
ゴールドマンの式により、眼圧は房水産生量と流出抵抗に加え、上強膜静脈圧(EVP)によって決定されます。房水はSchlemm管から集合管、上強膜静脈を経て体循環に排出されますが、この流出路の下流で静脈圧が上昇すると、Schlemm管からの房水流出に対する抵抗が増大します。その結果、房水が眼内に貯留して眼圧が上昇します。EVPが1mmHg上昇するとIOPは約0.83mmHg上昇するという線形関係が知られています。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”Rhoキナーゼ阻害薬の上強膜静脈流出への効果が注目されている。ネタスジル0.02%点眼後にEVPが平均-0.79mmHg低下したことが自動静脈圧計を用いた研究で報告されており、赤血球媒介血管造影でも上強膜静脈流出の有意な増加が確認されている。Sturge-Weber症候群関連緑内障6眼においてもネタスジル追加後に有意な眼圧低下が報告された。
日本・韓国で承認されているリパスジルについても、点眼8時間後に上強膜静脈内の房水柱幅が有意に増加し、上強膜静脈流出の増強が示唆されている。
前房内ビマトプロストインプラントは上強膜静脈系を選択的に拡張させ流出を増強する。局所点眼のプロスタグランジン関連薬が上強膜血管全体を拡張させるのに対し、前房内投与では静脈系のみに作用する点で異なる。
QLS-111は上強膜血管を選択的に標的としEVPを低下させる新規局所点眼薬であり、ATP感受性カリウムチャネル調節を介した血管拡張作用を持つ。現在開発中であり、予備データでは有意な眼圧降下と重篤な副作用の不在が示されている。
Radius-Maumenee症候群の手術治療では、XEN45ゲルステントが線維柱帯切除術に対する低侵襲な代替法として報告されている2)。症例1では73か月の長期追跡で良好な眼圧コントロールが得られたが、術後の脈絡膜滲出や嚢胞様黄斑浮腫などの合併症管理が課題として残る2)。
8. 参考文献
Section titled “8. 参考文献”
- Estacia CT, Gameiro Filho AR, da Silveira IBE, et al. Radius-Maumenee syndrome (idiopathic dilated episcleral vessels). GMS Ophthalmol Cases. 2024;14:Doc15.
- Elksne E, Steiner V, Hohensinn M, et al. Radius-Maumenee syndrome: A case series with a long-term follow-up. Clin Case Rep. 2023;11:e06918.
- European Glaucoma Society. European Glaucoma Society Terminology and Guidelines for Glaucoma, 5th Edition. Br J Ophthalmol. 2025.
- 日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2018.
