瞳孔ブロック型の原因薬剤
散瞳・調節麻痺作用を持つ薬剤:フェニレフリン、トロピカミド、シクロペントラート、アトロピン1)
抗コリン作用を持つ全身薬:三環系抗うつ薬、抗精神病薬(オランザピン)、ベンゾジアゼピン(ジアゼパム)、抗ヒスタミン薬1)2)
交感神経刺激作用を持つ薬剤:エピネフリン、ジピベフリン、鼻腔充血除去薬(フェニレフリン含有)、違法刺激薬(コカイン、エクスタシー)2)
その他:ボツリヌス毒素(眼周囲注射)、ジソピラミド(抗不整脈薬)

薬剤誘発性急性隅角閉塞緑内障(drug-induced AACG)は、外用薬または全身投与薬の使用に伴い急性隅角閉塞が誘発される眼科的救急疾患である1)。適切な治療が遅れると不可逆的な視神経障害による永続的視力喪失を招く。
急性隅角閉塞の素因を持つ患者は、遠視眼・短眼軸長・浅前房・狭隅角という解剖学的特徴を有する1)。狭隅角の有病率は白人で約3.8%、アジア人で約8.5%と報告されている1)。そのほかのリスク因子として高齢、女性、家族歴、対側眼のAACG既往が挙げられる1)。
薬剤誘発性AACGの発症機序は、瞳孔ブロック型と非瞳孔ブロック型の2つに大別される1)。瞳孔ブロックが最も一般的なメカニズムであるが、二次性の原因(プラトー虹彩、水晶体誘発性、後水晶体性など)を除外することが重要である3)。
急性発作の症状として、突然の片側性の強い眼痛、充血、頭痛、悪心・嘔吐、霧視、光の周囲の虹視症(ハロー)が出現する2)。全身症状として激しい頭痛・悪心・嘔吐が顕著に現れることがあり、神経疾患や消化器疾患と誤診される場合がある2)。眼圧上昇が40〜80mmHgに達することもある。
| 所見 | 特徴 |
|---|---|
| 眼圧 | 著明な上昇(40〜80mmHg) |
| 角膜 | 浮腫(上皮性が主体) |
| 瞳孔 | 中等度散大・対光反射減弱 |
| 前房 | 浅い(虹彩膨隆を伴う) |
| 結膜 | 毛様充血・静脈うっ血 |
| 水晶体 | グラウコムフレッケン |
隅角鏡検査では広範な虹彩線維柱帯接触(ITC)を認める3)。対側眼の隅角検査でも典型的に閉塞隅角のリスク所見がみられる3)。角膜浮腫のため隅角鏡検査が困難な場合はAS-OCTや超音波生体顕微鏡が有用である2)。
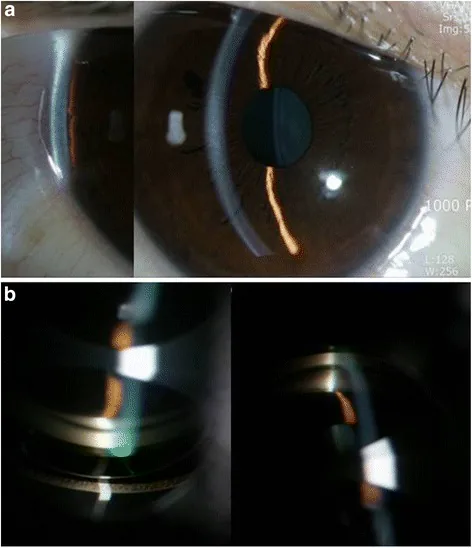
オランザピン誘発性AACの症例では、投薬開始1週間後に右眼のIOP 51mmHg、微小嚢胞性角膜浮腫、中等度散瞳固定、虹彩膨隆を伴う浅前房が認められた1)。超音波生体顕微鏡にて360度の隅角閉塞が確認され、脈絡膜滲出は認められなかった1)。
薬剤誘発性AACGの原因薬剤は、誘発メカニズムに基づき瞳孔ブロック型と非瞳孔ブロック型に分類される。
| 薬剤分類 | 代表的薬剤 | メカニズム |
|---|---|---|
| 散瞳薬・調節麻痺薬 | フェニレフリン、トロピカミド | 瞳孔ブロック |
| 三環系抗うつ薬 | アミトリプチリン、イミプラミン | 瞳孔ブロック |
| SSRI | パロキセチン、エスシタロプラム | 瞳孔ブロック/ぶどう膜滲出 |
| 抗精神病薬 | オランザピン | 瞳孔ブロック |
| 抗てんかん薬 | トピラマート | 非瞳孔ブロック |
| 気管支拡張薬 | イプラトロピウム | 瞳孔ブロック |
瞳孔ブロック型の原因薬剤
散瞳・調節麻痺作用を持つ薬剤:フェニレフリン、トロピカミド、シクロペントラート、アトロピン1)
抗コリン作用を持つ全身薬:三環系抗うつ薬、抗精神病薬(オランザピン)、ベンゾジアゼピン(ジアゼパム)、抗ヒスタミン薬1)2)
交感神経刺激作用を持つ薬剤:エピネフリン、ジピベフリン、鼻腔充血除去薬(フェニレフリン含有)、違法刺激薬(コカイン、エクスタシー)2)
その他:ボツリヌス毒素(眼周囲注射)、ジソピラミド(抗不整脈薬)
非瞳孔ブロック型の原因薬剤
トピラマート:毛様体上腔滲出・毛様体前方回旋・水晶体膨化により前房が浅くなる。投与開始2週間以内に発症し、ほぼ全例が両眼性2)3)
サルファ剤:水晶体膨隆・網膜浮腫・脈絡膜滲出による二次的な前房浅小化
SSRI(一部):エスシタロプラム・ベンラファキシンではぶどう膜滲出を伴う両眼性の隅角閉塞が報告されている2)
抗凝固薬:自発性脈絡膜出血による虹彩-水晶体隔膜の前方移動
散瞳作用や調節麻痺作用を持つ薬剤は、浅前房・厚い水晶体などの解剖学的素因を持つ眼でAPACAを誘発しうる2)。これは散瞳により瞳孔ブロックと隅角混雑が増強されるためである2)。具体的にはSSRI抗うつ薬、三環系抗うつ薬、鼻腔充血除去薬(抗ヒスタミン含有)、抗コリン薬、交感神経刺激薬、制吐薬が含まれる2)。
ネブライザーによる気管支拡張薬(イプラトロピウム臭化物・サルブタモール)も急性隅角閉塞を誘発しうる3)。全身麻酔中または麻酔後にも急性隅角閉塞が発生することがある3)。
大きく2つのメカニズムに分けられます。瞳孔ブロック型では散瞳作用を持つ薬剤(交感神経刺激薬、抗コリン薬、三環系抗うつ薬、SSRI、抗精神病薬、ベンゾジアゼピン、気管支拡張薬)が原因となります。非瞳孔ブロック型ではトピラマートやサルファ剤が毛様体浮腫・脈絡膜滲出を引き起こし、虹彩-水晶体隔膜を前方に押し出すことで隅角閉塞を誘発します。いずれの場合も解剖学的素因(浅前房・狭隅角・遠視眼)を持つ患者でリスクが高くなります。
薬剤誘発性AACGの診断には、臨床所見の評価と詳細な薬剤歴の聴取が不可欠である。急性隅角閉塞の高い割合が外用薬または全身薬により誘発されるため、処方薬・非処方薬を含む完全な薬剤歴を確認する必要がある3)。
隅角鏡検査は両眼で実施すべきである2)。角膜浮腫により罹患眼の隅角鏡検査が困難な場合でも、対側眼の所見は診断に有用である2)。
**前眼部光干渉断層計(AS-OCT)および超音波生体顕微鏡(UBM)**は、角膜浮腫がある場合でも前房深度・隅角形態・毛様体の状態を評価できる2)。超音波生体顕微鏡は脈絡膜や毛様体の腫大・回旋を特定するのに特に有用であり、非瞳孔ブロック型の診断に重要である。
二次性の原因を鑑別するために、対側眼で開放隅角・深い前房が認められる場合、罹患眼の角膜が比較的透明な場合、虹彩新生血管がある場合は注意が必要である2)。
薬剤歴・水晶体の状態・隅角と虹彩の解剖・急性隅角閉塞の側性(片側/両側)を総合的に評価することが原因解明に役立つ。両眼性の急性隅角閉塞はまれであるが、トピラマートやSSRIなど薬剤関連メカニズムの存在を示唆する2)。
薬剤誘発性AACGの治療は、まず急速な眼圧下降を優先し、原因メカニズムに応じた介入を行う2)。
薬物治療
アセタゾラミド:IOP≥40mmHgでは即時投与が推奨される。嘔吐時や迅速な効果が必要な場合は静注(10mg/kg)が望ましい3)
マンニトール:アセタゾラミドへの反応が不十分な場合に考慮する。0.5〜1.5g/kgを15〜20%溶液として静注する3)
ピロカルピン:1〜2%を点眼する。括約筋虚血時は無効であり、眼圧下降後に縮瞳が得られる3)
ステロイド点眼:炎症軽減のため頻回投与(1日4〜6回)を行う3)
レーザー・手術治療
レーザー虹彩切開術(LPI):瞳孔ブロック型の標準治療。角膜が十分透明になった時点で施行する。対側眼にも予防的レーザー虹彩切開術を行う1)3)
レーザー虹彩形成術:角膜浮腫が持続しLPIが施行困難な場合、または薬物療法で1〜2時間以内に眼圧が下がらない場合に有用3)
水晶体摘出術:薬物・LPIに反応しない場合に考慮する3)
トピラマート型の治療:原因薬剤の即時中止、調節麻痺薬点眼、ステロイド点眼が基本。レーザー虹彩切開術は無効1)
オランザピン誘発性AACの症例では、チモロール0.5%・ブリモニジン0.15%の点眼、経口アセタゾラミド、ピロカルピン2%投与後にNd:YAGレーザー虹彩切開術を施行し、翌日にIOP 51mmHgから20mmHgに低下、視力も6/200から20/30に回復した1)。対側眼にも予防的レーザー虹彩切開術が施行された1)。
全身薬(アセタゾラミド・マンニトール)は高齢者や併存疾患を持つ患者において、感覚異常・錯乱から肺水腫・急性腎不全に至る重篤な副作用を起こしうるため注意が必要である2)。
治療は原因メカニズムにより異なります。瞳孔ブロック型ではまず眼圧降下薬(アセタゾラミド静注、マンニトール点滴)で眼圧を下げ、角膜が透明になった時点でレーザー虹彩切開術を施行します。対側眼にも予防的レーザー虹彩切開術を行います。トピラマートなど非瞳孔ブロック型では原因薬剤の即時中止が最も重要であり、調節麻痺薬とステロイド点眼を使用します。いずれの場合も原因薬剤の特定と中止、および処方医との連携が必要です。
瞳孔ブロックは薬剤誘発性AACGの最も一般的なメカニズムである3)。交感神経刺激作用または副交感神経遮断作用を持つ薬剤が散瞳を誘発すると、虹彩と水晶体の接触面積が増大する1)。これにより後房から前房への房水の経瞳孔的流出に対する抵抗が上昇し、後房圧が前房圧を上回る3)。
後房圧の上昇により虹彩は前方に膨隆し(虹彩膨隆)、周辺部虹彩が線維柱帯を覆うことで房水流出路が閉塞され、急激な眼圧上昇が生じる3)。括約筋と散大筋の両方が共活性化される中等度散瞳位が最もリスクが高い3)。
オランザピンの症例では、弱い抗コリン作用が散瞳を誘発し、解剖学的に素因のある眼で瞳孔ブロックが発生した1)。非定型抗精神病薬による隅角閉塞緑内障はまれであるが、SSRIや三環系抗うつ薬と比較して報告が少ない1)。
トピラマートやサルファ剤は特異体質的薬物反応により、毛様体上腔滲出を引き起こす3)。これにより毛様体が前方に回旋し、水晶体弛緩帯の弛緩と水晶体の膨化が生じ、虹彩-水晶体隔膜全体が前方に移動して隅角を閉塞する2)。
この機序は開放隅角・狭隅角いずれの患者でも発生しうる。ベンラファキシンやエスシタロプラムによるぶどう膜滲出を伴う両眼性の急性隅角閉塞も報告されている2)。
プラトー虹彩形態は、前方に位置する毛様体突起が周辺虹彩を前方に押し上げ、散瞳時に直接隅角を閉塞する3)。瞳孔ブロック解除後も高眼圧が持続する場合、プラトー虹彩の関与を疑う必要がある。
瞳孔ブロック型は散瞳により虹彩と水晶体の接触が増大し、後房から前房への房水流出が妨げられることで虹彩が前方に膨隆し隅角を閉塞します。散瞳薬・抗コリン薬・交感神経刺激薬が原因となり、レーザー虹彩切開術が有効です。一方、非瞳孔ブロック型はトピラマートやサルファ剤による毛様体浮腫・脈絡膜滲出が原因で、虹彩-水晶体隔膜全体が前方に押し出されます。この型では虹彩切開術は無効であり、原因薬剤の中止と調節麻痺薬が治療の柱となります。両眼性発症は非瞳孔ブロック型を強く示唆します。
2025年に発表された国際コンセンサスでは、急性原発閉塞隅角発作の用語として**APACA(acute primary angle closure attack)**が提唱された2)。この用語は疾患の急性かつ緊急な性質を強調し、二次性の原因との区別を明確にする2)。また、迅速な眼圧下降が正確な診断に優先すべきであるとのコンセンサスが100%の合意で得られた2)。
コンセンサスステートメントでは、散瞳・調節麻痺作用を持つ薬剤が解剖学的素因のある眼でAPACAを誘発しうることが88.24%の合意で確認された2)。リスクのある患者への薬剤処方時には注意が必要であり、詳細な薬剤歴が診断の重要な手がかりとなる2)。
診断目的の薬理学的散瞳は一般集団では安全であり、散瞳不足による眼底疾患の見逃しリスクのほうが隅角閉塞誘発リスクよりもはるかに高い3)。適切な予防的治療(レーザー虹彩切開術)を受けた隅角閉塞既往患者では散瞳は通常安全である3)。散瞳後にピロカルピンで予防的に縮瞳させることは、中等度散瞳位での瞳孔固定を招き隅角閉塞リスクを増大させるため避けるべきである3)。
- Alarfaj MA, Almater AI. Olanzapine-Induced Acute Angle Closure. Am J Case Rep. 2021;22:e934432.
- Chan PP, et al. Acute primary angle closure attack - controversies and consensus. Prog Retin Eye Res. 2025.
- European Glaucoma Society. European Glaucoma Society Terminology and Guidelines for Glaucoma, 5th Edition. Br J Ophthalmol. 2025.