眼外アプローチ
冷凍凝固術:3時間以内の比較的小さな解離が適応。-85℃で2〜3回の凍結・融解サイクルを行う。初回成功率36〜50%
ジアテルミー:部分層強膜弁下でジアテルミーピンを適用。治療範囲は4時間を超えない

毛様体解離(cyclodialysis cleft)とは、毛様体筋の縦走線維が強膜突起から分離し、前房と脈絡膜上腔の間に直接的な連通路が形成された状態を指す。この連通路を通じて房水が脈絡膜上腔へ過剰に流出するため、眼は低眼圧に陥る。
多くは自然に閉鎖するが、閉鎖しない場合は慢性的な低眼圧を引き起こす。低眼圧の持続は低眼圧黄斑症、視神経乳頭浮腫、視力低下を招く。
最も一般的な原因は鈍的外傷であるが、線維柱帯切除術・隅角切開術・白内障手術・MIGS(micro-invasive glaucoma surgery)などの眼内手術後にも発生しうる1)。鈍的外傷後の発生頻度は稀であり、ある回顧的研究では145眼中わずか3眼(2%)に毛様体解離が認められた。
かつては開放隅角緑内障に対する治療法として意図的に毛様体解離を作成する手法もあったが、現在ではほぼ行われていない。
毛様体解離は、毛様体が強膜突起(隅角の骨格構造)から剥がれて、前房と脈絡膜上腔が直接つながった状態です。このため房水が通常の経路ではなく脈絡膜上腔へ過剰に流出し、眼圧が著しく低下します。主な原因は目への強い打撲や眼内手術です。多くは自然に閉じますが、閉じない場合は低眼圧による視力障害を防ぐための治療が必要になります。
低眼圧に伴う症状が主体である。
眼圧が4 mmHg以下になると高度の視力低下(0.2以下)をきたす頻度が高い。
定義上、解離部からの房水流出増加は脈絡膜上液をもたらすが、目に見える脈絡膜剥離や前房の浅層化は一般的な所見ではない。遠い過去の眼外傷歴も重要であり、以前閉鎖した解離部が手術中に再開通することがある。
毛様体解離の原因は大きく外傷性と医原性に分けられる。
外傷では毛様体筋縦走線維と輪状筋の間で断裂が起こり、毛様体が虹彩とともに後方に移動する。損傷部位は虹彩根部(虹彩離断)、毛様体内(隅角後退)、毛様体-強膜間(毛様体解離)と段階的に強膜側へ移行する。
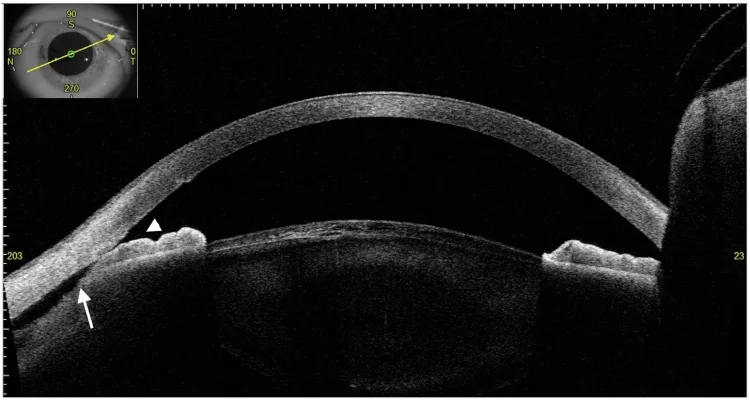
隅角鏡検査では、毛様体解離は強膜突起より後方の異常な深い領域として観察される。虹彩根部と毛様体が後方に変位している。解離領域は白色(強膜様)、黒色、または灰色に見える。
ただし、低眼圧で浅前房・前房消失している眼や、角膜浮腫・前房出血がある場合は隅角の評価が困難である。前房内に粘弾性物質を注入することで視認性が向上する場合がある。広範な周辺虹彩前癒着に隣接して解離部が隠れていることもあり、注意深い検索が必要である。
超音波生体顕微鏡は高周波Bモードトランスデューサー(50〜100 MHz)を使用し、25〜50μmの高解像度で前眼部構造を画像化する。毛様体解離の有無・大きさ・関連する脈絡膜上液を特定するための最良の検査法である。
隅角鏡で検出できない解離も超音波生体顕微鏡では同定可能であり、外傷後低眼圧で解離が疑われた6眼のシリーズでは、隅角鏡で確認されたのは1眼のみであったが超音波生体顕微鏡では6眼すべてで特定された。角膜混濁がある場合でも使用可能である。
AS-OCTは非接触で迅速に取得できる利点があるが、虹彩後面の色素沈着が光の透過を妨げるため、毛様体や脈絡膜上腔の十分な可視化は困難である。角膜混濁も画像品質を低下させる。毛様体解離の評価における有用性は限定的である。
| 検査法 | 解像度 | 利点 |
|---|---|---|
| 隅角鏡 | 肉眼 | 簡便・即時評価可能 |
| 超音波生体顕微鏡 | 25〜50μm | 最良の検出能 |
| AS-OCT | 18〜100μm | 非接触・迅速 |
超音波生体顕微鏡(UBM)が最も優れた検査法です。隅角鏡検査では検出できない小さな解離も超音波生体顕微鏡では同定でき、角膜混濁がある場合でも使用可能です。前眼部OCTは非接触で簡便ですが、虹彩色素により毛様体の可視化が制限されるため有用性は限定的です。
調節麻痺薬が第一選択である。毛様体筋の緊張を緩和させ毛様体輪を拡大させることで、剥離した筋線維を強膜に密着させる。
毛様体解離が1〜2週間で軽快しない場合は次のステップに進む。保存的治療のみで軽快する例も多い。ただし眼圧4 mmHg以下の場合は2か月以内に眼圧を回復させる必要がある。
薬物療法で閉鎖しない場合に適応となる。局所的な炎症を誘発し、脈絡膜と強膜の癒着を促進して解離部を封鎖する。
緑や黄色波長のレーザーで毛様体が少し収縮し少量のフィブリンが析出する程度の凝固を行う。
| レーザー | 出力 | 照射時間 |
|---|---|---|
| アルゴン | 0.3〜3W | 500ms |
| ダイオード | 1500〜2500mW | 1500〜2000ms |
| エンドレーザー | 3W | 1000ms |
眼外アプローチ
冷凍凝固術:3時間以内の比較的小さな解離が適応。-85℃で2〜3回の凍結・融解サイクルを行う。初回成功率36〜50%
ジアテルミー:部分層強膜弁下でジアテルミーピンを適用。治療範囲は4時間を超えない
眼内アプローチ
直接的毛様体固定術(cyclopexy):最もよく研究された方法。強膜弁下で毛様体を直視し、8-0〜9-0ナイロンで強膜に縫着。初回成功率67〜96%、2回でほぼ100%
前房横断的毛様体固定術:偽水晶体眼・無水晶体眼に適応。強膜弁不要で手技が簡便
その他にSF6ガス注入、硝子体切除術併用のガス注入、一時的強膜バックリング、IOLハプティクスの毛様溝配置、嚢拡張リング(CTR)の縫着なども報告されている。
解離閉鎖後に半数以上の眼で著明な眼圧上昇を経験する。通常は一過性であり、局所眼圧降下薬・経口炭酸脱水酵素阻害薬・高浸透圧薬で管理可能である。稀に濾過手術を要する。解離が大きいほど眼圧正常化に時間がかかり、低眼圧の持続期間が長いほど眼圧スパイクの発生率が高い傾向がある。
MIGS後に生じた2つの毛様体解離が順次閉鎖し、55 mmHgと54 mmHgの同等な眼圧スパイクが2回連続で発生した症例が報告されている1)。従来の代償機序(房水産生亢進・線維柱帯流出低下)による説明では、最初の閉鎖後に一部正常化しているはずの2回目のスパイクが同等の大きさであることは説明しにくく、解離閉鎖自体に対する直接的な反応である可能性が示唆されている1)。
正確な機序は未解明ですが、主に2つの仮説があります。(1)解離による過剰な房水流出に対抗するため毛様体の房水産生が代償的に亢進しており、解離閉鎖後もこの亢進が一時的に持続する、(2)解離が開存している間に線維柱帯やシュレム管の排出機能が低下(虚脱・線維化)しており、正常化に時間を要する、というものです。最近の症例報告では、解離閉鎖自体に対する直接的反応の可能性も示唆されています。
毛様体筋は縦走筋(Brücke筋)、斜走筋、輪状筋(Müller筋)の3層から構成され、いずれも前方では強膜突起に付着する。鈍的外傷では前房内圧の急激な上昇により角膜輪部が伸展し、房水が後方および隅角部へ移動することで虹彩・毛様体に機械的ストレスが加わる。
損傷は軽度から重度まで段階的であり、虹彩根部の断裂(虹彩離断)→毛様体内の裂隙形成(隅角後退)→毛様体の強膜からの完全剥離(毛様体解離)の順に進行する。
毛様体解離により前房と脈絡膜上腔が直接連通すると、通常のぶどう膜強膜流出路を介さずに房水が大量に脈絡膜上腔へ流出する。これに加え、損傷した毛様体による房水産生の低下も寄与する場合がある。
著しい低眼圧になると眼球後部が前方にたわみ、黄斑に皺襞が形成される。眼圧が10 mmHg以下で発症しうるが、5 mmHg以下で発症率が上昇する。4 mmHg以下が2〜3か月持続すると視力回復が不良となり、変視症や比較中心暗点が残りやすい。若年者および強度近視眼が発症リスク因子である。
解離閉鎖後の眼圧上昇には複数のメカニズムが推定されている1)。
MIGS後に生じた2つの毛様体解離が順次閉鎖し、各々で同等の眼圧スパイク(55/54 mmHg)が発生した症例報告は、従来の代償性亢進仮説では説明しきれない現象を提示している1)。解離閉鎖自体が眼圧上昇を直接惹起する可能性が示唆されており、そのメカニズムの解明は今後の重要課題である1)。
一般的には3か月以内の介入が推奨されるが、数か月〜数年にわたる低眼圧の後に視力が回復した症例も報告されている。長期にわたる毛様体解離であっても治療を躊躇すべきではないとされる。眼圧4 mmHg以下が持続する場合は2か月以内の眼圧回復が望ましい。
毛様体解離が解消した眼は少なくともある程度の隅角後退を伴うため、将来的な隅角後退緑内障の発症に注意した長期経過観察が必要である。
- Alshaikhsalama A, Nathan N. Cyclodialysis clefts following microinvasive glaucoma surgery with consecutive intraocular pressure spikes. Case Rep Ophthalmol Med. 2022;2022:7595507.