瞳孔ブロック
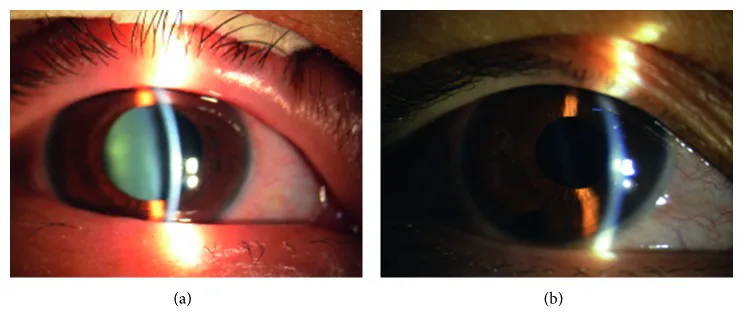
虹彩形態:周辺部虹彩の前方膨隆(iris bombé)
前房深度:周辺部が特に浅い
PI:閉塞または未施行
縮瞳薬:有効

房水誤導は、房水が正常な前方経路ではなく後方(硝子体腔側)へ誤導されることで、虹彩水晶体隔膜が前方に押し出され、隅角閉塞と眼圧上昇を引き起こす病態である。悪性緑内障(malignant glaucoma)、毛様体ブロック緑内障(ciliary block glaucoma)とも呼ばれる。ICD-10コードはH40.8。
1869年にVon Graefeが初めて報告した歴史的な疾患概念である3)。二次性閉塞隅角のうち「水晶体後方の押し出し機序(posterior pushing mechanism)」に分類される5)。
濾過手術後の発生率は0.6〜4%とされる。女性に多く、通常は片眼性に発症する。原発閉塞隅角緑内障眼の濾過手術後に最も多いが、白内障手術を含むあらゆる内眼手術後に生じうる5)。まれに自然発症の報告もある。
瞳孔ブロックでは瞳孔縁での房水通過障害により周辺部虹彩が前方へ膨隆(iris bombé)する。一方、房水誤導では水晶体後方から房水が硝子体腔に蓄積するため、前房が均一に浅くなる点が異なる。瞳孔ブロックには縮瞳薬が有効だが、房水誤導では縮瞳薬は禁忌である。
急性発症の場合は以下の症状を呈する。
症状は変動性(fluctuant)であり、白内障手術後数週〜数年経ってから顕在化することがある3)。初期には眼圧が正常範囲内の場合もある5)。
以下の所見の組み合わせで診断する。
AS-OCTでは、CTR-IOL複合体の前方偏位に伴いplateau iris様の所見(虹彩中央部は平坦だが隅角は閉塞)を示すことが報告されている2)。超音波生体顕微鏡では水晶体嚢-IOL複合体の前方偏位や毛様体の位置異常を直接確認できる4)。
最も多い誘因は内眼手術である5)。
小さい眼球ほどリスクが高い5)。
片眼に発症した場合、対側眼の発症リスクも上昇する3)。
| リスク因子 | 具体例 |
|---|---|
| 眼球形態 | 短眼軸(<21 mm)、高度遠視(>+6 D)、浅前房 |
| 手術 | 濾過手術、白内障手術、CTR留置 |
| 薬剤 | トピラマート、SSRI |
トピラマートは毛様体脈絡膜の血管透過性を亢進させ、毛様体の腫脹と前方回旋を引き起こす1)。小眼球症などのハイリスク眼では房水誤導の引き金となりうる。SSRIも散瞳作用を介して狭隅角眼に隅角閉塞を誘発する可能性がある。
房水誤導は除外診断である。瞳孔ブロック、脈絡膜出血・剥離、上脈絡膜出血を除外した上で診断する4)。
瞳孔ブロック
虹彩形態:周辺部虹彩の前方膨隆(iris bombé)
前房深度:周辺部が特に浅い
PI:閉塞または未施行
縮瞳薬:有効
房水誤導
虹彩形態:虹彩は全体的に前方偏位
前房深度:均一に浅い〜消失5)
PI:開存している
縮瞳薬:禁忌(悪化)
その他の鑑別として、脈絡膜出血(Bスキャンで高輝度エコー)、脈絡膜剥離(漿液性、低輝度エコー)、水晶体膨脹による閉塞隅角がある。
日本の教科書に基づく処方例を以下に示す。
| 薬剤 | 用法 |
|---|---|
| アトロピン点眼液1% | 1日1回点眼 |
| チモロール点眼液0.5% | 1日2回点眼 |
| ダイアモックス錠250 mg | 2錠 分2食後 |
高浸透圧薬(マンニトール点滴等)を併用し硝子体液を減少させるとともに、アトロピンにより毛様筋を弛緩させてブロックの解除を図る。房水産生抑制薬の点眼・内服も併用する。
EGSガイドラインでも副交感神経遮断薬(アトロピンまたはシクロペントラート)、房水産生抑制薬、高浸透圧薬の三者併用が推奨されている5)。薬物療法の奏効率は約50%(5日以内)とされるが、薬物単独での再発率は最大100%と報告されている。
偽水晶体眼ではNd:YAGレーザーによる後嚢切開を行い、さらに後嚢後方にフォーカスをずらして3〜4 mJのエネルギーで10〜20発照射し前部硝子体を破砕する。奏効した場合、直後〜翌日に前房深度の改善と眼圧下降が得られる。
ダイオードレーザー毛様体光凝固術(CPC)はいつの段階でも考慮しうる5)。
薬物・レーザー治療で効果不十分な場合、または再発例では手術を行う5)。
房水誤導は水晶体後方の押し出し機序による閉塞隅角である。縮瞳薬は毛様筋を収縮させ、水晶体-虹彩隔膜の前方移動を促進するため病態を悪化させる5)。これに対し、アトロピンなどの散瞳・調節麻痺薬は毛様筋を弛緩させてブロックの解除に有効である。
片眼での発症は対側眼のリスクを有意に上昇させる3)。緑内障の既往の有無にかかわらずリスクは高まるため、対側眼の定期的な眼圧・前房深度の評価が重要である。
房水誤導の正確な発症機序は未だ完全には解明されていないが、以下の機序が関与すると考えられている5)。
脈絡膜膨脹説
主要機序:脈絡膜の容積増大が後方から前方への液体移動に抵抗を生じさせる5)
結果:房水が硝子体腔に蓄積し、虹彩-水晶体隔膜を前方へ押し出す
毛様体ブロック説
主要機序:毛様体突起と水晶体(またはIOL)赤道部、前部硝子体膜の異常な解剖学的接触
結果:一方向弁として作用し、房水の前方流出を阻害する「悪性サイクル」が成立する
偽水晶体眼ではIOL-嚢複合体の水平径が天然水晶体より大きく、毛様体突起に接触しやすい4)。毛様体突起で産生された房水の一部が後方(硝子体腔)へ分泌される。前部硝子体膜が intact であれば前方への液体流出が妨げられ、圧較差が生じて前房が浅くなる。
硝子体切除術既往眼であっても、前部硝子体膜が残存していれば発症しうることが報告されている4)。
トピラマートは毛様体脈絡膜血管の透過性を亢進させ、毛様体・脈絡膜の腫脹と毛様体の前方回旋を引き起こす1)。小眼球症では強膜肥厚による渦静脈ドレナージ障害が加わり、uveal effusionのリスクがさらに上昇する1)。
CTR留置により水晶体嚢が拡大・肥厚し、CTR-IOL複合体が全周性に毛様体および後部虹彩に接触する2)。これにより毛様体腔が圧迫され、房水の後方から前方への移動に対する抵抗が増大する。CTR-IOL複合体の大きな径は前方偏位を部分的に制限するため、前房深度が保たれたままplateau iris様の隅角閉塞を呈することがある2)。
Cheanら(2021)は、白内障手術後に近視化(myopic surprise)を唯一の初期徴候として発症した房水誤導の1例を報告した3)。術後約3年間は眼圧が正常範囲内であり、診断が遅延した。生体計測による前房深度が一見正常であっても、短眼軸眼では計測誤差が生じうるため、近視化を認めた場合には房水誤導を鑑別に含めるべきとされた。
Stephensonら(2023)は、硝子体切除術・白内障手術・人工虹彩留置の既往眼で3 D以上のmyopic shiftとともに房水誤導を発症した症例を報告した4)。硝子体切除後でも前部硝子体膜が残存していれば発症しうることを示し、goniosynechialysis+虹彩切除+zonulo-hyaloidectomyにより屈折と眼圧が回復した。
Gotoら(2024)は、CTR-IOL複合体の前方偏位による二次性隅角閉塞をAS-OCTで初めて特徴づけた2)。前房深度が保持されたままのplateau iris様所見という非典型的な像を報告し、白内障手術+CTR留置後の二次性隅角閉塞の検出にAS-OCTが有用であることを示した。
薬物療法→Nd:YAGレーザー→cyclodiode→手術という段階的アプローチが提唱されている3)。Cyclodiodeは毛様体突起の凝固壊死と萎縮を引き起こし、毛様体-硝子体界面の破壊と毛様体の後方回旋をもたらす可能性がある。しかし、毛様体-硝子体界面を破壊するために必要な照射条件は未確立であり、薬物・レーザーのみでは効果不十分な場合にはunicameral eyeを作成する手術が依然として最終的な治療選択肢となる3)。