適応
片眼性の全周性LSCD:もっとも典型的な適応である。
部分的LSCD:全周性でなくても適応となりうる。
化学外傷・熱傷後:最も高頻度の適応である2)。
CLET失敗後の再手術:過去のLSCD手術不成功例にも施行される2)。
眼表面腫瘍切除後:輪部の広範な欠損を伴う場合に検討される。

簡易輪部上皮移植術(simple limbal epithelial transplantation; SLET)は、片眼性の輪部幹細胞疲弊症(limbal stem cell deficiency; LSCD)に対する眼表面再建手術である。2012年にインドのSangwanらが初めて報告した2)。
SLETでは健側眼の上方輪部から約2mm(1時間幅)の輪部組織を採取する。採取した組織を6〜10個の小片に分割し、罹患眼の角膜上にヒト羊膜(HAM)を敷いた上に配置する。小片はin vivoで増殖し角膜上皮を再生する。
本手技の最大の利点は、CLETのような培養施設が不要であり、CLAuよりもドナー眼から採取する組織量が少ない点にある2)。自家移植であるため全身免疫抑制も不要である。
片眼性のLSCDで、対側眼が健康な場合に適応される。化学外傷・熱傷が最も多い適応である2)。その他、医原性LSCD、コンタクトレンズ装用による LSCD、眼表面腫瘍切除後、過去のLSCD手術失敗例なども適応となる。角膜実質に混濁がある場合はSLETに加えて角膜移植が必要となる。
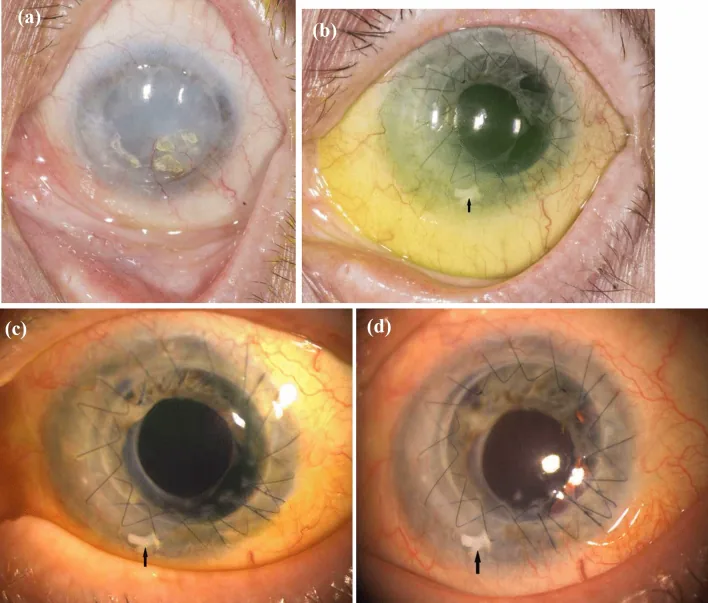
LSCDは角膜上皮幹細胞の機能障害により角膜上皮の正常な恒常性が維持できなくなった状態である1)。輪部幹細胞はVogt柵(palisades of Vogt)と呼ばれる特殊な構造に存在する1)。幹細胞が損傷されると角膜上皮が結膜上皮に置換(結膜化)され、角膜の透明性が失われ視力が低下する1)。
LSCDの原因として化学外傷が最も多く、そのほか無虹彩症、コンタクトレンズ装用、Stevens-Johnson症候群が知られている1)。LSCDに対して角膜移植のみを施行しても、上皮の破綻が繰り返され移植片不全に至るため、輪部幹細胞移植による眼表面再建が必要である2)。
適応
片眼性の全周性LSCD:もっとも典型的な適応である。
部分的LSCD:全周性でなくても適応となりうる。
化学外傷・熱傷後:最も高頻度の適応である2)。
CLET失敗後の再手術:過去のLSCD手術不成功例にも施行される2)。
眼表面腫瘍切除後:輪部の広範な欠損を伴う場合に検討される。
禁忌
ドナー眼の将来的LSCD リスク:対側眼に将来LSCDを生じる可能性がある場合は輪部採取を避ける。
角結膜の角化:レシピエント眼の上皮環境が不適切である。
重度のドライアイ:幹細胞の生着・増殖が困難である。
視力予後のない眼:手術の利益が期待できない。
未矯正の眼附属器疾患:兎眼、眼瞼外反などは術前に修正する。
移植幹細胞が増殖するための適切な環境を整備する。化学外傷後の症例では眼表面の炎症をSLET施行前に治療する。経口ドキシサイクリン、局所シクロスポリン、防腐剤無添加人工涙液を使用する。眼瞼の問題がある場合は術前に修正する。
術後1日目、1週目、1か月目に診察し、以降は必要に応じてフォローアップする。コンタクトレンズは7〜10日間留置する。術後2週までに角膜表面の完全な上皮化が得られ、8週までに移植片の透明化が期待される。羊膜は数週間で溶解する。小児では上皮化・透明化が成人より早い。
系統的レビューにおけるSLETの成績は以下の通りである2)。
| 術式 | 解剖学的成功率 | 機能的成功率 |
|---|---|---|
| SLET | 78% | 68.6% |
| CLAu | 81% | 74.4% |
| CLET | 61.4% | 53% |
SLETとCLAuの成績は同等であり、いずれもCLETより有意に良好であった(解剖学的成功 p=0.0048、機能的成功 p≤0.0001)2)。SLETとCLAuの機能的成功率の差は統計学的に有意ではなかった(p=0.27)2)。ドナー眼において重篤な有害事象は報告されていない2)。
系統的レビューでは解剖学的成功率(安定した上皮化角膜表面)78%、機能的成功率(最高矯正視力〔BCVA〕2段階以上の改善)68.6%と報告されている2)。CLAu(81%/74.4%)と同等であり、CLET(61.4%/53%)より有意に良好であった2)。
酸外傷、重度の瞼球癒着、角膜移植術との併用、術後の移植片喪失が失敗と関連する。
CLETのようにドナー細胞の温存ができないこと、フィブリン糊と羊膜のコスト・入手性が制限要因となりうることが挙げられる2)。結膜病変が軽度の症例にはSLET、重度の瞼球癒着を伴う症例にはCLAuが推奨される2)。
結膜病変が軽度(瞼球癒着の程度が少ない)のLSCDにはSLETが推奨される。重度の結膜病変(高度の瞼球癒着)を伴うLSCDにはCLAuが推奨される2)。また羊膜やフィブリン糊のコスト・入手性が制限要因となる場合はCLAuが選択肢となりうる2)。
角膜上皮幹細胞は輪部のVogt柵に存在する1)。これらの幹細胞は求心性に移動しながら基底上皮細胞に分化し、増殖して表層に向かい最終的に脱落する1)。輪部は結膜上皮の角膜への侵入を防ぐバリアとしても機能する1)。
LSCDでは部分的または完全に角膜上皮が結膜上皮に置換される1)。残存する輪部幹細胞がわずか7%でも、現代の外科的手技により角膜上皮を再生させることが可能とされている1)。
SLETでは少量の輪部組織を小片に分割して角膜上に配置し、各小片からin vivoで幹細胞が増殖・遊走して角膜上皮を再生する。羊膜は幹細胞の増殖を促進する足場として機能し、炎症抑制作用も有する。フィブリン糊は小片と羊膜を固定するとともに、生理的な足場としても作用する。
輪部幹細胞移植(LSCT)は3つの術式が発展してきた2)。1989年にKenyonとTsengがCLAuを報告し、1997年にPellegriniらがCLETを報告した2)。2012年にSangwanらがSLETを報告し、CLETの培養工程をin vivoでの増殖に置き換えることで手技を簡略化した2)。
輪部幹細胞には自己複製能と分化能がある1)。SLETでは輪部組織を小片に分割して広い範囲に分散配置することで、各小片からの幹細胞が同時に増殖・遊走して角膜表面を被覆する。羊膜が幹細胞の増殖に適した環境を提供することで、わずか2mm程度の輪部組織から角膜全体の上皮再生が可能となる。