眼合併症

強膜化角膜
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 強膜化角膜とは
Section titled “1. 強膜化角膜とは”強膜化角膜(sclerocornea)は、神経堤細胞の遊走異常により角膜縁原基(limbal anlage)が正常に形成されず、角膜が強膜様に白色混濁する稀な先天性疾患である。非進行性で、両眼性かつ非対称性に発症する。炎症性・感染性の原因とは無関係であり、性差はない。
角膜混濁は白色で血管侵入を伴い、角膜縁の境界が不明瞭となる。欧州ではcornea plana、米国ではsclerocorneaと呼ばれることが多い。
Waring分類
Section titled “Waring分類”| 分類 | 特徴 |
|---|---|
| 孤立性周辺部型 | 他の異常を伴わない周辺部のみの強膜化 |
| 扁平型 | 角膜屈折力38D未満の扁平角膜を伴い強度遠視を呈する |
| 前房異常合併型 | 虹彩角膜癒着など前眼部異常を合併する |
| 全型 | 角膜全体のびまん性混濁 |
症例の50%は常染色体優性(AD)または常染色体劣性(AR)遺伝を示す。残りの50%は孤発性(散発性)に発生する。
強膜化角膜では周辺部角膜が強膜化することで角膜が扁平化するため、扁平角膜を高頻度で合併する。扁平角膜は臨床的にCNA1(常染色体優性、12q)とCNA2(常染色体劣性、KERA遺伝子変異)の2つの遺伝形式に分類される。CNA2ではより高度な角膜扁平化と多数の前眼部異常を伴う。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”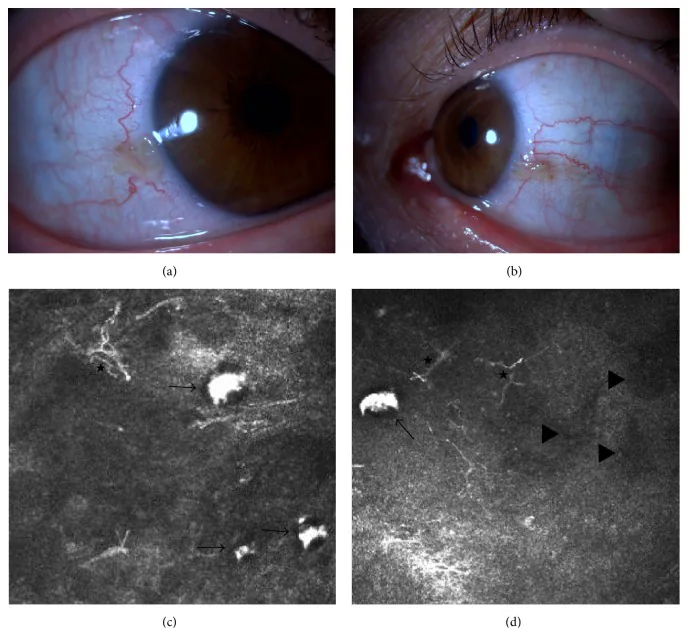
- 視力低下:角膜混濁の範囲と程度に応じて生じる。全型では高度な視力障害を呈する。
- 強度遠視:角膜扁平化により屈折力が25〜42Dに低下する。
- 弱視:乳幼児期の形態覚遮断弱視のリスクが高い。
臨床所見(医師が診察で確認する所見)
Section titled “臨床所見(医師が診察で確認する所見)”- 角膜混濁:周辺部から中心部に向かって強膜様の白色混濁を呈する。全型では角膜全体に及ぶが中心部の混濁密度はやや低い。部分型では中心領域が透明なことがある。
- 角膜縁の消失:角膜と強膜の境界が不明瞭となる。周辺部混濁例では角膜径の正確な評価が困難である。
- 角膜扁平化:側方からの細隙灯観察で角膜の扁平化が一目瞭然に確認できる。
- 角膜血管新生:角膜全層にわたり上強膜および結膜からの血管侵入を認める。
合併する異常
Section titled “合併する異常”全身合併症
知的障害:神経堤細胞異常の全身的な影響として認められる。
難聴:前眼部形成異常症候群の一部として合併する。
頭蓋顔面異常:神経堤細胞由来の組織形成異常に関連する。
心血管奇形:まれに合併する。
泌尿生殖器奇形:まれに合併する。
皮膚異常:神経堤細胞異常に関連する。
強膜化角膜では角膜扁平化と前房の狭小化により続発性緑内障のリスクが高い。発達性緑内障は10代以降に発症する。常染色体劣性変異が存在する症例でリスクがより高いとされる。隅角異常を伴うことも多く、定期的な眼圧評価が不可欠である。
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”発生学的原因
Section titled “発生学的原因”強膜化角膜は、胎生期における神経堤細胞の遊走異常に起因する。正常発生では胎生7〜10週に角膜縁原基(limbal anlage)が形成され、角膜曲率と角膜・強膜の境界を規定する。この構造が形成されないことで強膜と角膜の正常な境界が乱れ、角膜曲率が平坦化する。
- CNA1(扁平角膜1型):常染色体優性遺伝。第12染色体q腕に遺伝子座があるが原因遺伝子は未同定。
- CNA2(扁平角膜2型):常染色体劣性遺伝。12q22-q23領域のKERA遺伝子の変異による。KERA遺伝子は角膜の透明性に重要なケラタン硫酸プロテオグリカンであるケラトカン(keratocan)をコードする。CNA2ではより高度な角膜扁平化と前眼部異常を伴う。
- PAX6、FOXC1、PITX2:変異により虹彩角膜癒着、瞳孔異位、虹彩萎縮を伴うことがある。
- RAD21:強膜化角膜家系で同定された変異。WNT9Bシグナルを介して神経堤細胞から角膜角化細胞または強膜実質細胞への分化方向を制御する。
4. 診断と検査方法
Section titled “4. 診断と検査方法”眼科的検査
細隙灯顕微鏡検査:角膜混濁の範囲・程度、角膜縁の不明瞭化、血管侵入の有無を評価する。側方からの観察で角膜の扁平化を確認できる。
前眼部OCT(AS-OCT):非侵襲的で迅速な評価が可能である。新生児に対して麻酔なしで評価できる利点がある。角膜の厚さと高反射による強膜化を描出する。
超音波生体顕微鏡(UBM):前眼部を深さ5mmまで詳細に描写する。前房の狭小化、虹彩角膜癒着、隅角異常を評価する。
全身検査
遺伝学的検査:KERA、PAX6、FOXC1、PITX2、RAD21などの遺伝子変異を検索する。遺伝カウンセリングと併せて実施する。
全身的評価:知的障害、難聴、心血管奇形、泌尿生殖器奇形など関連する全身異常の有無を検索する。
- Peters anomaly:角膜中央部の混濁とDescemet膜・角膜内皮の欠損を伴う。虹彩角膜癒着や虹彩水晶体癒着を呈する。
- 先天緑内障:角膜浮腫による混濁であり、角膜径増大(牛眼)とDescemet膜破裂(Haab’s striae)を伴う点で鑑別される。
- 先天遺伝性角膜内皮ジストロフィ(CHED):両眼性のびまん性角膜浮腫・混濁であるが、角膜縁は明瞭である。
- 分娩時外傷:片眼性であることが多く、Descemet膜破裂を伴う。
5. 標準的な治療法
Section titled “5. 標準的な治療法”視軸に影響する角膜混濁に対しては全層角膜移植術(PKP)が第一選択となる。形態覚遮断弱視を回避するため、手術はできるだけ早期に実施する必要がある。ただし視力予後は不良であり、移植片拒絶反応率が高い。
移植成績に関する報告:
- Kimらは強膜化角膜に対する全層角膜移植の75%で不成功を示した。移植不全の主因は角膜縁領域の血管新生であった。
- FruehとBrownは全型15眼・部分型12眼の最大規模シリーズで1年移植片生存率70%を報告した。
- Michaeliらは小児6名12眼で1年後の移植片透明維持率がわずか37%であったと報告した。
角膜移植不全例では周辺部の血管新生が危険因子であり、同時に前眼部再建手術(隅角再建術、瞳孔形成術、水晶体摘出術、眼内レンズ整復術など)を要する場合がある1)。
視軸が保たれている部分型では光学矯正(眼鏡)を早期に行い、強度遠視による弱視を予防する。緑内障合併例には点眼薬や手術による眼圧管理が必要である。
強膜化角膜に対する角膜移植の予後は不良である。報告によると1年移植片生存率は37〜70%であり、75%で最終的な不成功が報告されている。主な不成功因子は角膜縁領域の血管新生である。小児例ではさらに予後が厳しく、複数回の再移植を要することがある。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”眼発生と神経堤細胞の役割
Section titled “眼発生と神経堤細胞の役割”正常な前眼部の発生には3つの重要なプロセスが関与する。前脳の神経外胚葉からの形成、水晶体胞の表面外胚葉からの分離、神経堤由来の間葉系前駆細胞の前方への遊走である。
正常発生では胎生4週に水晶体胞の分離後、表層外胚葉が角膜上皮へ分化する。胎生6週には眼杯前縁部付近の神経堤細胞が角膜上皮と水晶体の間に進入し、Bowman層と角膜内皮が形成される。続いてBowman層と角膜内皮の間に再び神経堤細胞が進入し角膜実質が形成される。胎生7週には神経堤細胞から強膜の形成が始まり、前方から後方へ進展して胎生5か月に後極部に達する。
強膜化角膜では胎生7〜10週に角膜縁原基が形成されないため、角膜と強膜の正常な境界が確立されない。この結果、角膜曲率が平坦化し、角膜実質が強膜様の性質を帯びる。
組織学的特徴
Section titled “組織学的特徴”- 上皮:免疫組織化学的にケラチン3・12陽性(角膜上皮マーカー)であり、角膜由来と確認されている。杯細胞は認めない。
- Bowman層:欠損しているか、不規則な硝子様物質の斑を伴う。
- 実質:コラーゲン線維の層構造が無秩序で配列が不規則である。線維径は一定でなく、深層ほど細い(強膜様の特徴)。一方、硫酸ケラタンなどのグリコサミノグリカンやI型コラーゲンの存在から、実質は強膜由来ではなく角膜由来と考えられている。前部・中部実質に上強膜および結膜からの血管侵入がある。
- Descemet膜:欠損または菲薄化(0.8〜1.5μm)を認める。均質な物質と線維芽細胞の増殖を伴う。
- 内皮:一部の症例では内皮の完全欠如が報告されている。
強膜化角膜では角膜実質のコラーゲン線維配列が不規則で層構造が無秩序であるため、角膜の透明性が維持されない。正常角膜では均一なコラーゲン線維の規則的配列が光の干渉を制御し透明性を保つが、強膜化角膜ではこの構造が破綻している。加えて角膜全層にわたる血管侵入も混濁の原因となる。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”強膜化角膜の家系においてRAD21遺伝子変異が同定された。RAD21はコヒーシン複合体の構成要素であり、遺伝子発現の制御に関与する。研究では、RAD21の発現に影響されるプロセスにおいてWNT9Bが神経堤細胞から角膜角化細胞(keratocyte)または強膜実質細胞への分化方向を決定する上で極めて重要な役割を果たすことが発見された。
この知見は、角膜と強膜の実質細胞がいずれも神経堤細胞に由来するにもかかわらず異なる組織特性を持つ理由を解明する手がかりとなる。将来的にはWNT9Bシグナル経路の制御を通じた新たな治療戦略の開発が期待される。
8. 参考文献
Section titled “8. 参考文献”- American Academy of Ophthalmology. Corneal Edema and Opacification Preferred Practice Pattern. Ophthalmology. 2024.
