眼症状
流涙:結膜病変や涙嚢閉塞による。涙嚢病変では血性涙液(bloody tears)を認めることがある1)
結膜炎:結膜の充血と異物感を伴う
羞明:光過敏を呈する
眼瞼腫脹:涙嚢病変では内眼角部の腫脹として現れる。慢性涙嚢炎と誤診されることが多い1)2)

ライノスポリジウム症(rhinosporidiosis)は、内生胞子を形成する微生物 Rhinosporidium seeberi による稀な慢性肉芽腫性感染症である。1900年にブエノスアイレスのGuillermo Seeberが血管に富む鼻ポリープとして初めて報告した。1923年にAshworthがライフサイクルを記述し学名を確立した。
長年その分類は議論されてきたが、リボソームDNAの系統解析により、真菌と魚類寄生体の境界に位置するメソミセトゾア(Mesomycetozoea)に分類されることが判明した3)。人工培地では増殖できず、薬剤感受性試験は現在も確立されていない。
症例の90%以上がインド亜大陸で報告されており、インド、スリランカ、パキスタン、アフリカ、南米の風土病である4)。鼻咽頭が最も一般的に侵され(70%以上)、眼病変は約15%を占める。眼では結膜が69%、涙嚢が24%を占める2)。涙嚢ライノスポリジウム症の文献レビューでは156例が報告されている1)。
ヒトからヒトへの伝染は確認されておらず、伝染性疾患とはみなされない。犬、猫、馬、牛などの動物でも症例が報告されている。
ヒトからヒトへの伝染は確認されていない。R. seeberi の感染は汚染された停滞水や土壌との接触により損傷した上皮を介して起こる。したがって伝染性疾患ではなく、患者の隔離は不要である。
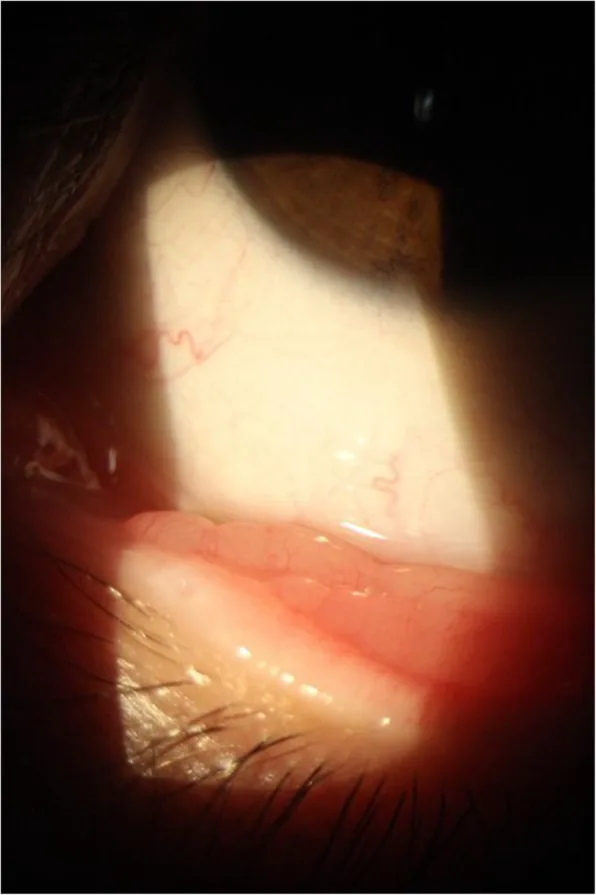
病変の部位により症状は異なる。
眼症状
流涙:結膜病変や涙嚢閉塞による。涙嚢病変では血性涙液(bloody tears)を認めることがある1)
結膜炎:結膜の充血と異物感を伴う
羞明:光過敏を呈する
眼瞼腫脹:涙嚢病変では内眼角部の腫脹として現れる。慢性涙嚢炎と誤診されることが多い1)2)
全身症状(眼外病変)
鼻閉・鼻出血:鼻咽頭病変(70%以上)で最も多い症状である
嗅覚消失:鼻腔内のポリープ増大による
呼吸困難:喉頭・気管・気管支への播種時に生じる。肺虚脱を来す場合がある5)
皮下腫瘤:播種性感染では四肢・体幹に多発性の皮下結節を認める3)
涙嚢ライノスポリジウム症は慢性涙嚢炎と臨床的に類似するため誤診されやすい1)。鑑別にはCTが有用で、涙嚢内の充実性腫瘤と骨浸食の有無を評価する2)。流行地域での涙嚢腫脹、特に血性涙液を伴う場合は本症を疑う。確定診断は組織病理学的検査による。
R. seeberi は停滞水と土壌に存在し、損傷した上皮を介して粘膜に感染する。最も高い発症率は川砂採取作業者で報告されている6)。内生胞子が損傷した上皮に接種されることで感染が成立する。
涙嚢への感染は、鼻腔の病変から鼻涙管を経由して上行性に広がると考えられている2)。ただし弁の存在により鼻涙管経由の伝播を否定する研究者もいる1)。結膜から涙小管を経由する経路や、結膜下結合組織・リンパ管を介した経路も報告されている1)。
確定診断は組織病理学的検査に基づく。切除生検、表面病変の擦過、または細針吸引で組織を採取する。
組織学的所見として、薄い壁に囲まれた複数の成熟段階の胞子嚢(sporangia)が観察される。胞子嚢の直径は50〜1000μmで、内部に約5〜10μmの内生胞子(endospores)を含む。周囲組織には過形成と疎な線維血管性間質を認め、リンパ球、マクロファージ、形質細胞、多形核白血球の浸潤を伴う。
重要な特徴として、感染部位に好酸球がほとんど存在せず、スプレンドレ・ヘップリ現象(Splendore-Hoeppli reaction)を欠く点がある。
涙嚢病変では造影CTを行い、腫瘤の範囲と骨浸食の有無を評価する1)2)。鼻涙管への進展が疑われる場合はCT涙嚢造影(CT-DCG)が推奨される2)。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 化膿性肉芽腫 | 外傷歴、急速増大 |
| 結膜乳頭腫 | ヒト乳頭腫ウイルス |
| コクシジオイデス症 | 胞子嚢が小さい(60μm) |
両者は組織学的に類似し、内生胞子を含む大きな厚壁の胞子嚢として観察される。鑑別にはムチカルミン染色が有用で、R. seeberi は陽性、Coccidioides immitis は陰性である。また R. seeberi の内生胞子は C. immitis より大きく数も多い。
第一選択は外科的切除+電気焼灼である。電気焼灼は出血の最小化と周囲粘膜への内生胞子の散布防止に有用である。内生胞子のこぼれ落ちが再発の原因となるため、完全切除が重要である5)6)。
結膜病変の治療
完全切除+電気焼灼:ポリープの完全切除後に基部を電気焼灼する。内生胞子の散布を防ぐため切除中は周囲組織の汚染に注意する
術後管理:再発監視のための定期的経過観察が必要である。眼ライノスポリジウム症の再発率は鼻咽頭病変より低い
涙嚢病変の治療
涙嚢摘出術(dacryocystectomy):涙嚢全体の完全除去が推奨される1)。術後ダプソン療法が通常推奨される2)
内視鏡的涙嚢鼻腔吻合術(endoscopic DCR):涙嚢内の腫瘤を切除し涙液排泄路を再建する1)2)。外部切開を回避でき瘢痕部への播種リスクが低い
涙嚢のグレーディング:Grade 1(涙嚢+鼻涙管のみ)、Grade 2(鼻・眼を合併)、Grade 3(涙嚢皮膚瘻を合併)に分類し治療法を選択する2)
ダプソン(dapsone)が外科的治療の補助として用いられる。100mg/日を3〜6か月間投与する2)。胞子嚢の成熟を抑制し間質の線維化を促進すると考えられている。
播種性疾患でダプソンが使用できない場合、リポソーマルアムホテリシンB+ケトコナゾール+サイクロセリンの多剤併用療法が有効であったとする報告がある3)。
予後は一般的に良好である。局所的な病変であれば完全切除により治癒が見込める。ただし再発率は部位により異なり、鼻病変で約10%、涙嚢病変で約40%と報告されている2)。播種性感染は稀であるが、骨破壊や脳への波及が生じた場合は致命的となりうる。
ダプソンの主な副作用は溶血性貧血であり、特にG6PD欠損症の患者で重篤化する。投与前にG6PD活性の定量検査が必要である。また稀にダプソン誘発性の自己免疫性溶血性貧血(直接抗グロブリン試験陽性)が報告されている3)。メトヘモグロビン血症も全身麻酔時の合併症として注意を要する2)。
R. seeberi の内生胞子が損傷した上皮を介して組織に接種されると、栄養体(trophocytes)と呼ばれる若年期の胞子嚢へと発達する。栄養体は大きさ10〜100μmで単層の細胞壁を持つ。成長に伴い中間胞子嚢となり、より大きく厚い二重層の壁を形成する。
成熟胞子嚢は約100〜300μmに達し、多数の内生胞子で満たされ周囲を免疫細胞に囲まれる。水分の刺激により胞子嚢が破裂し内生胞子が放出され、感染とライフサイクルが継続する。
感染部位の粘膜で急速に複製が起こり、宿主組織の過形成と局所免疫反応の動員が生じる。肉芽腫が形成され、多葉状の血管に富むポリープ状腫瘤へと発達する。胞子嚢の破裂は巨細胞反応を引き起こすことがある。
R. seeberi は免疫偏向(immune deviation)、局所免疫抑制、免疫グロブリン結合、抗原変異など複数の免疫回避機構を有する5)。Th-1からTh-2への免疫応答のシフトも感染の持続に関与すると考えられている6)。
通常は局所病変にとどまるが、血行性・リンパ行性に播種することがある3)。手術中の不注意な操作による内生胞子のこぼれ落ち(spillage)が、遠隔部位への二次的植え付け(secondary implantation)の原因となる5)。鼻手術後の気管支への播種がこの機序で説明されている5)。
再発の主な原因は手術中の内生胞子のこぼれ落ち(spillage)である。不完全な切除や電気焼灼の不十分さにより、周囲粘膜に内生胞子が散布される。また R. seeberi は複数の免疫回避機構を持ち、宿主の免疫応答を抑制するため感染の制御が困難である5)。再発防止には完全切除、基部の十分な焼灼、術後ダプソンの投与が重要である。
播種性ライノスポリジウム症でダプソンが使用できない症例に対して、リポソーマルアムホテリシンB+ケトコナゾール+サイクロセリンの多剤併用療法が有効であった報告がある3)。各薬剤は R. seeberi に対する抗胞子活性を持ち、治療5か月後に多くの病変が縮小または消失した3)。
涙嚢ライノスポリジウム症に対しては3段階のグレーディングシステムが提案されており、病変の範囲に応じた至適な術式選択に活用されている2)。内視鏡技術の発達により、外部切開を回避した低侵襲手術が可能となり再発率の低下が期待されている1)。
非流行地域(マレーシア、日本など)からの散発例報告が増加しており4)6)、グローバルな疾患認知の向上が求められている。R. seeberi の培養困難性が薬剤開発の障壁となっており、今後の研究課題である。
- Pradhan P, Samal S. Rhinosporidiosis of the lacrimal sac masquerading as chronic dacryocystitis: a rare presentation. Autops Case Rep. 2021;11:e2020214.
- Parida PK, Thangavel S, Raja K, Saxena SK. Lacrimal sac rhinosporidiosis. BMJ Case Rep. 2021;14:e243926.
- Ghosh R, Mondal S, Roy D, Ray A, Mandal A, Benito-León J. A case of primary disseminated rhinosporidiosis and dapsone-induced autoimmune hemolytic anemia: a therapeutic misadventure. IDCases. 2021;24:e01076.
- Ahmad MF, Samri SB, Wan Ahmed WA, Che Jalil NA, Sapiai NA. A rare case of disseminated rhinosporidiosis mimicking tuberculosis. IDCases. 2024;36:e02009.
- Nagi K, Sekar R, Saxena SK, Stephen N. Naso-bronchial rhinosporidiosis. BMJ Case Rep. 2022;15:e247133.
- Bano G, Angral S, Sasanka KSBS, Varshney S, Sarangi PK. A rare case of nasal rhinosporidiosis in the Santhal Pargana region of Jharkhand. Cureus. 2024;16(10):e72674.