黄色ブドウ球菌
現在最多の原因抗原:先進国におけるPKCの主要原因である。慢性眼瞼炎に伴うブドウ球菌蛋白が角結膜で過敏反応を惹起する。マイボーム腺炎や眼瞼縁炎を合併している症例が多い。

フリクテン性角結膜炎(phlyctenular keratoconjunctivitis: PKC)は、外来抗原に対するIV型(遅延型)過敏反応によって生じる角膜または結膜の結節性炎症である。宿主が以前に感作された微生物抗原に再曝露した際に発症する。
1950年代以前は結核菌(Mycobacterium tuberculosis)のツベルクリン蛋白が主要原因であった。結核罹患率の低下に伴い、現在の先進国では黄色ブドウ球菌(Staphylococcus aureus)が最も一般的な原因抗原である。近年ではPropionibacterium acnes(アクネ菌)の重要性も指摘されている。
PKCは主に6か月から16歳の小児に発生し、女性に多く、春に発生率が増加する傾向がある。マイボーム腺炎を合併している症例が多く、マイボーム腺炎の重症度と角結膜炎の重症度が相関する。このため、近年ではマイボーム腺炎角結膜上皮症(meibomitis-related keratoconjunctivitis: MRKC)とも呼ばれる。
Wiriyachaiらは、結核が流行する地域ではPKCと結核の関連が依然として重要であることを報告し、副鼻腔結核に伴うPKCの小児例を記載した2)。抗結核薬の全身投与のみでフリクテン病変が消退した。
小児〜思春期に好発する疾患であり、特に女児に多い。霰粒腫やマイボーム腺炎の既往がある小児では再発しやすい。成人での発症は比較的少ないが、眼瞼炎を背景にした症例は年齢を問わず認められる。
| 分類 | 特徴 |
|---|---|
| 結膜フリクテン | 輪部近傍の白〜黄色結節。表層血管集積 |
| 角膜フリクテン | 結節性浸潤+表層血管侵入(束状角膜炎) |
| 遊走性フリクテン | 角膜表面を横断する進行性病変 |
結膜フリクテンは、角膜輪部近傍の球結膜上に生じる白色〜黄色の結節性隆起病変であり、表層性血管の集積と上皮欠損を伴う。瞼裂部に好発する。結膜病変は軽度〜中等度の眼刺激症状のみのことが多い。
角膜フリクテンは角膜下方周辺部に好発するが、瞼裂部にも生じる。角膜に結節性の細胞浸潤とそれに向かう表層性血管侵入が特徴であり、束状角膜炎(fascicular keratitis)と呼ばれる。重症例では角膜の混濁と菲薄化が生じ、高度の視力低下をきたす。
**遊走性フリクテン(marching phlyctenules)**では、フリクテンが角膜表面を横切って進行する。隆起した先端部とその後方に続く血管束を呈する。
黄色ブドウ球菌
現在最多の原因抗原:先進国におけるPKCの主要原因である。慢性眼瞼炎に伴うブドウ球菌蛋白が角結膜で過敏反応を惹起する。マイボーム腺炎や眼瞼縁炎を合併している症例が多い。
P. acnes(アクネ菌)
近年注目される原因菌:霰粒腫の既往歴がある症例に多い。マイボーム腺炎の合併を高率に認め、マイボーム腺炎角結膜上皮症(MRKC)の原因菌として重要視されている。
結核菌
結核流行地域で重要:ツベルクリン蛋白に対する過敏反応として発症する。結核に関連するフリクテンでは、より重度の羞明を伴う傾向がある2)。肺結核、リンパ節結核、副鼻腔結核との関連が報告されている2)。
その他の原因として、単純ヘルペスウイルス(HSV)、クラミジア、緑色連鎖球菌、Dolosigranulum pigrum、腸内寄生虫(Hymenolepis nana)が報告されている。
Khanらは、単純ヘルペスウイルス-2の既往歴を有する66歳女性で結膜フリクテンから結節性強膜炎に進展した症例を報告した1)。ステロイド点眼単独では改善せず、バラシクロビルの追加で著明に改善したことから、単純ヘルペスウイルス-2がPKCの原因となりうる可能性が示唆された。
PKCは眼酒さ(ocular rosacea)と同様のIV型過敏症を背景に持つ可能性があり、両疾患の関連も指摘されている。
結核菌のツベルクリン蛋白はPKCの代表的な原因抗原の一つである。先進国では黄色ブドウ球菌が主因となっているが、結核が流行する地域では依然として重要な原因である2)。PKCを発症した小児、特に結核流行地域からの渡航者では、胸部X線やQFT検査による結核のスクリーニングが推奨される。結核関連のPKCでは抗結核薬の全身投与が必須である2)。
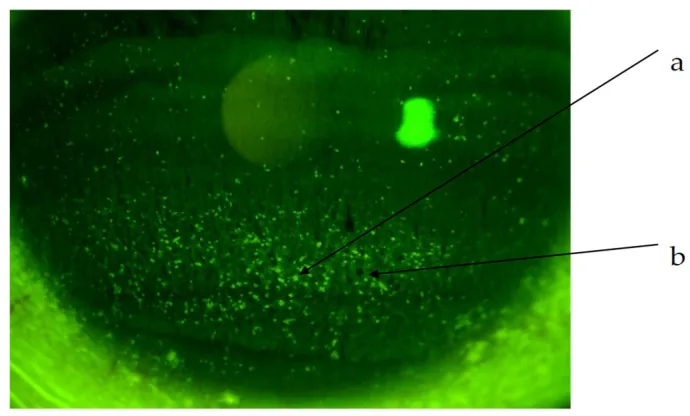
PKCの診断は病歴と特徴的な臨床所見に基づく。角膜輪部近傍の結節性病変と表層性血管集積を認め、マイボーム腺炎の合併があれば診断はほぼ確実である。フルオレセイン染色は結節部位の上皮欠損の検出に有用である。
結核が疑われる場合は、胸部X線検査、ツベルクリン反応検査(PPD)、またはQuantiFERON-TB Gold検査を実施する。Wiriyachaiらの報告では、組織学的・細菌学的検査が陰性であっても、ホルマリン固定パラフィン包埋(FFPE)組織のPCR検査で結核菌が検出された2)。
クラミジアが疑われる場合は結膜スワブの蛍光抗体法またはPCR検査を行う。単純ヘルペスウイルスが疑われる場合はIgG・IgM血清学的検査を行う1)。
| 疾患 | 鑑別のポイント |
|---|---|
| カタル性角膜潰瘍 | 輪部と病変の間に「透明帯」あり |
| 春季カタル | 巨大乳頭、輪部のTrantas斑 |
| 結節性強膜上炎 | 強膜上の結節。充血は限局性 |
その他の鑑別として、酒さ性角膜炎、トラコーマ、感染性角膜潰瘍、周辺部潰瘍性角膜炎、単純ヘルペス角膜炎が挙げられる。カタル性角膜潰瘍はIII型アレルギーが関与し、輪部と病変の間に1〜2 mmの透明帯を認める点でフリクテンと鑑別される。
ステロイド点眼が第一選択である。0.1%フルオロメトロン点眼を1日4回から開始し、症状に応じて漸減する。角膜潰瘍を伴う症例では抗菌薬の併用が推奨される。
再発を繰り返す症例やステロイド依存性となった症例では、シクロスポリンA点眼(0.1%パピロックミニ:適応外)が有効な治療選択肢となる。長期的なステロイド使用に伴う白内障や高眼圧のリスクを回避できる利点がある。
マイボーム腺炎が大きく関与しているため、点眼治療のみならず抗菌薬内服治療の併用が有効である。ドキシサイクリンの内服が補助療法として有益であるが、8歳未満の小児では歯牙着色のリスクからエリスロマイシンが推奨される。
眼瞼衛生として温罨法と眼瞼洗浄を継続し、抗原となる細菌量の減少を図る。1.5%アジスロマイシン点眼が眼酒さを背景とするPKCに有効であるとの報告がある。
結核関連PKCでは抗結核薬の全身投与が必須である2)。Wiriyachaiらの症例では、イソニアジド・リファンピシン・ピラジナミド・エタンブトールの4剤併用で治療を開始し、2か月後にフリクテン病変の著明な改善を認めた2)。ステロイド点眼の併用なしでも改善が得られた。
単純ヘルペスウイルスが原因と考えられる場合はバラシクロビルの全身投与が有効である1)。Khanらの症例では、ステロイド点眼単独ではフリクテンが増大したが、バラシクロビル1 g 1日3回の追加で著明に改善した1)。
結膜フリクテンは1〜2週間で自然消退することもあるが、ステロイド点眼により数日〜1週間で改善する。角膜フリクテンはより長期の治療を要する場合がある。結核関連PKCでは抗結核薬の全身投与に2か月以上を要する2)。マイボーム腺炎を背景とする再発例では、眼瞼衛生と抗菌薬内服を数週間〜数か月継続する必要がある。
PKCの本態は、局所の細菌蛋白に対する遅延型(IV型)アレルギー反応による炎症細胞浸潤である。抗原提示細胞(ランゲルハンス細胞)が微生物抗原を処理し、感作されたヘルパーT細胞に提示する。感作T細胞がサイトカインを放出し、単球やマクロファージを動員して肉芽腫様の結節性病変を形成する。
組織学的には、浸潤部からの擦過検体にはヘルパーT細胞、抑制性/細胞障害性Tリンパ球、単球、ランゲルハンス細胞が認められる。細胞の大部分がHLA-DR陽性であり、細胞性免疫反応の関与を示す。
輪部は血管系、免疫系、神経系が密集する特殊な領域であり、ランゲルハンス細胞やリンパ組織が豊富に存在する。この免疫系の集積がフリクテンが輪部に好発する理由と考えられる。角膜フリクテンでは、結節性浸潤に向かって表層性血管が束状に侵入し、これが束状角膜炎の所見を呈する。
結核菌のツベルクリン蛋白に対する感作が成立した患者では、眼表面での微量の抗原曝露により局所的なIV型反応が惹起される。PKCは結核の活動性とは必ずしも一致せず、ツベルクリン蛋白への過敏性の存在が発症条件となる2)。