眼瞼所見
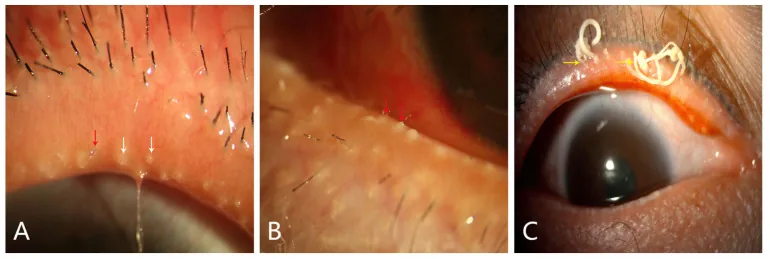
眼瞼縁毛細血管拡張:50〜94%に認める。紅斑を伴う1)。
マイボーム腺機能不全:最大92%に存在。濃縮・混濁したマイバムの分泌。腺開口部の閉塞。
霰粒腫・麦粒腫の反復:マイボーム腺機能不全に続発する。

眼酒皶(ocular rosacea)は、慢性炎症性皮膚疾患である酒皶の眼型(第IV亜型)である1)。毛細血管拡張、眼瞼炎、マイボーム腺機能不全(MGD)、角膜炎を主徴とし、眼表面の慢性炎症を引き起こす。
酒皶の全世界的有病率は約5.5%であり、そのうち眼症状は患者の58〜72%に認められる1)。好発年齢は25〜55歳で、女性がより多く診断される。Fitzpatrick skin type I〜II(色白の肌)に多いが、暗い肌色の人種にも生じる1)。
皮膚所見が先行する例が53%、皮膚と眼の同時発症が27%、眼所見が先行する例が20% に達する1)。そのため、皮膚症状がなくても眼酒皶は発症しうることを認識する必要がある。小児例(pediatric blepharokeratoconjunctivitis)も報告されている1)。
眼所見が皮膚所見に先行する例は全体の約20%に達する1)。顔面紅斑や毛細血管拡張といった典型的な皮膚症状がなくても、慢性の眼瞼炎やマイボーム腺機能不全として現れることがある。眼表面症状が遷延する場合は眼酒皶の可能性を考慮すべきである。
眼酒皶の自覚症状は非特異的であり、ドライアイとの鑑別が必要である1)。
症状は増悪と寛解を繰り返しながら経過とともに進行する傾向がある1)。皮膚症状の重症度と眼症状の重症度は必ずしも相関しない。
眼瞼所見
眼瞼縁毛細血管拡張:50〜94%に認める。紅斑を伴う1)。
マイボーム腺機能不全:最大92%に存在。濃縮・混濁したマイバムの分泌。腺開口部の閉塞。
霰粒腫・麦粒腫の反復:マイボーム腺機能不全に続発する。
結膜・角膜所見
結膜充血:球結膜の発赤。濾胞反応・乳頭反応を伴う1)。
角膜病変:25〜50%に出現。点状表層角膜炎→辺縁浸潤→新生血管→潰瘍→穿孔と進行しうる1)。
角膜瘢痕:遷延する炎症が視軸に及ぶと視力障害の原因となる。
まれな所見
Morbihan症候群:額・鼻・眉間・頬・眼窩周囲の潜行性浮腫。リンパ浮腫を伴う5)。
鼻瘤(rhinophyma):晩期の皮膚所見。皮膚の肥厚・結節・線維化。
マイボーム腺の形態評価には非侵襲的マイボグラフィーが有用である。マイボグラフィーは眼瞼を透過光で観察し、マイボーム腺構造を生体内で形態学的に評価する唯一の方法である。
眼酒皶の正確な原因は不明であるが、免疫異常・血管調節不全・微生物要因・遺伝的素因が複合的に関与する1)。
紫外線への長時間曝露、アルコール・カフェインの摂取、辛い食物や熱い飲み物、精神的ストレス、激しい運動、極端な気温・風への曝露が代表的な増悪因子である。これらは血管拡張や炎症を促進し、症状の再燃を引き起こす。個人ごとに増悪因子が異なるため、生活日誌で自身のトリガーを把握することが推奨される。
眼酒皶は臨床診断であり、特異的な検査基準は存在しない1)。2019年のGlobal ROSacea COnsensus(ROSCO)パネルが包括的な診断アプローチを推奨している1)。
ドライアイ症候群、細菌性/アレルギー性結膜炎、脂漏性眼瞼炎、単純ヘルペス角膜炎、全身性エリテマトーデス、シェーグレン症候群などとの鑑別が必要である1)。眼酒皶は通常の眼瞼炎治療に反応不良な場合に疑うべきである6)。
眼酒皶の治療は重症度に応じた段階的アプローチが推奨される1)。ROSCO国際パネル、全米酒皶協会専門家委員会、スイス治療ガイドラインが治療推奨を提示している。
軽症
眼瞼衛生:非刺激性石鹸による眼瞼洗浄、温罨法、マッサージ1)。
人工涙液:防腐剤入りでも可。
増悪因子の回避:UV対策、食事指導。
オメガ3脂肪酸:EPA 720 mg + DHA 480 mg/日1)。
中等症
アジスロマイシン点眼1〜1.5%:2日間1日2回、または5日間1日1回1)。
シクロスポリン点眼0.05〜0.1%:1日2回。長期使用可1)。
タクロリムス点眼0.03%:1日2回1)。
ステロイド点眼:活動性炎症に短期使用。
重症
経口ドキシサイクリン:初回100 mg 1〜2回/日→維持40 mg/日。12週間1)。
経口アジスロマイシン:500 mg 1日1回×3日、または週1回×3週1)。
全身シクロスポリン:難治例に限る1)。
IPL + MGX:中等症以上で検討。
小児では経口エリスロマイシンまたはメトロニダゾールが使用される1)。
| 薬剤 | 用量 | 備考 |
|---|---|---|
| ドキシサイクリン | 40〜100 mg/日 | 第一選択。RCTで有効性証明1) |
| アジスロマイシン | 500 mg/日×3日 | テトラサイクリン不耐例に |
| ミノサイクリン | 100 mg/日×12週 | ドキシサイクリン代替 |
テルピネン-4-オール(T4O)含有眼瞼ワイプによるDemodex除去が有効である。
Yinら(2021)は、72歳女性の5年間にわたる難治性の酒皶関連眼瞼炎に対し、T4Oワイプを使用した症例を報告した4)。1ヶ月で顔面・眼瞼の紅斑が著明に改善し、2ヶ月で毛細血管拡張が消失した。OSDI スコアは37から15に改善し、8ヶ月の経過観察でDemodexの完全駆除と症状消失が維持された。
Shergillら(2024)の系統的レビューでは、IPL + MGX併用により98例中91%(89例)が部分奏効を示した3)。完全寛解例はなかったが、ドライアイ症状の頻度・重症度、眼瞼縁の発赤が軽減した。3〜4回のセッションを4〜6週間隔で実施するToyosプロトコールが多く用いられている。
角膜瘢痕が視軸に及ぶ場合は深層層状角膜移植術(DALK)が推奨される1)。全層角膜移植は角膜新生血管と慢性炎症のため予後不良となりやすい。角膜穿孔には結膜フラップ、テノン嚢パッチ移植、組織接着剤が用いられる1)。
眼酒皶は慢性疾患であり、完全な治癒は困難である。治療の目標は症状のコントロールと合併症の予防にある。眼瞼衛生の継続と増悪因子の回避により安定した状態を維持できることが多いが、炎症の再燃には適切な薬物療法で対応する必要がある。
眼酒皶の病態は、自然免疫系の過剰活性化、神経血管調節異常、マイボーム腺機能不全が複合的に関与する慢性炎症である1)2)。
角化細胞におけるTLR2の過剰発現が中心的役割を果たす1)2)。TLR2はNF-κBシグナル経路を活性化し、IL-1β、TNF-α、IL-6、IL-8などの炎症性サイトカインの産生を誘導する。同時にセリンプロテアーゼKLK5を介してカテリシジンLL-37の産生が促進される2)。
LL-37は以下の複合作用により慢性炎症を維持する:
眼酒皶患者の涙液中ではIL-1α/β、粘膜類天疱瘡-8、粘膜類天疱瘡-9の濃度が上昇している2)。IL-1αは粘膜類天疱瘡-9の産生・活性化を促進し、眼瞼・眼表面の刺激症状、角膜上皮欠損、角膜潰瘍、角膜新生血管の原因となる2)。涙液クリアランスが低下するほど、これらの炎症因子の濃度は上昇する。
MGDは「マイボーム腺のびまん性の慢性異常で、導管終末部の閉塞および/または腺分泌の質的・量的変化を特徴とする」と定義される。導管上皮の角化亢進とマイバム粘度の上昇により閉塞が生じ、腺の脱落・萎縮・分泌低下を来す2)。脂質層の減少は涙液蒸発を促進し、蒸発型ドライアイを引き起こす。
マイボーム腺機能不全は分泌減少型と分泌増加型に大別され、それぞれ原発性と続発性がある。
Demodex folliculorumおよびD. brevisは皮脂腺に寄生する。酒皶患者では正常皮膚より高密度に存在し、TLR2を活性化して自然免疫応答を亢進させる4)。共生細菌Bacillus oleoniusが産生するスーパー抗原は、IL-8・IL-12p70の産生を介してCD4+ T細胞・マクロファージを活性化し、ランゲルハンス細胞の浸潤を促す4)。Demodexはまた、リパーゼ・エステラーゼの産生を亢進させてマイバムの脂質分解を促進し、マイボーム腺機能不全を悪化させる。
Mohamed-Noriegaら(2025)のレビューでは、免疫調節異常やマイクロバイオーム変化の理解の進展に伴い、生物学的製剤や低分子阻害薬を含む標的治療の探索が進んでいることが報告されている1)。具体的な薬剤名や臨床試験結果はまだ十分に蓄積されていない。
腸内細菌叢の異常(gut dysbiosis)が酒皶の増悪や再燃に関与する可能性が指摘されている1)。腸-眼軸(gut-eye axis)を介した炎症経路の解明は、新たな治療標的の発見につながる可能性がある。
ゲノムワイド関連解析(GWAS)により、HLA-DRA、BTNLA2、HLA-DRB1*03:01などの一塩基多型が酒皶と関連することが報告されている1)。遺伝的素因の解明は個別化治療の基盤となりうる。
抗VEGF点眼または結膜下注射が角膜新生血管の管理に検討されている1)。既存の毛細血管拡張に対するfine-needle diathermyも選択肢として報告されている。