
眼神経障害性疼痛(角膜神経障害性疼痛)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 眼神経障害性疼痛とは
Section titled “1. 眼神経障害性疼痛とは”眼神経障害性疼痛(corneal neuropathic pain: CNP)は、角膜や眼表面の器質的所見に乏しいにもかかわらず持続する慢性疼痛である1)。「pain without stain」「phantom cornea」とも称される。通常は非侵害性の刺激に対して異常な痛覚応答が生じる状態を指す1)。
角膜は体表で最も高い神経密度を有する組織である。1 mm²あたり約7000本の神経終末が存在し、皮膚の300〜600倍に達する。三叉神経第1枝(眼神経)→鼻毛様体神経→長毛様体神経を経由して角膜に分布し、角膜上皮下で密な神経叢(sub-basal nerve plexus)を形成する4)。
角膜の感覚神経線維は機能的に3種類に分類される4):
- ポリモーダル侵害受容器:全体の約70%を占める。機械的・化学的・熱刺激に反応し、CGRP(カルシトニン遺伝子関連ペプチド)を約60%が含有する
- 機械的受容器:約20%。物理的刺激に特化して反応する
- 冷覚受容器:10〜15%。温度変化や涙液蒸発を感知する。TRPM8チャネルを発現する
CNPは発症機序により末梢性と中枢性に大別される1)。末梢性は角膜神経の直接的損傷に起因し、中枢性は脳幹や視床レベルでの神経可塑的変化による。両者が混在する例も多い。
ドライアイは涙液層の不安定化や眼表面の炎症が主体であり、フルオレセイン染色やSchirmer試験で客観的所見を認める。一方、眼神経障害性疼痛は角膜に目立った器質的所見がないにもかかわらず強い疼痛が持続する状態である。ただし両者は併存しうるため、診断と検査方法の項に示すプロパラカインテスト等で鑑別する。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”CNPの自覚症状は多彩であり、通常のドライアイとは質的に異なる1)。
- 灼熱感・刺痛:最も頻度の高い訴え。持続的で、通常の点眼では軽快しにくい
- 光アロディニア(photoallodynia):通常は痛みを感じない光刺激で眼痛が誘発される1)
- 異物感・乾燥感:涙液量が正常でも訴えることがある
- 顔面ジストニア・眼瞼痙攣:疼痛に伴う反射的な筋緊張
- 精神的合併症:不安障害・抑うつ・片頭痛を高頻度に合併する1)
症状は日内変動を示し、風・空調・画面注視などの環境因子で増悪することが多い。
細隙灯顕微鏡検査では角膜に顕著な上皮障害を認めないことが特徴的である(“pain without stain”)。軽度の涙液不安定性を示す場合はあるが、自覚症状の強さと不釣り合いである1)。
生体共焦点顕微鏡(IVCM)では以下の所見が検出される1)2):
- 神経腫(neuroma):損傷した角膜神経の異常な腫大
- 角膜神経密度の低下:sub-basal nerve plexusの減少
- 樹状細胞の増加:慢性的な神経原性炎症を反映する
- 神経線維の蛇行・ビーディング(beading):神経変性の所見3)
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”CNPの原因は末梢神経の直接的損傷と、慢性炎症による二次的な神経障害に大別される。
- 屈折矯正手術:LASIK・PRKなどで角膜フラップ作成時に角膜神経が切断される1)5)。SMILEはLASIKと比べ神経損傷が少ないとされるが、完全に回避はできない5)
- ドライアイ:慢性の眼表面炎症が持続し、角膜神経の感作を引き起こす1)
- ヘルペスウイルス感染:角膜知覚神経を障害し、感染後に神経障害性疼痛へ移行しうる
- 糖尿病:代謝性の末梢神経障害として角膜神経にも影響する
- シェーグレン症候群:神経障害性の過敏状態を生じやすい4)
- 薬剤性角膜障害:BAC(塩化ベンザルコニウム)含有点眼の長期使用による神経毒性
三叉神経痛との鑑別も重要である。三叉神経痛は罹患率が10万人に4〜5人で、高齢女性に多い。カルバマゼピンが有効である点がCNPと異なる。
4. 診断と検査方法
Section titled “4. 診断と検査方法”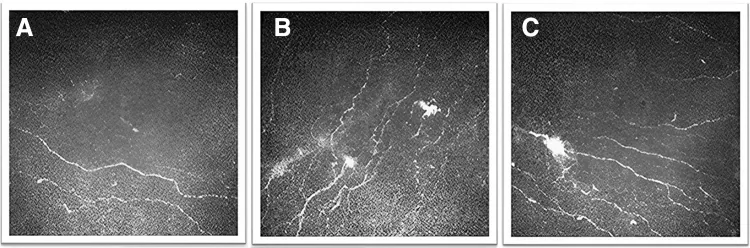
CNPの診断は「器質的所見と不釣り合いな疼痛」の認識から始まる1)。まず細隙灯顕微鏡検査や涙液検査で他の眼表面疾患を除外し、その上で以下の検査を行う。
プロパラカインチャレンジテスト
Section titled “プロパラカインチャレンジテスト”0.5%プロパラカイン点眼後の疼痛変化で末梢性と中枢性を鑑別する1)。
| 疼痛の変化 | 判定 | 意味 |
|---|---|---|
| 完全に消失 | 末梢性 | 角膜神経の異常が主因 |
| 変化なし | 中枢性 | 脳幹・視床の感作が主因 |
| 部分的に軽減 | 混合性 | 両機序の関与 |
生体共焦点顕微鏡(IVCM)
Section titled “生体共焦点顕微鏡(IVCM)”角膜神経叢を細胞レベルで観察できる唯一の非侵襲的検査である1)2)。神経腫・神経密度低下・樹状細胞増加・ビーディングなどの所見をとらえる3)。客観的な診断マーカーとしての活用が進んでいる。
疼痛評価質問票
Section titled “疼痛評価質問票”- OPAS(Ocular Pain Assessment Survey):眼痛の強度・頻度・日常生活への影響を定量化する1)2)
- NPSI-Eye(Neuropathic Pain Symptom Inventory for the Eye):神経障害性疼痛に特化した質問票1)
神経麻痺性角膜症(neurotrophic keratopathy)との鑑別も必要である。Mackie分類ではstage 1(点状表層角膜症)、stage 2(遷延性上皮欠損)、stage 3(角膜潰瘍・穿孔)に分類される。神経麻痺性角膜症は「痛みがない」のに対し、CNPは「所見がないのに痛い」という対照的な病態である。
0.5%プロパラカイン(局所麻酔薬)を点眼し、痛みの変化を評価する簡便な検査である。末梢性の場合は点眼後に痛みが消失し、中枢性の場合は痛みが持続する。結果により治療戦略が異なるため、標準的な治療法に記載する段階的治療の選択に重要な情報を提供する。
5. 標準的な治療法
Section titled “5. 標準的な治療法”CNPの治療は段階的アプローチ(治療ラダー)が推奨される1)。まず局所治療から開始し、効果不十分な場合に全身薬・補助療法・外科的介入へ進む。精神科を含む多職種連携が重要である1)。
局所治療(第1段階)
Section titled “局所治療(第1段階)”- 副腎皮質ステロイド点眼:神経原性炎症を抑制し、樹状細胞密度を低下させる2)。短期間の使用にとどめる
- 自己血清点眼(20%):神経栄養因子(NGF等)を含み、神経再生を促進する3)。治療期間中央値3.8ヶ月で疼痛スコアが9.1から3.1へ改善した報告がある3)
- ラコサミド1%点眼:冷覚過敏神経の興奮を抑制するナトリウムチャネル遮断薬2)。Vimpat 10 mg/mLから調製する院内製剤で、冷蔵保存で14日間安定2)
- 低用量ナルトレキソン(LDN)0.001〜0.2%点眼:TLR(Toll様受容体)を介したオピオイド拮抗作用により抗炎症・鎮痛効果を発揮する2)
全身薬(第2段階)
Section titled “全身薬(第2段階)”局所治療で効果不十分な場合、特に中枢性CNPに対して全身薬を併用する1)。
| 薬剤 | 用量 | 薬効分類 |
|---|---|---|
| ガバペンチン | 100〜900 mg×3回/日 | 抗てんかん薬 |
| プレガバリン | 25〜200 mg×2回/日 | 抗てんかん薬 |
| ノルトリプチリン | 10〜100 mg/日 | 三環系抗うつ薬 |
| デュロキセチン | 20〜60 mg/日 | SNRI |
カルバマゼピン100〜400 mg×2回/日は三叉神経痛に対して有効であり、CNPにも使用される1)。日本では三叉神経痛の第一選択薬として広く用いられている。
補助療法(第3段階)
Section titled “補助療法(第3段階)”- ボツリヌス毒素注射:眼瞼痙攣や顔面ジストニアを伴う例に有用1)
- 経皮的電気神経刺激(TENS):眼痛に対する非侵襲的な疼痛緩和法として報告がある8)
- 神経ブロック:眼窩上神経・滑車上神経ブロックなど1)
外科的治療(第4段階)
Section titled “外科的治療(第4段階)”- 羊膜移植(AMT):眼表面の炎症抑制と神経保護作用1)
- 角膜神経移植(corneal neurotization):直接法(対側の眼窩上神経を移植)と間接法(腓腹神経などの自家神経移植片を用いる)がある7)。感覚回復までに6〜12ヶ月を要する7)
自己血清点眼は患者自身の血液から調製する特殊な点眼薬であり、一般的なクリニックでは対応が難しい場合がある。大学病院や角膜専門の医療機関に相談することが望ましい。詳細は局所治療の項を参照。
個人差が大きく一概にはいえないが、局所治療のみで改善する例では数ヶ月、全身薬を要する例では年単位の治療が必要となることもある。段階的に治療を調整しながら経過を観察することが重要である。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”CNPの病態は末梢感作と中枢感作の2つの機序が重層的に関与する1)。
角膜神経の損傷(手術・感染・炎症など)により神経腫が形成される1)2)。損傷部位では以下のイオンチャネルがアップレギュレーションされる:
- Nav1.7:電位依存性ナトリウムチャネル。異所性発火の閾値を低下させる
- TRPV1:侵害受容に関与するバニロイド受容体。熱刺激・化学刺激への感受性が亢進する
- TRPM8:冷覚受容器に発現するチャネル。涙液蒸発による微小な温度変化で疼痛が誘発される2)
これらの変化により、通常は痛みを生じない微弱な刺激でも異所性発火が生じ、アロディニア(異痛症)が成立する。
神経原性炎症
Section titled “神経原性炎症”損傷した感覚神経終末からCGRPやサブスタンスP(SP)が放出される4)。CGRPは血管拡張、SPは血管透過性亢進を引き起こし、局所の神経原性炎症を惹起する4)。さらに神経切断後には脱神経過敏(denervation supersensitivity)が生じ、残存する神経終末の感受性が異常に高まる4)。
末梢からの持続的な侵害刺激入力により、脳幹三叉神経核や視床のニューロンに可塑的変化が生じる1)。NMDA受容体のアップレギュレーションが主要な分子基盤であり、シナプス伝達効率が長期的に増強される。この段階に至ると、末梢神経の治療のみでは疼痛が改善しにくくなる。
自己血清点眼の作用機序
Section titled “自己血清点眼の作用機序”Anamら(2024)は自己血清点眼の多面的な作用機序を報告した3)。NGF(神経成長因子)を介した神経再生促進に加え、エクソソーム内のmicroRNAによる遺伝子発現調節、TRPV1受容体活性の調整、サブスタンスP濃度の低減が複合的に神経修復に寄与する。20%自己血清点眼3.8ヶ月の治療で、光アロディニアスコアは8.8から1.6に改善し、IVCMでは神経線維密度・長さの増加と神経腫・ビーディングの減少が確認された3)。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”神経成長因子(NGF)製剤
Section titled “神経成長因子(NGF)製剤”rhNGF(cenegermin)はREPARO試験(Phase I/II)において神経栄養性角膜症に対する有効性が示された6)。局所点眼により角膜知覚の回復と上皮修復が促進される。CNPへの応用はまだ研究段階であるが、DHA(ドコサヘキサエン酸)との併用で神経再生がさらに促進される可能性が報告されている6)。
血液由来点眼薬の標準化
Section titled “血液由来点眼薬の標準化”自己血清点眼に加え、臍帯血血小板溶解物(cord blood platelet lysate)や汎網膜光凝固(多血小板血漿)など多様な血液由来製剤の開発が進んでいる3)。しかし調製プロトコールや濃度の標準化が課題であり、大規模な長期比較試験が求められている3)。
IVCMの診断マーカー化
Section titled “IVCMの診断マーカー化”IVCMで検出される神経腫・神経密度低下・樹状細胞増加などの所見を客観的な診断マーカーとして確立する試みが進行中である1)2)。画像解析技術の進歩により、定量的評価の精度向上が期待される。
エンケファリン調節薬
Section titled “エンケファリン調節薬”内因性エンケファリン(内因性オピオイド)の分解を阻害し、局所の鎮痛効果を高める新しいアプローチが研究されている2)。オピオイド受容体を直接刺激するのではなく、内因性の鎮痛機構を増強する点で依存性のリスクが低いと考えられている。
鼻腔内神経刺激
Section titled “鼻腔内神経刺激”鼻腔内に電気刺激装置を挿入し、三叉神経を刺激して涙液分泌と鎮痛効果を誘導する手法が検討されている1)。非侵襲的な治療オプションとして今後の臨床試験結果が注目される。
8. 参考文献
Section titled “8. 参考文献”- Watson SL, Le DTM. Corneal neuropathic pain: a clinical practice narrative review. Eye. 2024;38:2350-2358.
- Nortey J, Atalay E, Aham-Onu PE, et al. Topical therapeutic options in corneal neuropathic pain. Front Pharmacol. 2022;12:769909.
- Anam A, Zayan K, Gallo R, et al. Blood-derived eye drops for the treatment of corneal neuropathic pain. J Ocul Pharmacol Ther. 2024;40(5):281-289.
- Dartt DA. Neural regulation of lacrimal gland secretory processes. In: Corneal sensory innervation and neuropeptides. (nihms126639)
- Craig JP, Willcox MDP, Argüeso P, et al. TFOS DEWS III report: Lifestyle and environment. Ocul Surf. 2023;22:100938.
- Kanu LN, Ciolino JB. Nerve growth factor as an ocular therapy: applications, challenges, and future directions. Semin Ophthalmol. 2021;36(4):224-231.
- Jowett N, Pineda R II. Corneal neurotization: current state of the art. Curr Opin Ophthalmol. 2022;33(4):294-300.
- Jones L, Downie LE, Korb D, et al. TFOS DEWS III management and therapy report. Ocul Surf. 2023;22:100901.
