眼所見
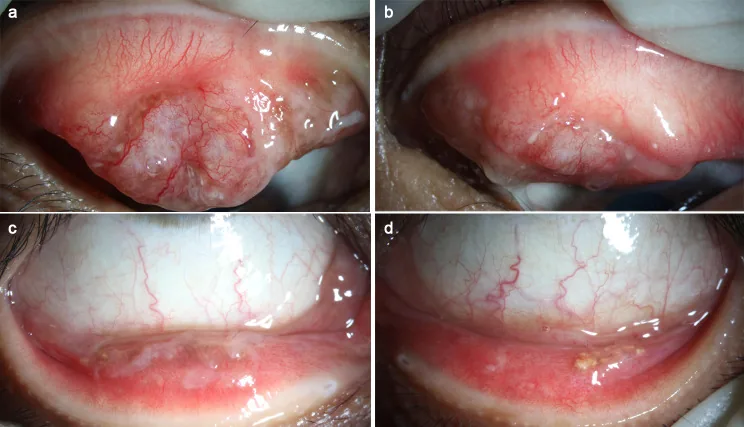
眼瞼結膜の偽膜:上眼瞼に好発する硬くて厚い黄白色の偽膜が認められる。除去しても再発する
両眼性が多い:症例の約50%が両眼性であり、上眼瞼に次いで下眼瞼・眼球結膜に生じる
角膜合併症:長期の炎症により角膜混濁・新生血管・角膜穿孔を引き起こしうる
眼瞼の硬結:偽膜形成に伴い眼瞼が硬くなることがある

木様結膜炎(ligneous conjunctivitis)は、眼瞼結膜上に木のような硬さの線維素性偽膜が慢性的・再発性に形成される極めて稀な結膜炎である。「ligneous(木質の)」という名称はこの偽膜の特徴的な硬さに由来する。
本疾患はI型プラスミノゲン欠乏症(低プラスミノゲン血症)と強く関連する。プラスミノゲンはフィブリン溶解酵素プラスミンの前駆体である。その量的・機能的低下によりフィブリンを溶解できず、偽膜として蓄積する。推定有病率は100万人あたり1.6人とされる2)4)。2001年時点で過去50年間に報告された症例は120例未満であった。
PLG遺伝子の変異が原因であり、常染色体劣性遺伝形式をとる。乳幼児期に発症することが多いが、成人発症例も報告されている1)。歯肉、耳、気道、女性生殖器、腎臓など全身の粘膜に偽膜性病変を伴うことがある。先天性水頭症との合併も複数報告されている2)4)5)。
粘性の眼脂、充血、異物感が初期症状として出現する。流涙を伴うこともある。全身感染症(上気道感染症、耳の感染症など)に先行して、または同時に発症することがある。
眼所見
眼瞼結膜の偽膜:上眼瞼に好発する硬くて厚い黄白色の偽膜が認められる。除去しても再発する
両眼性が多い:症例の約50%が両眼性であり、上眼瞼に次いで下眼瞼・眼球結膜に生じる
角膜合併症:長期の炎症により角膜混濁・新生血管・角膜穿孔を引き起こしうる
眼瞼の硬結:偽膜形成に伴い眼瞼が硬くなることがある
全身所見
歯肉炎・歯肉病変:結膜に次いで2番目に多い病変部位である
気道病変:喉頭・声帯・気管気管支に偽膜が生じうる。気道閉塞は生命を脅かす2)
先天性水頭症:フィブリン沈着による脳室系の閉塞が原因とされる2)4)5)
その他:女性生殖器・腎臓・中耳にも偽膜形成がみられることがある
組織学的には、潰瘍化した結膜の上皮下にフィブリン・免疫グロブリンを含む好酸性のアミロイド様物質が認められる。リンパ球・形質細胞・好中球の浸潤を伴う1)。極めて稀にIgG4陽性の所見を呈し、結膜腫瘤と誤認された報告がある1)。
Liらは41歳女性において両眼の結膜腫瘤として紹介された木様結膜炎の症例を報告した。病理学的にIgG4陽性所見(IgG4+細胞≒100/HPF、IgG4/IgG比>40%)を認め、LCの炎症が免疫異常を惹起しIgG4上昇をもたらした可能性を指摘している。外科的切除+局所ステロイド投与で10か月間再発なく経過した。1)
木様結膜炎は乳幼児に発症することが多いですが、成人や高齢者でも発症することがあります。文献では46歳や70歳で初めて治療を受けた症例も報告されています。幅広い年齢層に生じうる疾患です。
木様結膜炎の主な原因はPLG遺伝子の変異によるI型プラスミノゲン欠乏症である。
プラスミノゲン欠乏症には2つの型がある。I型(低プラスミノゲン血症)ではプラスミノゲンの抗原量と活性の両方が低下する。II型(異常プラスミノゲン血症)では抗原量は正常だが機能活性が低下する3)。木様結膜炎は主にI型に関連する。
診断は臨床所見・組織検査・血液検査・遺伝子検査を組み合わせて行う。
診断基準:
必要な検査:
| 疾患 | 鑑別のポイント |
|---|---|
| ウイルス性結膜炎 | 急性経過、偽膜は薄い |
| クラミジア結膜炎 | 封入体の確認 |
| アミロイドーシス | Congo Red染色陽性 |
このほか、細菌性結膜炎(ジフテリアなど)、Stevens-Johnson症候群、眼類天疱瘡も偽膜性結膜炎をきたしうるが、木様結膜炎は慢性再発性の経過が特徴であり、臨床経過が他の偽膜性結膜炎と異なる。
木様結膜炎に対する根治的治療のコンセンサスは確立されていない。外科的切除と薬物療法の併用が基本である。
薬物療法
ステロイド点眼:炎症抑制の基本治療。長期使用はステロイド緑内障に注意が必要である
シクロスポリン点眼:免疫抑制により偽膜再発を抑制する4)
ヘパリン点眼:フィブリン産生を直接抑制する3)
プラスミノゲン点眼:局所的にフィブリン溶解を促進する。市販されていない地域が多い
全身療法・その他
新鮮凍結血漿(FFP):プラスミノゲンを含む血漿の局所投与・全身投与3)5)
クライオ除去血漿:FFPから凝固因子を除去した血漿。血栓リスクを軽減しつつプラスミノゲンを補充できる4)
Ryplazim:ヒト由来プラスミノゲン製剤。I型PLGD治療薬としてFDA承認済み
偽膜切除術:単独では48時間以内に再形成しうるため、必ず薬物療法と併用する
Almeidaらは偽膜切除+術中結膜下FFP注入+術後局所FFP・ヘパリン点眼のプロトコルで2例ともに12か月間再発なく経過したと報告している3)。
症例1(46歳男性)はプラスミノゲン値4.75 mg/dLであり、過去の切除+自家血清・シクロスポリン・タクロリムスでは再発を繰り返した。FFP+ヘパリンプロトコルにより12か月間再発を認めなかった。症例2(70歳女性)はプラスミノゲン活性43%であり、同プロトコルで同様に再発なく経過した。3)
Bonde Scheel-Bechらは12歳のトルコ人少女(PLG活性<10%)に対し、クライオ除去血漿を週2〜3回静脈内投与+シクロスポリン点眼を行い、7週間で偽膜が消退し、1年後も完全寛解を維持したと報告している4)。
クライオ除去血漿はFFPからクリオプレシピテートを除去した製剤であり、凝固促進因子を欠くため血栓形成リスクが低い一方、プラスミノゲンは正常量を保持している。FFPと比較して大量投与が可能であり、より高い血中プラスミノゲン濃度を達成できる利点がある。4)
偽膜切除単独では再発率が非常に高く、早ければ48時間以内に偽膜が再形成されます。手術による外傷自体がフィブリン沈着を促進するためです。切除は必ずヘパリン点眼や新鮮凍結血漿などの薬物療法と組み合わせて行います。
木様結膜炎の病態はプラスミノゲン-プラスミン系のフィブリン溶解経路の障害に基づく。
正常な創傷治癒過程:組織損傷→フィブリンマトリックスの沈着→肉芽組織形成→プラスミンによるフィブリン分解→コラーゲンリモデリング→治癒。
木様結膜炎の発症機序:
結膜は埃・局所感染・軽微な外傷などの刺激に頻繁にさらされやすい部位であり、特に乳幼児で顕著である。このため結膜が最も罹患しやすい臓器となる。
水頭症の合併は脳室系へのフィブリン沈着による脳脊髄液循環の閉塞が原因とされる2)4)5)。ある症例集では木様結膜炎の小児16例中7例に水頭症が認められた5)。
Alghubaishiらは正期産の男児がPLG遺伝子のホモ接合型変異(c.2095T>C、p.Cys699Arg)を有し、先天性水頭症・木様結膜炎・再発性髄膜炎を合併した症例を報告した。プラスミノゲン値は15%(正常75〜150%)と著明に低下しており、心房内血栓も認められた。集中治療にもかかわらず、1歳前に上気道閉塞で死亡した。2)
はい。プラスミノゲン欠乏症はフィブリン溶解の障害を全身にもたらします。歯肉炎、気道の偽膜形成(気道閉塞のリスク)、女性生殖器の病変、腎障害、先天性水頭症など、多臓器に影響が及ぶことがあります。特に気道病変は生命を脅かす可能性があり、早期診断と多職種連携が重要です。
Ryplazim(ヒト由来プラスミノゲン製剤):I型プラスミノゲン欠乏症に対する初のFDA承認治療薬である。静脈内投与で全身の木様病変を制御できる。推奨用量は体重1kgあたり6.6mgを2〜4日ごとに投与する。ただし入手困難な地域が多く、高価であることが課題である。
クライオ除去血漿の有効性:Bonde Scheel-Bechらは従来のFFPに代わるクライオ除去血漿の長期投与の有効性を報告した4)。凝固因子を除去しつつプラスミノゲンを保持するため、血栓リスクを軽減しながら大量投与が可能である。
FFPベースの治療プロトコル:資源が限られた地域においてFFPは実用的な治療選択肢として注目されている5)。Almeidaらは偽膜切除+FFP+ヘパリンの周術期プロトコルで良好な長期成績を報告した3)。
IgG4関連疾患との関連:LCにおけるIgG4陽性所見の報告はこれまでに2例のみであり、LCの慢性炎症が免疫異常を惹起する可能性が指摘されている1)。両疾患の関連性の解明には更なる症例の蓄積が必要である。
遺伝子治療:PLG遺伝子の根本的治療としての遺伝子治療はまだ研究段階であるが、将来的な治療オプションとして期待される。