前眼部所見
角膜球状突出:角膜全体が球状に前方へ突出する。側面からの観察で著明である。
びまん性菲薄化:角膜周辺部で最も顕著である。周辺角膜厚は330 μm以下まで菲薄化しうる1)。
Descemet膜異常:皺襞・断裂・肥厚を認めることが多い。Descemet膜の自然破裂により急性水腫を生じうる。
前房深度増大:5 mmを超える深い前房を呈することがある1)。

球状角膜(keratoglobus)は、角膜全体がびまん性に菲薄化し球状に前方へ突出する稀な非炎症性角膜拡張症である。角膜径は正常であるが角膜厚が薄く、強膜の菲薄化を伴うことが多い。稀な疾患であり、通常先天性で小児に認められる5)。
先天型と後天型の2つの形態が存在する。先天型は出生時に認められ、Ehlers-Danlos症候群VI型(眼側弯型)、Leber先天黒内障、青色強膜症候群に関連する。後天型は成人期に発症し、角膜辺縁透明変性(pellucid marginal degeneration)や円錐角膜から進展する場合がある。
高度近視と不正乱視を呈し、眼鏡やコンタクトレンズでの矯正が困難であることが多い4)。外力により角膜破裂をきたすことがある。
円錐角膜は角膜中央部〜下方の局所的な菲薄化と突出を特徴とする。一方、球状角膜は角膜全体がびまん性に菲薄化し球状に突出する。円錐角膜ではFleischer輪やVogt線条が認められるが、球状角膜ではこれらは典型的でない。円錐角膜は通常10歳以降に発症するが、球状角膜の先天型は出生時に認められる。円錐角膜では目をこすることがリスク因子であるが、球状角膜ではリスク因子として指定されていない。
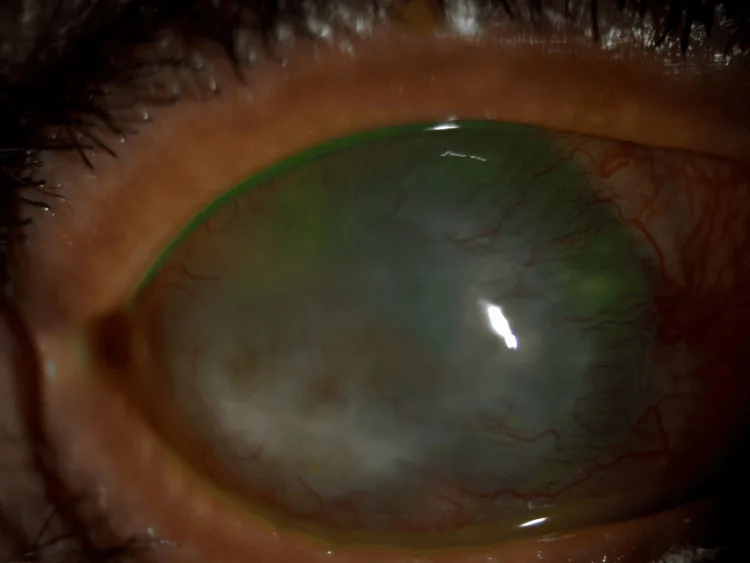
視力低下は高度近視と不正乱視による。眼鏡やコンタクトレンズでは適切な矯正が得られないことが多い3)。急性水腫やDescemet膜の自然破裂が生じた場合、激しい眼痛を伴うことがある。
前眼部所見
角膜球状突出:角膜全体が球状に前方へ突出する。側面からの観察で著明である。
びまん性菲薄化:角膜周辺部で最も顕著である。周辺角膜厚は330 μm以下まで菲薄化しうる1)。
Descemet膜異常:皺襞・断裂・肥厚を認めることが多い。Descemet膜の自然破裂により急性水腫を生じうる。
前房深度増大:5 mmを超える深い前房を呈することがある1)。
鑑別に有用な所見
Fleischer輪・Vogt線条:球状角膜では典型的に認めない。これらは円錐角膜に特徴的な所見である。
角膜曲率:50〜60 Dに達することがある。円錐角膜に比べ全体的に急峻化する。
強膜菲薄化:強膜の菲薄化を伴うことが多く、青色強膜を呈する場合がある。
病因は不明であるが、コラーゲンの合成または分解の欠陥に関連すると考えられている。Ehlers-Danlos症候群・Marfan症候群・骨形成不全症・青色強膜症候群との関連は、コラーゲン異常が病因である可能性を示唆する。
角膜拡張症ではマトリックスメタロプロテイナーゼ(MMP)の増加とその阻害因子(TIMP)の減少が報告されている5)。これらの酵素が角膜実質の分解に関与する可能性がある5)。
円錐角膜とは異なり、目をこすること(eye rubbing)はリスク因子として認められていない。アトピー性疾患との関連も指摘されていない。
Ehlers-Danlos症候群はコラーゲン構造遺伝子の異常により結合組織の脆弱性を生じる疾患群である。皮膚の過伸展・関節の過可動・眼球の脆弱性を特徴とし、眼球破裂のリスクが高い。ダウン症候群では角膜拡張症のリスクが約100倍に上昇すると報告されている4)。
臨床診断は細隙灯顕微鏡検査で行われる。角膜の球状突出と周辺部で最も顕著なびまん性菲薄化が必須所見である。
| 検査法 | 評価項目 |
|---|---|
| 角膜トポグラフィ | びまん性急峻化 |
| パキメトリ | びまん性菲薄化 |
| AS-OCT | 断面構造の評価 |
AS-OCTは角膜・前房・隅角の高解像度断面画像を提供する5)。パキメトリマッピングにより菲薄化の分布を定量的に評価できる5)。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 円錐角膜 | 局所的菲薄化・突出 |
| 角膜辺縁透明変性 | 下方周辺部の菲薄化 |
| 術後拡張症 | 屈折矯正手術の既往 |
円錐角膜では角膜中央〜下方に局所的な菲薄化と突出を認める。角膜辺縁透明変性は角膜下方周辺部が透明なまま帯状に菲薄化する。球状角膜は生下時から両眼に発症し、角膜全体が菲薄化する点で鑑別される。
管理は眼鏡矯正から始まる。ポリカーボネートレンズは粉砕されずに変形するため、角膜保護にも有用である。コンタクトレンズの安全性については議論がある。RGPレンズのフィッティングは慎重に行う必要がある。
球状角膜に対する手術治療にゴールドスタンダードは確立されていない1)。
角膜移植術
従来PK:技術的難易度は低いが、正常厚のグラフトを極薄のレシピエント組織に接合するため術後高度乱視が生じやすい1)。
フェムトセカンドレーザー補助half top hat PK:ドナー角膜のみにtop hat構成を作製する。外径9.5 mm、中央全層ボタン7.1 mmの構成により周辺角膜厚を増大させる1)。最高矯正視力(BCVA)が20/30〜20/40に改善した2例が報告されている1)。
層状角膜移植:構造的支持を提供し輪部幹細胞を温存する5)。びまん性菲薄化例では角膜を平坦化しうるが、著明な皺襞が生じることがある5)。
2段階手術:層状移植の6か月後にPKを行う方法であり、角膜混濁が残存する場合に適応がある。
特殊な手術例
強角膜移植(SKP):広範囲角膜破裂例で前眼部再建に有用である2)。輪部を越えた大径グラフトを使用するため強固な縫合が可能である2)。ただし拒絶率は約70%と高い2)。
SKP+硝子体手術の同時施行:角膜破裂と眼内出血を合併した球状角膜に対し、SKP後に25G硝子体手術を施行した報告がある2)。グラフトを通した眼底透見性は良好であった2)。
修正超音波乳化吸引術:進行した球状角膜で白内障を合併した症例に対し、強膜弁アプローチとトリパンブルー染色+内視鏡照明を用いた手技が報告されている3)。角膜混濁下での視認性向上に有用である3)。
軽度の球状角膜では眼鏡やコンタクトレンズによる矯正で管理できる場合がある。手術の適応となるのは、保存的治療で十分な視力が得られない場合、角膜混濁・瘢痕がある場合、または角膜破裂を繰り返す場合である。手術にはグラフト拒絶・高度乱視・上皮治癒不全などの合併症リスクがあるため、適応は慎重に判断する。
角膜移植後の予後は術式と症例により異なる。フェムトセカンドレーザー補助half top hat PKでは、2例で最高矯正視力が20/30〜20/40に改善し12〜24か月の経過で拒絶や合併症を認めなかったと報告されている1)。一方、SKPでは拒絶率が約70%と高く2)、長期的な免疫抑制が必要である。全体として球状角膜の外科的予後は不良であり、多くの合併症を伴うとされている。
球状角膜の組織学的特徴は、びまん性の角膜実質菲薄化と周辺部で最も顕著なボウマン層の局所的断裂である。菲薄化にもかかわらず実質の層板構造は正常な構成から変化していない。その他の所見として、中央部の上皮増殖、実質の新生血管・瘢痕化、Descemet膜の断裂・肥厚がある。
非炎症性角膜拡張症では、角膜実質内のα1-プロテイナーゼ阻害剤(α1-PI)の低下と転写因子Sp1の上昇が報告されている。球状角膜でも同様の変化が認められ、実質の分解プロセスの変化が角膜菲薄化の根本的原因であると考えられている。
角膜拡張症全般において、粘膜類天疱瘡増加とTIMP減少が報告されている5)。これらの酵素の不均衡が角膜実質の分解に関与する可能性がある5)。炎症性メディエーター(IL-6、TNF-α、粘膜類天疱瘡-9)の涙液中濃度上昇も報告されており、角膜細胞のアポトーシスを誘導しうる5)。このことから、非炎症性と分類されている角膜拡張症にも炎症性要素が関与している可能性がある5)。
球状角膜はアトピー性疾患との関連が認められていない点で、円錐角膜と病態が異なる。コラーゲンの合成または分解の欠陥が根底にあると推定されている。
フェムトセカンドレーザー補助half top hat PKは、ドナー角膜のみにtop hat構成を作製する比較的新しい術式である1)。従来のtop hat PKではドナーとレシピエントの双方を加工するが、本法ではレシピエントの極薄角膜の操作を回避できる1)。2例の報告で最高矯正視力が20/30に改善し、周辺角膜厚の増大と構造的安定性が得られた1)。今後、患者の角膜径に基づいたサイズカスタマイズや長期成績の検証が課題である1)。
角膜破裂と眼内出血を合併した球状角膜に対するSKPと25G硝子体手術の同時施行が報告されている2)。広角観察システムとシャンデリア照明の発達により、角膜移植後のグラフトを通した眼底透見性が向上し、人工角膜やエンドスコープを用いずに硝子体手術が可能となっている2)。
フェムトセカンドレーザー補助half top hat PKは比較的簡便な手技でありながら良好な解剖学的・視覚的転帰を提供する。今後、白内障手術との同時手術や術後長期成績の蓄積が必要とされる。1)
ダウン症候群に合併した球状角膜の小児例(6か月児)に対する角膜クロスリンキングの施行が報告されている4)。球状角膜に対するクロスリンキングの有効性については今後の検討が必要である。