ICKの鑑別診断
パラプロテイン血症性角膜症:両側性で進行性。免疫グロブリン軽鎖の角膜沈着による。血液検査でM蛋白を確認する2)。
角膜ジストロフィ:家族歴を確認する。若年発症が多い。
薬剤性結晶沈着:フルオロキノロン等の局所薬剤歴を確認する。
シスチン症:小児に好発する全身性代謝疾患である。
痛風:尿酸値上昇を伴う全身性疾患である。

感染性結晶状角膜症(infectious crystalline keratopathy:ICK)は、1983年にGorovoyらが全層角膜移植後の角膜グラフト内に非炎症性の細菌定着を認めた症例として初めて報告した2)。角膜実質内に細く枝分かれした結晶様の混濁が出現し、周囲の炎症反応が乏しいことが臨床的特徴である1)。
ICKは角膜移植後の局所免疫抑制療法(ステロイド点眼)使用下で最も多く発症する3)。雪片状または氷晶状の外観を呈し、角膜実質内の縫合糸や手術創近傍に好発する3)。全層角膜移植の増加に伴いICKの症例数も増加した2)。
成人に好発し、多くは片眼性である2)。性別や人種による優位性は認められていない2)。起因菌としてはStreptococcus mitis(viridans群連鎖球菌)が最多であるが、グラム陰性菌、真菌、アカントアメーバによる報告もある1)。
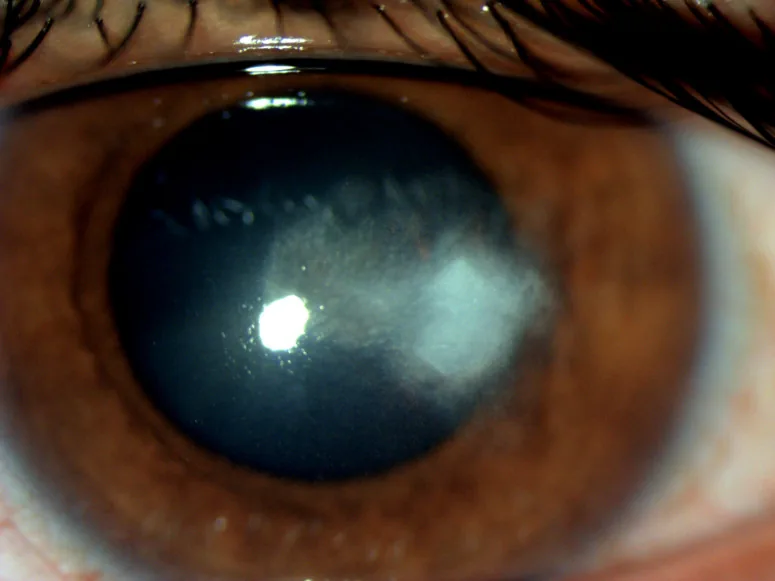
ICKは無症状で経過することがある1)。症状を呈する場合は軽度の視力低下が多い3)。羞明や疼痛を伴うこともあるが、他の感染性角膜炎と比較して軽微である1)。免疫抑制下では局所の炎症が抑制されるため、患者の自覚症状が乏しいまま診断が遅れることがある3)。
細隙灯顕微鏡検査で角膜実質内に枝分かれ状・針状・シダ状の結晶様混濁を認める1)2)。混濁は前部〜中部実質に分布することが多い2)。結膜充血や前房内炎症は軽度ないし欠如しており、この所見が他の感染性角膜炎との重要な鑑別点となる1)。
角膜浮腫や上皮欠損は伴わないか軽微である。前房蓄膿は通常認めない。角膜移植眼ではグラフト・ホスト接合部や縫合糸周囲に病変が生じやすい3)。
ICKの発症には上皮欠損を介した微生物の侵入と、免疫抑制による炎症反応の欠如が関与する1)。
| リスク要因 | 詳細 |
|---|---|
| PK後+ステロイド | 最も典型的な発症状況3) |
| 全身性免疫抑制 | GVHD、Stevens-Johnson症候群1) |
| 神経栄養性角膜 | ヘルペス後、PK後の除神経、LASIK後1) |
免疫抑制がなくとも、神経栄養性角膜疾患(ヘルペス角膜炎後、角膜手術後の除神経、長期点眼麻酔薬使用後)ではICKが発症しうる1)。神経栄養性の状態は角膜創傷治癒を遅延させ、病原体の初期定着の機会を提供する1)。
ICKの起因菌の多くはバイオフィルムを形成する1)。バイオフィルムは抗菌薬の浸透を阻害し、治療抵抗性の主因となる1)。Meislerらの報告では、ICKから培養されたStreptococcus viridansの最小発育阻止濃度は他の状況で同菌種を治療する際の4倍であった1)。
バイオフィルムは細菌が産生する多糖体マトリックスで構成される保護膜である。細菌はバイオフィルム内に包み込まれることで抗菌薬や免疫細胞から保護される。ICKではバイオフィルムが角膜実質内で形成されるため、局所抗菌点眼薬だけでは十分な薬剤濃度が得られず、治療が困難となる。
ICKの診断は特徴的な臨床所見に基づく。枝分かれ状の結晶様混濁と炎症反応の欠如が診断の鍵である1)2)。
角膜擦過培養は実施すべきであるが、表層の擦過では深部の起因菌に到達できず陰性となることが多い1)2)。培養陽性率を高めるには角膜生検が有用である2)。角膜生検は浸潤辺縁部から採取する3)。
共焦点顕微鏡では実質内の高反射性針状構造を描出でき、結晶状角膜症の存在を確認できるが、個々の病原体の特定には不十分である1)。
**前眼部OCT(AS-OCT)**は混濁の深度と範囲の評価に有用であり、鑑別診断にも役立つ2)。AS-OCTにより上皮下・前部実質に限局した高反射病変の分布パターンを評価できる2)。
ICKの鑑別診断
パラプロテイン血症性角膜症:両側性で進行性。免疫グロブリン軽鎖の角膜沈着による。血液検査でM蛋白を確認する2)。
角膜ジストロフィ:家族歴を確認する。若年発症が多い。
薬剤性結晶沈着:フルオロキノロン等の局所薬剤歴を確認する。
シスチン症:小児に好発する全身性代謝疾患である。
痛風:尿酸値上昇を伴う全身性疾患である。
診断のポイント
炎症の欠如:充血・前房内炎症がほとんどないことがICKの最大の特徴である。
既往歴の確認:角膜移植歴、ステロイド使用歴、ヘルペス角膜炎既往が診断の手がかりとなる2)。
両側性の場合:ICKは通常片側性であり、両側性の場合はパラプロテイン血症性角膜症等の非感染性原因を考慮する2)。
培養の限界:表層擦過では陰性のことが多い。角膜生検を検討する1)。
ICKは通常片側性で、角膜移植やステロイド使用の既往がある。パラプロテイン血症性角膜症は両側性に進行し、眼科的既往がないことが多い。AS-OCTによる沈着深度の評価と、血液検査(遊離軽鎖、M蛋白)が鑑別に有用である。ICKの典型的外観であっても、眼科的リスク因子がない場合や両側性の場合は非感染性原因を積極的に検索する必要がある。
初期治療は高濃度広域抗菌点眼薬である。グラム陽性菌をカバーするセファゾリン(50mg/mL)やバンコマイシンに加え、フルオロキノロン系(モキシフロキサシン等)を頻回点眼する4)。起因菌が判明した場合は感受性に基づき治療を調整する3)。
免疫抑制療法の中止または減量が治療の重要な要素である3)。ステロイド点眼を減量するとバイオフィルムに封じ込められていた炎症反応が顕在化し、一時的に症状が悪化することがある3)。
局所治療に抵抗する症例では実質内抗菌薬注射が有効な選択肢となる1)。Khanらはセフロキシムの実質内注射でStreptococcus mitis/parasanguinisによるICKを治療した1)。Martinez-Velazquezらはセフロキシム(1mg/0.1mL)とモキシフロキサシン(0.5mg/0.1mL)の2回の実質内注射により、GVHD患者のICKを治療的PKなしに治療することに成功した1)。
実質内注射は抗菌薬を病原体の存在する深部に高濃度で直接送達し、バイオフィルムによる障壁を克服できる利点がある。注射は結晶状沈着物を囲む円形パターンで行い、針痕を視軸から離すことが推奨される。1)
抗菌薬治療に反応しない場合や重度の角膜瘢痕が残存する場合は治療的全層角膜移植(PK)が必要となる2)3)。
実質内注射は白内障手術時の前房内注射で使用される濃度と同等の薬剤を用いるため、内皮毒性のリスクは低いと考えられている。注入量を制限しDescemet膜剥離を予防すること、針痕を視軸外に配置することが重要である。2年以上の経過観察で内皮機能障害やその他の角膜毒性の徴候は認められなかったと報告されている。
ICKの発症機序は上皮欠損を介した微生物の角膜実質への侵入に始まる1)。微生物は実質のラメラ間隙とケラトサイトの細胞体間の空間を利用して増殖する1)。
免疫抑制状態では炎症反応と免疫細胞の浸潤が抑制される。通常の感染性角膜炎で見られる浮腫や化膿性変化が生じないため、結晶様の外観が形成される1)。この特徴的外観は免疫抑制によって初めて出現するものである1)。
バイオフィルム形成はICKの病態の核心である1)。起因菌はバイオフィルム内で保護され、局所抗菌薬に対する最小発育阻止濃度が通常の4倍以上に上昇する1)。バイオフィルムは実質深部に位置するため、表層からの薬剤浸透が不十分となり治療抵抗性を示す。
ステロイド点眼の長期使用はICKのリスクを高める3)。局所免疫抑制に加え、コルチコステロイドによるコラーゲン合成阻害が角膜の脆弱化にも寄与する可能性がある3)。真菌性角膜炎のリスク因子としてもステロイド点眼は共通して挙げられている4)。
ICKが発症する患者の多くは角膜移植後のステロイド点眼や全身性免疫抑制療法を受けている。これらの免疫抑制が炎症細胞の浸潤と炎症反応を抑制する。また、バイオフィルムが免疫細胞の接近を阻害する。この結果、通常の感染性角膜炎で見られる化膿性変化や浮腫が生じず、特徴的な結晶様混濁が形成される。
実質内抗菌薬注射はICKの新たな治療戦略として注目されている1)。局所点眼に比べ、バイオフィルムで覆われた深部病原体に対して高濃度の薬剤を直接到達させることができる1)。ただし薬剤選択、濃度、注入量に関するガイドラインは未確立であり、今後の臨床試験が必要である1)。
パラプロテイン血症性角膜症は早期にはICKと類似した片側性・上皮下の結晶状沈着として発症しうる。免疫抑制の既往がない結晶状角膜症では、両側性への進展を注視し、血液検査によるM蛋白のスクリーニングが推奨される。2)
AS-OCTによる角膜沈着物の深度・分布評価が鑑別診断に有用であることが報告されている2)。ICKと非感染性結晶状角膜症(パラプロテイン血症性角膜症等)の鑑別において、臨床所見に加えAS-OCTと血液検査を組み合わせた体系的アプローチの構築が今後の課題である2)。
感染性角膜炎の微生物学的診断においては、角膜擦過物のPCR法による迅速同定が実用化されつつある4)。ICKのように培養陰性例が多い病態では、分子生物学的手法の導入が診断精度の向上に寄与する可能性がある。