糸状菌
羽毛状潰瘍(hyphate ulcer):境界不明瞭で毛羽立った灰白色の浸潤を呈する。
隆起性病巣:擦過すると硬い。
衛星病巣:主病巣周囲に小浸潤が散在する。
Endothelial plaque:角膜後面に白色沈着物を形成する。深層へ進展した菌糸に対する免疫反応として生じる。
前房蓄膿:前房内への炎症波及を示す。

真菌性角膜炎は、角膜に真菌が感染して生じる角膜炎の総称である。炎症を伴わず角膜内で真菌が増殖する病態も含めて「角膜真菌症(keratomycosis)」と呼ばれる1)。
真菌は形態学的に糸状菌(filamentous fungi)と酵母様真菌(yeast-like fungi)の2つに分類される1)。両者は臨床像・リスク因子・治療戦略が大きく異なる。
世界的に発生頻度は増加傾向にある。温暖な地域ではフザリウム属やアスペルギルス属などの糸状菌が主要な原因菌であり、温帯地域ではカンジダ属が多い6)。米国では年間発生率が10万人あたり6〜8例と推定されている6)。日本では、アルテルナリア属が糸状菌の中でカンジダ属・フザリウム属に次ぐ第3位の分離頻度を示す4)。
まったくリスク因子のない健常眼に真菌性角膜炎が生じることは稀で、何らかの契機が存在することが多い1)。
真菌性角膜炎は細菌性角膜炎に比べて進行が緩徐で、抗菌薬に反応しないのが特徴である。糸状菌では羽毛状の境界不明瞭な浸潤を呈し、衛星病巣やendothelial plaqueを認めることがある。確定診断には塗抹検鏡や培養による真菌の証明が必要で、治療には抗真菌薬を使用する。
ごく初期には自覚症状が軽微で、わずかな上皮障害のみの場合もある。痛みが比較的軽く経過が緩徐であることが真菌性角膜炎の特徴であり、診断の遅れにつながりやすい1)。
糸状菌と酵母菌では臨床像が大きく異なる。
糸状菌
羽毛状潰瘍(hyphate ulcer):境界不明瞭で毛羽立った灰白色の浸潤を呈する。
隆起性病巣:擦過すると硬い。
衛星病巣:主病巣周囲に小浸潤が散在する。
Endothelial plaque:角膜後面に白色沈着物を形成する。深層へ進展した菌糸に対する免疫反応として生じる。
前房蓄膿:前房内への炎症波及を示す。
酵母菌
限局性膿瘍:境界が比較的明瞭なカラーボタン状の浸潤を呈する。
浅層限局:角膜実質浅層に限局することが多い。
融解傾向:病巣周辺に角膜実質の融解を認める。
細菌性角膜炎との類似:ブドウ球菌感染と臨床的に区別しにくい。
糸状菌は深層へ向かって進行しやすく、デスメ膜を越えて前房内に菌糸が到達することがある。感染が拡大すると最終的に強い融解を生じ、角膜穿孔に至る。一方、アルテルナリア属など低温で増殖しやすい菌種は角膜表面で面状に広がる傾向がある。
糸状菌ではフザリウム属(Fusarium solaniが代表)が最も頻度が高く重症化しやすい。ほかにアスペルギルス属、アルテルナリア属などが角膜感染を起こす。酵母菌ではカンジダ属が圧倒的に多く、Candida albicansが代表的だが、近年はC. parapsilosisによる症例が増加している1)。C. glabrataやC. kruseiはフルコナゾールに感受性が低い1)。
糸状菌と酵母菌に共通するリスク因子としてステロイド点眼の先行使用がある1)。
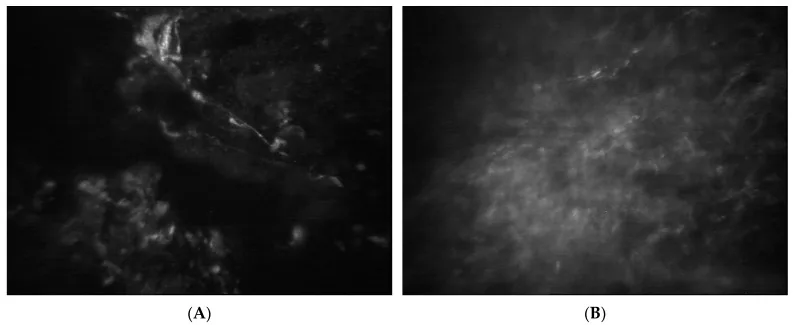
広域抗菌薬に反応しない角膜潰瘍、衛星病巣の存在、大きな潰瘍に対して分泌物が少ないことは、真菌感染を疑うべき重要な所見である1)。
角膜所見から糸状菌感染か酵母菌感染かを臨床的に推定し、患者背景(外傷歴・ステロイド使用歴・コンタクトレンズ装用歴)を鑑別診断の参考とする。
確定診断には病巣部からの真菌の証明が必要である1)。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 細菌性角膜炎 | 急速な進行、膿性分泌物 |
| アカントアメーバ角膜炎 | 放射状角膜神経炎、輪状浸潤 |
| 角膜ヘルペス | 樹枝状病変、再発歴 |
確定診断には角膜病巣部の擦過物から真菌を証明する必要がある。ファンギフローラY染色やGram染色による塗抹検鏡で菌糸を確認し、サブロー培地などで培養する。培養には2〜4週間を要するため、臨床所見から疑われたら培養結果を待たずに治療を開始する。
真菌性角膜炎の治療は抗菌薬に比べて反応が悪く、治療が長期にわたる。日本の感染性角膜炎診療ガイドライン(第3版)では、抗真菌薬の局所投与・全身投与・病巣掻爬を組み合わせた三者併用療法が推奨されている1)。
3系統の抗真菌薬を菌種に応じて使い分ける1)。
ガイドラインでは、酵母様真菌・フザリウム属・フザリウム属以外の糸状菌に分けて治療戦略を立てることが推奨されている1)。
酵母菌(カンジダ属)
第一選択:アゾール系の単独または複数薬の併用。
併用:アゾール系+キャンディン系の併用も推奨される。
注意点:フルコナゾール耐性株の増加に注意する。1%ピマリシン眼軟膏も使用可能だが薬剤毒性に注意する。
糸状菌
第一選択:ポリエン系(ピマリシン)。フザリウム属の頻度を考慮し、当初からピマリシンを加えた処方を考慮する。
フザリウム属以外:ボリコナゾール点眼液が推奨される。特にアスペルギルス属に有効。
抵抗例:ピマリシンで改善がない場合、ボリコナゾール点眼の追加を検討する。
抗真菌薬の全身投与の有効性については明確なエビデンスがない1)。ボリコナゾールは全身投与により前房内へ薬剤が移行する1)。全身投与は副作用が多いため、起炎真菌が同定されターゲットが明確になっていることが望ましい1)。
ガイドラインでは、真菌性角膜炎の治療にボリコナゾール自家調製点眼を条件付きで推奨している(推奨の強さ:弱い推奨、エビデンスの強さ:B)1)。Mycotic Ulcer Treatment Trial(MUTT)で323例を対象にした比較では、5%ピマリシン点眼のほうが1%ボリコナゾール点眼より良好な結果を示した1)。ただしフザリウム属以外の糸状菌では、ボリコナゾール点眼が治療選択肢となる1)。
病巣掻爬は点眼薬の組織移行を高め、菌量を物理的に減少させる効果がある1)。真菌の種類によって薬物療法の効果が異なるため、治療効果を増強させるために積極的に併用すべきである1)。角膜の菲薄化がある場合は穿孔に注意する。アルテルナリア属のような表層型では、表層角膜切除も有効である1)。
真菌性角膜炎の治療は数週間から数か月に及ぶことがある。細菌性角膜炎に比べて薬剤に対する反応が遅く、また点眼薬の角膜深層への移行が不良であるため、長期間の治療継続が必要となる。治療中は定期的な経過観察が不可欠である。
角膜上皮の完全性が外傷や眼表面疾患によって損なわれると、真菌が組織内に侵入して増殖する。角膜上皮に真菌が付着・増殖すると、好中球が病巣に遊走・集簇して白色の浸潤巣を形成する。組織破壊が進行して膿瘍となり、ボウマン膜を越えて潰瘍を形成する。
前房内にも好中球が遊走し、炎症細胞が多数となれば前房蓄膿を形成する。真菌が産生するタンパク質分解酵素、抗原、毒素が角膜内に放出され、壊死と組織構造の損傷が生じる。
糸状菌(特にフザリウム属)は菌糸が角膜深層に向かって進展しやすく、デスメ膜を破って角膜後面で拡大するとendothelial plaqueを形成する。必ずしもデスメ膜を破らなくても、深層に浸潤した糸状菌に対する強い免疫反応としてendothelial plaqueが生じることもある。
酵母菌は糸状菌よりも炎症を伴わない角膜真菌症の形態をとりやすい。境界明瞭な浅層限局性の膿瘍を形成し、融解傾向を示す。
Dongらは、局所抗真菌薬に抵抗性を示す深部角膜真菌感染の2例に対し、前房内アムホテリシンB(10μg/0.1mL)の単回注射を行い、両例とも最終矯正視力20/20を達成したことを報告した2)。局所投与や全身投与では到達困難な角膜深層・前房に直接薬剤を送達できる利点がある。
抗真菌点眼薬は分子量が大きく角膜実質深層への移行が不良であるため、難治性の深層病変に対して薬剤を直接注入する角膜実質内注射が試みられている。
使用される薬剤はボリコナゾール(50μg/0.1mL)およびアムホテリシンB(5〜10μg/0.1mL)であり、手術顕微鏡下に針のベベルを下向きにして病変のない部位から斜めに刺入し、膿瘍周囲5か所に分割注射して薬剤の障壁(バラージ)を形成する手技が報告されている。実質内に注入された薬剤はデポとして貯留し、有効濃度を約7日間維持できるとされる。動物実験ではアムホテリシンBの20μg/0.1mLを超える濃度は角膜浮腫・上皮びらん・新生血管を引き起こすと報告されており、濃度管理に注意が必要である。
Lerらは、深部糸状菌感染(Penicillium属)に対し、ボリコナゾール50μg/0.1mLの実質内注射を病巣周囲に環状に行い、5日間隔で3回繰り返して治療に成功した症例を報告した3)。
ナタマイシンおよびボリコナゾール点眼に反応しなかった25例を対象とした研究では、72%がボリコナゾール実質内注射に反応した。反応しなかった症例の大部分はフザリウム属培養陽性例であった。20例を対象とした別の研究では14例が注射に反応し、平均2.65回の注射を要した。
5%ピマリシン点眼に反応しない真菌性角膜炎40例を対象としたRCTでは、1%ボリコナゾール点眼追加群とボリコナゾール実質内注射追加群を比較した結果、治癒率に有意差はなかったが、3か月後の矯正視力は点眼追加群のほうが良好であった1)。このRCTは症例数が限られるものの、実質内注射の点眼に対する優位性は示されなかった。
実質内注射は点眼・全身投与に対する補助療法であり、単独治療ではない。今後の課題として、最適な注射回数・間隔の確立、菌種別の有効性の検証(特にフザリウム属に対する効果)、他の補助療法(コラーゲン架橋療法など)との併用効果の検討が挙げられる。
Todokoroらは、Mooren潰瘍に合併したアルテルナリア・アルテルナータ角膜炎をDNA配列解析により菌種同定し、薬剤感受性試験でボリコナゾールのMICが0.5μg/mLであることを確認した上で治療に成功した4)。ボリコナゾール点眼とステロイド点眼の併用下で3か月後に視力0.7に回復した。
Chenらは、羊膜移植後10日以内にフザリウム角膜炎およびSistotrema biggsiae角膜炎を発症した2例を報告した5)。Sistotrema biggsiae のヒト感染は文献上初の報告である。羊膜移植後の感染性角膜炎の発症間隔は通常28〜347日とされており、早期発症例への注意喚起がなされた5)。