細隙灯顕微鏡所見
DM line:角膜混濁部位に一致して前房内にデスメ膜剥離の線が確認される
角膜浮腫:局所的またはびまん性の角膜実質・上皮浮腫を呈する
二重前房:広範囲かつ中心性のDMDでは典型的な「二重前房(double anterior chamber)」の外観を呈する
DM皺:デスメ膜の皺(folds)を認めることがある

デスメ膜剥離(Descemet membrane detachment: DMD)は、デスメ膜が角膜実質後面から剥離する病態である。主に眼内手術の合併症として発生し、眼外傷や稀に自然発症もみられる。ICD-10コードはH18.33に分類される。
白内障手術が最も多い発生場面であり、水晶体嚢外摘出術(ECCE)後の発生率は2.5%、PEA後は0.5%と報告される。近年のPEA技術の進歩により臨床的に有意な広範囲DMDの頻度は0.044%に低下している。一方、OCTを用いた詳細な観察では術後1日目に37.1%で微小なDMDが検出されるが、1〜3か月で4.5%に減少し3か月以降は消失する。
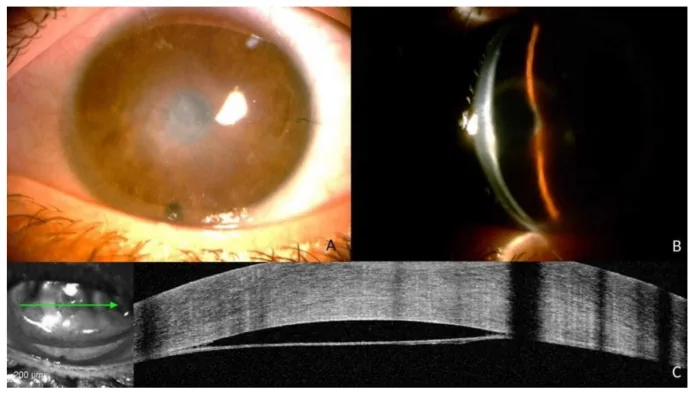
白内障手術後の視力改善不良または突然の視力低下が主訴となる。角膜浮腫に伴う霧視や角膜上皮不整による異物感を訴えることがある。
細隙灯顕微鏡所見
DM line:角膜混濁部位に一致して前房内にデスメ膜剥離の線が確認される
角膜浮腫:局所的またはびまん性の角膜実質・上皮浮腫を呈する
二重前房:広範囲かつ中心性のDMDでは典型的な「二重前房(double anterior chamber)」の外観を呈する
DM皺:デスメ膜の皺(folds)を認めることがある
分類と特徴
限局性DMD:1mm以内の創口周囲の限局的剥離。視機能に影響せず経過観察でよい
広範囲DMD:角膜実質に広範な浮腫を生じ、前房内の視認性が低下する
出血性DMD:シュレム管手術後に血液が剥離腔に流入する型。カナロプラスティ後の1.6〜9.1%に発生する2)
非出血性DMD:粘弾性物質や房水を含む透明な剥離
DMDは通常、デスメ膜の裂け目に沿って房水がデスメ膜前腔に進入することで発生する。
| 手術 | 特徴 |
|---|---|
| 白内障手術 | 最多。切開創への物理的作用 |
| カナロプラスティ | 粘弾性物質の下方蓄積2) |
| Nd:YAG LPI | 衝撃波によるDM亀裂8) |
白内障手術における発生機序: 切れないメスによる切開創の作製、狭い切開創からの手術器具の不用意な出し入れ、OVDやハイドレーション時の灌流液の角膜実質内への誤注入が原因となる。ハイドレーション時にトンネル内方弁近く(デスメ膜近傍)で施行するとDMDのリスクが高い。
DALK術後の白内障手術: DALK後の角膜にはドナー実質とホストのデスメ膜前層との間にcleavage plane(剥離面)が存在する。創口ハイドレーション時にBSSがこの剥離面に到達し、水圧によりDMDが発生しうる7)。
カナロプラスティ: マイクロカテーテル牽引時に注入された粘弾性物質がシュレム管の下方象限に蓄積し、シュワルベ線でのデスメ膜終端部を超える圧力が加わることでDMDが生じる。複合手術(ファコカナロプラスティ)で発生頻度が高い2)。
Nd:YAG レーザー虹彩切開後: 光崩壊による衝撃波がデスメ膜レベルに線状亀裂を生じさせDMDを引き起こしうる。浅前房と偽落屑はリスク因子である8)。
DALKではドナー角膜実質がホストのデスメ膜前層まで置換される。この手術により、ドナー実質とホストのデスメ膜前層の間にcleavage plane(潜在的な剥離面)が形成される。白内障手術時のハイドレーションで灌流液がこの面に達すると、水圧により容易にDMDが生じる7)。このDMDはDALKグラフト内に限局し、ホスト角膜周辺部には及ばないのが特徴である7)。
診断は病歴聴取と細隙灯顕微鏡検査に基づくが、角膜浮腫が著明な場合は画像診断が不可欠である。
AS-OCTに基づくDMD管理の構造化アプローチとしてHELPアルゴリズムが提唱されている5)。Height(高さ)、Extent(範囲)、Length(長さ)、Pupil(瞳孔との位置関係)を評価し治療方針を決定する。
角膜実質浮腫との鑑別が重要である。実質浮腫は健常角膜との境界が不鮮明で不整形であるのに対し、DMDは境界が鮮明で円弧状である。
広範囲DMDでは角膜浮腫により細隙灯顕微鏡での評価が困難となる。AS-OCTは非接触で迅速に角膜の断面像を得ることができ、DMDの正確な位置・高さ・範囲を評価できる4)。HELPアルゴリズムに基づく治療方針の決定にも不可欠であり5)、治療後の再接着確認にも有用である。
限局的な1mm以内のDMDは経過観察でよい。保存的治療では局所ステロイド点眼(炎症抑制・線維化予防)と高張薬点眼(実質脱水)を用いる。自然再接着率は約60%と報告される。
持続性DMDに対するゴールドスタンダードである。前房内に気体を注入し、剥離したデスメ膜を角膜実質後面に再接着させる。再接着成功率は90〜100%であるが、4〜7%の症例で再注入が必要となる。
使用する気体:
手技: 27〜30Gの針で気体を注入する。15〜20分間前房を気体で満たした後、瞳孔ブロック予防に気泡の1/3を排出する。術後は仰臥位を維持する。
巻き上がったDMDに対する新しい手技である1)。まず小さな気泡でDMの巻き上がりを解除(unrolling)し、次に大きな気泡でDMを再接着させる。62歳女性の白内障術後広範囲DMD(巻き上がりあり)に対し、本法で6週後にBCVA 6/9を達成した1)。
descemetopexy後にデスメ膜上腔の残留液を排液するため、DMDの最深部に23G針で角膜部分切開を加える手法である5)。5症例の検討で従来法より早期(1週間以内)の視力回復が得られた5)。1例は再発性DMDにより角膜移植が必要であった5)。
全層角膜移植後45年の遅発性DMDで空気/SF₆によるdescemetopexが奏効しない症例に対し、グラフト-ホスト境界の中心側でDMの部分的descemetorhexisを施行し、牽引を解除することでDMの完全再接着が得られた6)。デスメ膜裂開のない牽引性DMDに対する新しい治療選択肢である6)。
複数回の気体注入にもかかわらず再発を繰り返す症例や水疱性角膜症に至った場合には角膜移植を検討する。全症例の7〜8%で角膜移植が必要となる。DMEK またはDSAEKが選択される。
デスメ膜固定術の合併症
持続性DMD:最も一般的な合併症
眼圧上昇:特にC₃F₈使用時に多い
瞳孔ブロック緑内障:最大13%の症例で報告。下方虹彩切開で予防する
ぶどう膜炎:稀
治療方針の再発時対応
角膜透明化後の再混濁:DMD再発を強く疑い、速やかに気体再注入を行う
複数回再発:空気からSF₆またはC₃F₈への変更を検討する
難治例:デスメ膜縫着術や部分的descemetorhexis6)を考慮する
初回は空気を選択するのが基本である。空気は安全性が高く、角膜内皮へのダメージが少ない。再発した場合はSF₆やC₃F₈を検討する。これらのガスは滞留時間が長く有効であるが、膨張性のため瞳孔ブロックや二次性緑内障のリスクがある。再発例でもガスの長期滞留による角膜内皮障害を考慮し、空気を繰り返す方が安全とする意見もある。
DMDの発生機序はデスメ膜の裂開部位を通じて房水がデスメ膜前腔(pre-descemetic space)に進入することによる。角膜切開時に実質とデスメ膜の間に間隙が形成され、この間隙を通じて灌流液やOVDが侵入する。
デスメ膜は角膜内皮の基底膜であり、前方帯状層(ABL、厚さ約3μm、出生前に形成)と後方非帯状層(PNBL、内皮細胞が生涯にわたり分泌、20歳で約3μm、80歳で約10μm)から構成される。
DALK後の角膜ではドナー実質とホストのデスメ膜前層の間にcleavage planeが存在する7)。白内障手術時のハイドレーションでBSSがこの面に到達すると、水圧によりDMDが発生する。特徴的にDMDはグラフト内に限局し、ホスト角膜周辺部には及ばない7)。
PK後の遅発性DMDでは、移植片-ホスト境界における長年の瘢痕組織のリモデリングと円錐角膜のホスト側進行により、境界の両側で不均衡な牽引力が生じDMDを引き起こす可能性がある6)。この牽引性メカニズムはデスメ膜裂開を伴わず、空気/ガスdescemetopexでは再発を繰り返す6)。
光崩壊による衝撃波と音響圧力波がデスメ膜レベルに線状亀裂を生じさせる8)。浅前房では角膜とプラズマの距離が近いため過剰なエネルギーが角膜内皮に伝達される。偽落屑ではデスメ膜のびまん性・不規則な肥厚と偽落屑物質の蓄積によりDMDへの脆弱性が増加する8)。
DSAEK術中にSheets glideでのレンチクル挿入時に不規則なグライド縁がデスメ膜を引っ掛けDMDを生じうる3)。極めて稀な合併症であるが、早期発見と迅速なdescemetopexが一次グラフト不全の防止に重要である3)。
Köppe MK et al.(2024)は高解像度swept-source OCT(Anterion)を用いてDMDの診断と治療効果判定を行い、71歳男性の白内障術後DMDに対する空気tamponadeの即時成功を確認した。高解像度SS-OCTが臨床的意思決定を導く有用なツールであることを示した4)。
Kundan S et al.(2025)は白内障術後DMD 5症例に対しdescemetopexy(C₃F₈またはSF₆)と角膜ベンティング切開の併用を報告した。4例で1週間以内に良好な視力回復が得られた。デスメ膜上腔の残留液排除が早期のDM再接着に寄与すると考察している5)。
Sharma A et al.(2023)は巻き上がったDMDに対するdouble bubble pneumodescemetopexyを報告した。小気泡でDMの巻き上がりを解除し大気泡で再接着させる制御性の高い手技であり、角膜内皮移植を回避できた1)。
Hasan SM et al.(2021)は全層角膜移植後45年の遅発性DMDに対し、空気およびSF₆によるdescemetopexが失敗した後に部分的descemetorhexisで完全再接着を達成した。牽引性メカニズムを提唱し、牽引解除が治療の鍵であることを示した6)。
- Sharma A, Sharma R, Kulshreshta A, Nirankari VS. Double bubble pneumodescemetopexy for the management of Descemet membrane detachment: An innovative technique. Indian J Ophthalmol. 2023;71(5):2234-2236.
- Orejudo de Rivas M, Martínez Morales J, Pardina Claver E, et al. Descemet’s Membrane Detachment during Phacocanaloplasty: Case Series and In-Depth Literature Review. J Clin Med. 2023;12(17):5461.
- Bevara A, Murthy SI. Iatrogenic Descemet membrane detachment in the donor lenticule during Descemet stripping automated endothelial keratoplasty. BMJ Case Rep. 2023;16(12):e256380.
- Köppe MK, Khoramnia R, Auffarth GU, Augustin VA. Pseudophakic corneal edema caused by Descemet membrane detachment using high-resolution swept-source OCT imaging. GMS Ophthalmol Cases. 2024;14:Doc12.
- Kundan S, Sahu PK, Sharma A, Das GK, Aamir PA. Descemet Membrane Detachment Assessed by Anterior Segment-Optical Coherence Tomography and Managed With Descemetopexy and Corneal Venting Incision: A Case Series. Cureus. 2025;17(6):e86631.
- Hasan SM, Jakob-Girbig J, Pateronis K, Meller D. Partial descemetorhexis for delayed Descemet membrane detachment following penetrating keratoplasty, suggestion of a pathomechanism. Am J Ophthalmol Case Rep. 2021;22:101077.
- Das アカントアメーバ角膜炎, Panigrahi A, Gupta N. Central and bullous Descemet membrane detachment during cataract wound hydration: an insightful complication in a post-DALK eye. BMJ Case Rep. 2022;15(3):e249260.
- Turaga K, Kalary J, Velamala IP. Descemet’s membrane detachment after Nd:YAG laser iridotomy in a patient with pseudoexfoliation. BMJ Case Rep. 2022;15(2):e246071.