軽症(ステージ1〜2)
周辺部無血管域:V字型の無血管領域が耳側周辺部に形成される。最も基本的な所見。
血管直線化・牽引:無血管域との境界付近で血管が直線化し、黄斑方向に牽引される。
刷子様変化(brushing):FA上、無血管域辺縁での網膜血管の刷子状拡張が特徴的。
黄斑偏位:牽引による黄斑の側方偏位。

家族性滲出性硝子体網膜症(Familial Exudative Vitreoretinopathy; FEVR)は、網膜血管の形成不全を本態とする遺伝性硝子体網膜疾患である。1969年にCriswickとSchepensによって初めて報告された。
本疾患では網膜周辺部に無血管域が生じ、そこから新生血管・滲出・網膜牽引・網膜剥離へと進展する。新生児における発生率は0.11%、平均発症年齢は6歳とされる1)。遺伝形式は常染色体優性(AD)が最多で、常染色体劣性(AR)およびX染色体連鎖劣性(XLR)も報告される1)。現在11以上の原因遺伝子が同定されているが、既知変異で説明できる症例は約50%にとどまる1)。
臨床像は患者間でも同一家系内でも非対称的で、無症状の軽症から重篤な視力障害まで多様である1)。
「家族性」とあるが、散発例も存在する。不完全浸透率のため家族内に無症状の変異保因者がいることがあり、必ずしも家族歴が明確でない場合もある。遺伝子検査で変異が同定されれば診断の確度が高まるが、変異が検出されなくてもFEVRを否定できない。
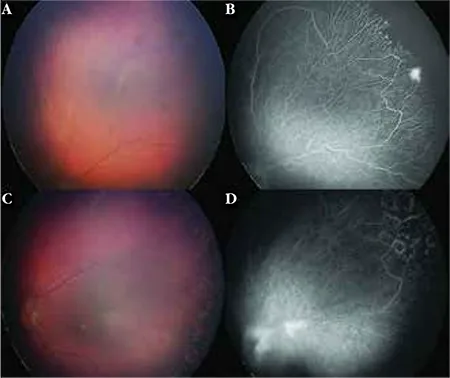
多くの患者は無症状であり、学校健診や家族歴をきっかけに発見されることがある。
FEVRの臨床所見はステージ1〜5に分類される。
軽症(ステージ1〜2)
周辺部無血管域:V字型の無血管領域が耳側周辺部に形成される。最も基本的な所見。
血管直線化・牽引:無血管域との境界付近で血管が直線化し、黄斑方向に牽引される。
刷子様変化(brushing):FA上、無血管域辺縁での網膜血管の刷子状拡張が特徴的。
黄斑偏位:牽引による黄斑の側方偏位。
重症(ステージ3〜5)
網膜ひだ:増殖性変化を伴う網膜ひだの形成。症例の約28%に認められる5)。
新生血管・滲出:虚血網膜からの新生血管形成と脂質滲出。
部分/全網膜剥離:滲出性または牽引性の網膜剥離。症例の21〜64%に認められる5)。
白色瞳孔:ステージ5(全剥離)で認められる最重症の所見。
ステージ分類の詳細を以下に示す。
| ステージ | 所見 | 主な治療方針 |
|---|---|---|
| 1 | 無血管域のみ | 経過観察 |
| 2 | 新生血管・滲出 | レーザー/抗VEGF |
| 3 | 周辺部網膜剥離 | 硝子体手術/バックリング |
| 4 | 黄斑外網膜剥離 | 硝子体手術 |
| 5 | 全網膜剥離 | 硝子体手術 |
FEVRの多くは両眼性だが、片眼性の例も報告されている。Boalら(2021)は片眼性FEVRの症例を報告し、臨床的に非対称な表現型をとりうることを示した5)。家族内でも重症度が大きく異なる場合があり、非常に非対称的な臨床像は本疾患の特徴の一つである。
FEVRの原因となる主な遺伝子を遺伝形式別に示す。
AD/AR(常染色体)
FZD4:Frizzled-4受容体をコードする。Norrin/β-カテニン経路の中心的役割1)。
LRP5:Wnt共受容体。毛細血管成熟に関与3)。
TSPAN12:FEVR患者の5.6〜8.0%1)。細胞外ループ2(ECL-2)に変異の38%が集中1)。
ZNF408・KIF11:その他の原因遺伝子。
XLR(X連鎖劣性)
NDP:Norrinタンパクをコードする。X染色体連鎖劣性FEVRの原因遺伝子。
ノーリー病との関連:NDP変異はノーリー病(失明・難聴・精神遅滞)とも関連し、疾患スペクトラムを形成する。
複数の変異が重なると重症化する。LRP5とTSPAN12の二重変異を持つ症例では、単一変異例より有意に重度の表現型を示すことが報告されている3)。
TSPAN12の新規欠失変異がFEVR患者で同定されており、エクソン欠失がTSPAN12変異全体の一部を構成する可能性が示唆されている1)。
診断できる。既知の変異で説明できる症例は約50%にとどまり、残りは未同定の遺伝子変異が原因と考えられている1)。典型的な臨床所見(周辺部無血管域・V字型FA所見・家族歴)があれば、変異未検出でも臨床診断が可能である。
FEVRの診断には広角蛍光眼底造影(広角FA)が最も重要である。
全ゲノムシーケンシング(WGS)はコピー数変異(CNV)の検出に有用であり、従来のターゲット配列決定では見落とされるエクソン欠失等の検出に優れる1)。
| 検査 | 主な情報 | 特徴 |
|---|---|---|
| 広角FA | 無血管域・漏出 | 診断の主力・全年齢 |
| OCT | 網膜層構造・牽引 | 非侵襲・繰返し可 |
| OCTA | 毛細血管密度・FAZ | FA造影剤不要 |
FEVRは以下の疾患との鑑別が必要である。
必要である。FEVRは不完全浸透率が高く、無症状の家族にも病変が存在することがある。家族歴を持つ者には乳幼児期からのスクリーニングが推奨される。RetCam IIIを用いた新生児スクリーニングプログラムの有用性が報告されている4)。
FEVRの治療は病期(ステージ)に応じて段階的に選択する。
無灌流領域に対するレーザー光凝固が標準的な治療法である4)6)。無血管域を光凝固することで新生血管の退縮と滲出の抑制を図る。
ベバシズマブ・ラニビズマブなどの抗VEGF薬が使用される3)4)。新生血管や滲出に対して有効だが、単独投与では牽引性変化を悪化させるリスクがある点に注意が必要である3)。レーザー光凝固と組み合わせて使用されることが多い。
増殖性変化(増殖膜・牽引性剥離)に対して硝子体手術が行われる3)。ステージ3以上の症例で適応となる。
周辺部裂孔を伴う網膜剥離に対して強膜バックリングが選択される。
必要である。FEVRでは成人後も虚血の進行が報告されている。LRP5とTSPAN12の二重変異を持つ症例では19歳以降も疾患が進行したことが報告されており3)、治療後であっても生涯にわたる定期的な眼科管理が推奨される。
FEVRの病態の中心はNorrin/β-カテニン経路の機能不全にある1)。
正常では、Norrinタンパク(NDPがコード)がFZD4受容体に結合し、LRP5共受容体およびTSPAN12を介してWnt/β-カテニンシグナルを活性化する。このシグナルが網膜血管の形成・成熟に不可欠である1)。
このシグナルが障害されると、網膜周辺部の毛細血管形成が不完全となり、無血管域が形成される。無血管域は虚血をもたらし、VEGFが上昇して新生血管・滲出・牽引が生じる。
FADD(Fas-associated protein with death domain)欠損によるFEVR様病変では、TNFα–FAS–FADD–カスパーゼ経路のアポトーシス下方調節が網膜血管内皮細胞の生存異常と虚血・新生血管形成につながると考えられている7)。
Meerら(2022)はFADD欠損を持つ患者でFEVR様の網膜血管異常を報告した7)。この例はNorrin/FZD4経路とは独立したFEVR類似表現型の存在を示し、病態の多様性を示唆する。
FZD4受容体の特異的アゴニストであるSZN-413が前臨床研究において網膜血管発生の回復を示した4)。Norrin/FZD4経路を直接活性化することで、遺伝子変異の下流にある共通の病態を修正することが期待される。
Yangら(2025)のFZD4変異症例報告でも、FZD4シグナルの増強を目指す治療的アプローチの理論的根拠が論じられている4)。
EMC1がWnt経路の新規調節因子として同定された4)。EMC1はFZD4タンパクの安定性に関与する可能性があり、新たな治療標的となりうる。
WGSはFEVRの遺伝子診断において従来の手法より高感度であり、エクソン欠失などの脈絡膜新生血管を検出できる1)。新規TSPAN12欠失変異の同定や、未解明の遺伝子変異の探索において重要な役割を担う1)。
RetCam IIIを用いた新生児・乳幼児スクリーニングプログラムの有用性が報告されており4)、早期発見・早期治療による予後改善が期待される。