炎症性(VKH)
両側性漿液性剥離:多発性のドーム状隆起が両眼に生じる。
脈絡膜肥厚:OCTで著明な脈絡膜肥厚(約600μm)を認める。2)
乳頭充血・浮腫:視神経乳頭にも炎症性変化を伴う。

滲出性網膜剥離(exudative retinal detachment; ERD)は、網膜裂孔や牽引力を伴わずに網膜下腔に液体が貯留する非裂孔性網膜剥離の一型である。血液網膜関門(blood-retinal barrier; BRB)の破綻により、脈絡膜血管・網膜血管・網膜色素上皮(RPE)から漏出した液体が網膜下に蓄積することで生じる。「漿液性網膜剥離」とほぼ同義に用いられることもあるが、本稿では腫瘍性・炎症性・薬剤性を含む広義の滲出性網膜剥離を対象とする。
裂孔原性網膜剥離との相違を以下に示す。
| 項目 | 滲出性 | 裂孔原性 |
|---|---|---|
| 網膜裂孔 | なし | あり |
| 剥離の形態 | ドーム状・滑らか | ひだ状・不整 |
| Shifting fluid | あり | なし〜乏しい |
| 治療原則 | 原因疾患の治療 | 手術(裂孔封鎖) |
裂孔原性網膜剥離は網膜に穴(裂孔)が開き、硝子体液が流入して生じる。滲出性網膜剥離は裂孔を持たず、血管やRPEの障害によって網膜下に液体が貯留する。前者は手術による裂孔封鎖が原則であるのに対し、後者は原因疾患の治療が基本となる。体位変換で剥離部位が移動する「shifting fluid」は滲出性に特徴的な所見である。
剥離した網膜は滑らかなドーム状隆起を呈し、体位変換によって液体が重力方向に移動する「shifting fluid」が認められる。裂孔原性剥離でみられるような皺襞や不整な隆起は通常生じない。
炎症性(VKH)
両側性漿液性剥離:多発性のドーム状隆起が両眼に生じる。
脈絡膜肥厚:OCTで著明な脈絡膜肥厚(約600μm)を認める。2)
乳頭充血・浮腫:視神経乳頭にも炎症性変化を伴う。
薬剤性(MEKAR)
急性発症の両側性SRD:MEK阻害薬投与後に急速に発症する。4)
症状が軽微なことも多い:視力低下が軽度で自覚症状に乏しい例もある。
可逆性:薬剤中止後3日以内に消退することが多い。4)
妊娠関連
両側性漿液性RD:子癇前症・HELLPに合併することがある。6)
黄斑部優位の剥離:黄斑部に液体が貯留し変視症・視力低下を呈する。
分娩後消退:分娩後に自然消退し、視力は回復することが多い。6)
外傷性・医原性
RPE裂孔後ERD:外傷後RPE裂孔に続発して滲出性剥離が生じる。1)
ROPレーザー後ERD:未熟児網膜症のレーザー治療後に生じることがある。5)
体位変換で液が移動:Shifting fluidが確認できる。
BRBの破綻が最終共通病態であり、その原因は多岐にわたる。
炎症性・免疫性
Vogt-小柳-原田病(VKH):CD4陽性T細胞によるメラノサイト自己免疫反応。HLA-DRB1*0405との関連が知られる。2)
交感性眼炎:貫通外傷後の対側眼への免疫反応。
後部強膜炎・ぶどう膜炎:強膜・脈絡膜の炎症による二次性滲出。
全身疾患・その他
MEK阻害薬(ビニメチニブ等)を含む一部の抗腫瘍薬は、MAPK経路を介してRPEの機能を障害し、滲出性網膜剥離(MEKAR)を引き起こすことがある。4)多くは無症状〜軽症であり、薬剤を中止することで数日以内に消退する。治療継続の可否については担当医と相談が必要である。
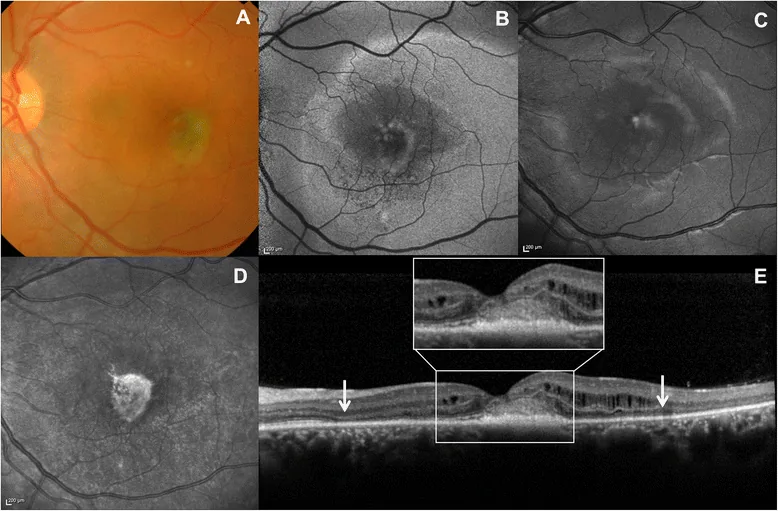
原因疾患の特定と病態の評価に複数のモダリティを組み合わせるマルチモーダルアプローチが重要である。
| 検査 | 主な所見・用途 |
|---|---|
| OCT | 網膜下液の確認、脈絡膜厚計測 |
| 蛍光眼底造影(FA) | 漏出点・新生血管の同定 |
| ICGA | 脈絡膜循環不全・低灌流域の評価 |
| 超音波検査 | 後部強膜炎・脈絡膜腫瘍の鑑別 |
OCTは網膜下液の確認と追跡に欠かせないが、原因疾患の同定にはFA・ICGA・超音波検査を組み合わせたマルチモーダルイメージングが必要なことが多い。2)たとえばVKHではICGAの多発低灌流域がFA所見とともに診断の根拠となる。
治療の基本は原因疾患の特定とその治療である。網膜下液の直接的な排出は通常不要であり、原因が解消されれば液体は自然消退することが多い。
VKHに対するテノン嚢下トリアムシノロン注射(20mg)と経口プレドニゾン(1mg/kg/日)および免疫抑制薬(メトトレキサート; MTX)の組み合わせによって、漿液性網膜剥離が2週間以内に消失したと報告されている。2)
Pengら(2025)はVKH合併片側性脈絡膜剥離の1例において、テノン嚢下TA 20mgとプレドニゾン1mg/kg/日+MTXによる治療を行い、2週間で網膜下液・脈絡膜剥離ともに消失したことを報告した。2)
原因薬の中止が第一選択である。中止後3日以内の迅速な消退が報告されており、多くの場合は特別な眼科的治療を要しない。4)
Sakumuraら(2022)はビニメチニブ(MEK阻害薬)による両側性漿液性網膜剥離の1例を報告した。OCTで両眼に多発する網膜下液を確認したが、ビニメチニブ中止後3日で完全消退した。4)
血圧管理と分娩が最も重要な治療介入である。分娩後に漿液性剥離は自然消退し、視力は通常回復する。6)
Phangら(2022)は子癇前症合併HELLP症候群に両側性漿液性網膜剥離を来した妊婦の1例を報告した。緊急帝王切開および降圧療法後に網膜下液は消退し、視力は発症前の水準に回復した。6)
閾値下マイクロパルスレーザーが有効とされる。
Minowaら(2021)は傾斜乳頭症候群に伴う漿液性網膜剥離5眼に対して閾値下レーザー治療を施行し、5眼中4眼(80%)で網膜下液が消失したことを報告した。3)
外傷後のRPE裂孔に続発した滲出性網膜剥離に対しては、保存的治療(プレドニゾロン点眼など)が施行される。
Panigrahi ら(2023)は外傷後にRPE裂孔と滲出性網膜剥離を来した1例を報告した。プレドニゾロン点眼投与2週間後に自然消退し、視力が回復した。1週間後のOCTでは脱色素化した細胞がRPE裂孔部を充填している像が確認された。1)
Zouら(2022)は未熟児網膜症に対するレーザー治療後に片眼に滲出性網膜剥離を来した症例を報告した。プレドニゾロン点眼の増量(1日4回→8回)により、8週間後に網膜下液は消退した。5)
滲出性網膜剥離の発症には**血液網膜関門(BRB)**の破綻が共通の病態として存在する。
BRBには2つの構成要素がある。
| BRBの種類 | 解剖学的部位 | 障害の例 |
|---|---|---|
| 内側BRB(iBRB) | 網膜血管内皮 | 糖尿病網膜症・放射線網膜症 |
| 外側BRB(oBRB) | RPEの密着結合 | VKH・CSC・薬剤性 |
CD4陽性T細胞がメラノサイト(RPEおよびブドウ膜のメラニン産生細胞)を標的とする自己免疫反応が主病態である。HLA-DRB1*0405との強い遺伝的関連が知られる。2)炎症によりRPEの密着結合(タイトジャンクション)が破壊され(oBRB破綻)、脈絡膜からの漿液が網膜下腔に流入する。
MEK阻害薬はMAPK経路を抑制することでRPEのアクアポリン発現密度に変化を来し、RPEの液体輸送機能を障害する(oBRB破綻)。4)この機序は可逆的であり、薬剤中止後に速やかに機能が回復する。
子癇前症では胎盤由来の因子(抗VEGF抗体様物質など)が全身の血管攣縮を引き起こす。脈絡膜の動脈攣縮により脈絡膜虚血が生じ、RPEのポンプ機能が障害されてoBRBが破綻する。6)
強膜の肥厚と脈絡膜の菲薄化が局所的な脈絡膜循環異常を招く。この異常循環がRPEの液体輸送能を低下させ、慢性的な漿液性剥離を引き起こすと考えられている。3)
打撲等の物理的外力によりRPEが断裂し、局所のoBRBが急性に破綻する。RPE裂孔後1週間以内に脱色素化した細胞が裂孔部を充填・修復し始め、自然消退に至ることがある。1)
BRBは血液と網膜組織の間の物質交換を制御するバリア機構である。網膜血管内皮細胞の密着結合からなる内側BRB(iBRB)と、RPEの密着結合からなる外側BRB(oBRB)の2層構造を持つ。oBRBの破綻が滲出性網膜剥離の多くに共通する病態である。
傾斜乳頭症候群(TDS)に伴う慢性漿液性網膜剥離に対して、閾値下(subthreshold)レーザーの有効性が症例レベルで報告されている。3)光凝固瘢痕を残さず、RPE機能を温存しながら液体の吸収を促す可能性が示唆されているが、対照試験による検証はまだ十分ではない。
MEK阻害薬による眼副作用(MEKAR)と抗腫瘍効果との相関については、現時点で十分なデータが存在しない。4)薬剤継続と視機能温保のバランスをどのように設定すべきかは今後の重要な研究課題である。
OCTアンギオグラフィー(OCTA)とICGAの組み合わせにより、脈絡膜毛細血管板の血流変化をより詳細に評価できるようになっている。2)これにより滲出性網膜剥離の原因疾患の病態解明と治療効果判定の精度向上が期待されている。