定義
OCT上の診断基準:後部ぶどう腫底面のRPE外面接線から50μm以上の内方突出
初報告:2008年、Gaucherらによって初めて記載

ドーム状黄斑(Dome-Shaped Macula; DSM)は、強度近視および後部ぶどう腫(ぶどう腫内の陥凹変形)を背景に、黄斑部が後部眼壁に対して前方(硝子体側)へ凸状に隆起する形態異常である。2008年にGaucherらによって初めて報告された1)。
OCT(光干渉断層計)画像において、後部ぶどう腫底面のRPE(網膜色素上皮)外面接線から50μm以上内方に突出した黄斑の隆起として定義される1)。病院ベースの強度近視眼における有病率は10.7〜12%と報告されている1)。
片眼性DSMは遠視や正視眼でも認められることがあり、軽度近視や非近視眼における報告も存在する。
定義
OCT上の診断基準:後部ぶどう腫底面のRPE外面接線から50μm以上の内方突出
初報告:2008年、Gaucherらによって初めて記載
有病率
強度近視眼(病院ベース):10.7〜12%
近視以外での発生:遠視・正視眼でも片眼性DSMが報告されている
形態の多様性
水平卵円形:最多(62%)
中央円形:21%
垂直卵円形:17%
DSMは3つの形態学的タイプに分類される。
| 形態 | 特徴 | 頻度 |
|---|---|---|
| 水平卵円形ドーム | 黄斑を水平方向に広く覆う | 62%(最多) |
| 中央円形ドーム | 黄斑中央部に集中した隆起 | 21% |
| 垂直卵円形ドーム | 垂直方向に長い形態 | 17% |
主なOCT所見は以下の通りである。
蛍光眼底造影(FA)ではピンポイントの漏出、インドシアニングリーン蛍光造影(ICGA)では局所的な点状過蛍光が認められることがある。
Takahashiら(2023)は84歳女性(右眼軸長27.41mm、左眼28.17mm)の両眼にridge-shaped DSMを確認した症例を報告している。右眼では強膜が内層と外層に分裂し内層のみが前方へ突出し、左眼では中心窩強膜の均一な肥厚が観察された1)。
合併症がなければ無症状で経過することが多い。SRFやCNVを伴わないDSMはOCT検査で偶然発見されることも多く、視力は比較的保たれる。自覚症状の有無にかかわらず、強度近視の方は定期的な眼科受診が重要である。
強度近視(高度近視)が最大のリスク要因であり、眼軸長の延長(26.5mm以上)が後壁の伸展と後部ぶどう腫形成を引き起こす2)。高齢も関連因子として挙げられる。
DSMの正確な病因は解明されていない。以下の機序が提唱されている。
以下に主な病因仮説を示す。
| 仮説 | 提唱者・根拠 |
|---|---|
| 中心窩下強膜の局所的肥厚 | Imamuraら、EDI-OCTによる観察 |
| 強膜内血管による強膜分裂 | Takahashiら(2023)1) |
| ブルッフ膜欠損による強膜張力低下 | Takahashiら(2023)1) |
| 脈絡膜の局所的肥厚 | 複数の観察研究 |
| 後部眼壁の虚脱・硝子体黄斑牽引 | 形態的特徴から推察 |
強膜内血管(短後毛様体動脈・長後毛様体動脈・黄斑渦静脈の分枝)がDSMの形成・形態に関与する可能性がある1)。また、DSMが長い眼軸長による中心窩への牽引損傷を防ぐ保護的役割を果たす可能性も議論されている。
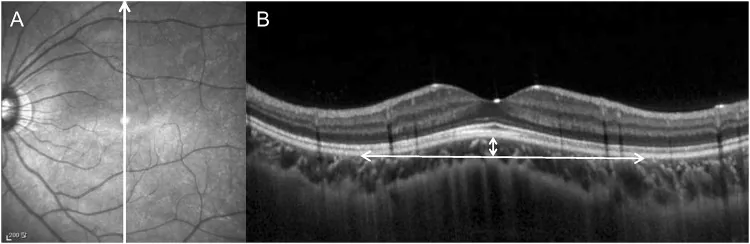
OCTがDSMの診断に必須の検査である。放射状スキャン(radial scanning)が推奨され、垂直・水平の両方向で断面を取得することで形態の評価精度が向上する。
主な検査・診断法は以下の通りである。
鑑別診断として以下の疾患を考慮する。
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 中心性漿液性脈絡網膜症(CSC) | 後部ぶどう腫の有無、黄斑形態 |
| 脈絡膜血管腫・無色素性メラノーマ | 隆起性病変の性状・エコー所見 |
| 両眼性びまん性ぶどう膜メラノサイト増殖症(BDUMP) | 全身検索・両眼性 |
| ぶどう膜滲出症候群 | 周辺部滲出性網膜剥離の合併 |
| 後部強膜炎 | 疼痛・炎症所見・エコー |
OCT(特に放射状スキャン)が診断に必須である。EDI-OCTで強膜肥厚の評価、swept-source OCTで強膜内血管の詳細観察が可能となる。FA・ICGAはCNV活動性やSRF漏出の評価に用いる補助的検査である。
確立された効果的治療法は現在のところ存在しない。SRF(漿液性網膜下液)の減少と視力維持が管理の主な目標となる。
経過観察
適応:無症状・SRFが少量・視力良好な症例
経過:SRFは消失と再発を繰り返すことが多く、定期的なOCTフォローアップが必要
抗VEGF治療
その他の治療
光線力学的療法(光動力学療法):有効性は結果が分かれ、確立されていない
MRA(ミネラルコルチコイド受容体拮抗薬):漿液性中心窩剥離が消失した限定的報告あり
硝子体手術:網膜下剥離の一時的消失が報告されているが、標準的ではない
56眼を対象とした研究では、ベバシズマブ・ラニビズマブ・光線力学的療法のいずれも、BCVA有意改善やSRFの完全消失は得られなかったことが報告されている。
現時点では確立された治療法はない。SRFを伴わない軽症・無症状例では経過観察が基本となる。アフリベルセプトが有望な選択肢として注目されているが、エビデンスはまだ限られている。CNVを合併した場合は抗VEGF治療が必須となる。
DSMの主たる形成機序として、中心窩下強膜の局所的肥厚が提唱されている(ImamuraらのEDI-OCT研究による)1)。しかしこの肥厚がなぜ生じるかは未解明である1)。
Takahashiら(2023)の報告では、強膜が強膜内血管によって内層と外層に分裂し、内層のみが前方へ突出する一方、外層は正常位置に留まる特異な形態が観察された1)。関与する血管は短後毛様体動脈(SPCAs)、長後毛様体動脈(LPCAs)、黄斑渦静脈の分枝であり、これらの血管断面周囲では強膜線維が外方に押されて菱形に変形する1)。
また、黄斑周囲に存在するブルッフ膜欠損が強膜の張力を局所的に低下させ、DSM形成に寄与する可能性が示唆されている1)。穿通血管はCNV(近視性脈絡膜新生血管)周囲に多く認められ、CNVの発生に関与する可能性もある1)。
SRFの発生機序としては以下が考えられている。
DSMが中心窩への牽引損傷を防ぎ、牽引力を周辺部に分散させる保護的役割を果たすという仮説も提唱されている。
眼軸延長により後部眼壁が前後方向に伸展し、後部ぶどう腫が形成される。この過程で中心窩強膜に局所的肥厚が生じ、DSMが形成されると考えられている。ブルッフ膜欠損による強膜張力の低下や、強膜内血管による強膜分裂も関与する可能性がある1)。
Carlàら(2025)は欧州コホートを15年間追跡した研究で、DSM 220眼のうち37%が近視性黄斑症(MNM)を発症したことを報告した(OR 4.95、95%CI 3.50-6.97、P<0.0001)2)。DSMなし眼ではMNM発症率は11%にとどまった。
同研究では、DSMとラッカー亀裂が新生血管合併症と有意に相関することが示された2)。一方、DSM自体はMNM発症後の視力予後悪化とは相関しなかった2)。近視性黄斑症は57%の症例で10年超の経過にわたり進行し、活動性近視性CNV(N2a期)は190眼(15%)に発症し、平均4.5±1.8年後に確認された2)。
Takahashiら(2023)は、swept-source OCTおよびEDI-OCTを用いてDSMの強膜が二層に分裂するという特異な形態を初めて詳細に報告した1)。強膜内を走行する血管が強膜の分裂に関与することが示唆され、DSM形成における強膜血管の役割に注目が集まっている。
DSMの長期予後に関する研究から、以下が重要な予後予測因子として示唆されている。
BCVAは数年間安定することも多いが、長期的には37%がMNMを発症するとの報告があり、DSMなし眼(11%)と比較してリスクが高い2)。ドーム高が400μmを超える場合は予後不良因子となる。定期的な眼科フォローアップが重要である。