非増殖糖尿病網膜症(NPDR)
軽症非増殖糖尿病網膜症:毛細血管瘤(微小動脈瘤)のみ認める。
中等症非増殖糖尿病網膜症:点状・火炎状出血、硬性白斑、軟性白斑(綿花様白斑)を伴う。重症基準は満たさない。
重症非増殖糖尿病網膜症(4-2-1ルール):①4象限すべての網膜内出血、②2象限以上の静脈数珠状拡張、③1象限以上の網膜内血管異常(IRMA)のいずれか一つを満たす。

糖尿病網膜症(Diabetic Retinopathy; DR)は、糖尿病による網膜血管障害を原因とする疾患である。就労年齢層における予防可能な失明の主要原因の一つであり、早期発見・早期介入によって視力喪失を防ぐことができる。
疫学規模は大きい。米国成人糖尿病患者の約28.5%(420万人)にDRが認められ、視力喪失を伴う重篤なDR(VTDR: Vision-Threatening DR)は4.4%に達する1)。世界全体では糖尿病患者の34.6%(約9300万人)がDRを有し、VTDRは10.2%(約2854万人)である1)。糖尿病黄斑浮腫(CSME)は世界で約1883万人に認められる1)。
スクリーニングの目的は、眼科的治療を要する患者を適切に紹介することにある1)。治療対象となる段階を見逃さないために、定期的かつ系統的なスクリーニングプログラムが不可欠である。
しかし実態として、米国では推奨スクリーニングを受診している患者は60%にすぎない1)。43〜65%の患者が散瞳眼底検査を受けていないとされ1)、受診率の向上が依然として大きな課題である。
1型糖尿病では診断後5年以内(思春期前発症の場合は初経または12歳時)に、2型糖尿病では診断時に眼科受診を行う1)。妊娠合併の場合は第1三半期の早期に受診する。診断直後からの定期受診が視力喪失予防の基本である。
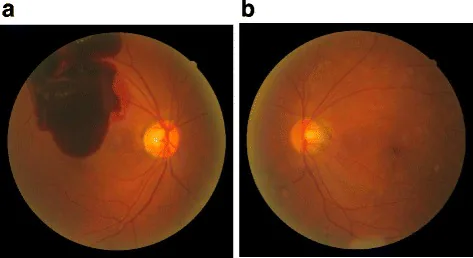
DRの初期は無症状であることが多い。これがスクリーニングが特に重要な理由である。
DR病期は国際基準に基づき分類される。病期による治療方針・フォローアップ間隔が異なる。
非増殖糖尿病網膜症(NPDR)
軽症非増殖糖尿病網膜症:毛細血管瘤(微小動脈瘤)のみ認める。
中等症非増殖糖尿病網膜症:点状・火炎状出血、硬性白斑、軟性白斑(綿花様白斑)を伴う。重症基準は満たさない。
重症非増殖糖尿病網膜症(4-2-1ルール):①4象限すべての網膜内出血、②2象限以上の静脈数珠状拡張、③1象限以上の網膜内血管異常(IRMA)のいずれか一つを満たす。
増殖DR(PDR)・糖尿病黄斑浮腫
増殖DR(PDR):新生血管形成(NVD/NVE)、硝子体出血、牽引性網膜剥離を認める。視力喪失リスクが高い。
糖尿病黄斑浮腫(DME):黄斑部の網膜肥厚。OCTで膨化型・嚢胞様・漿液性剥離型の3型に分類される。いずれのDR病期にも合併しうる。
DRの根本的な原因は慢性高血糖による網膜血管障害である。罹患期間の延長が最大のリスク要因とされる。1型糖尿病では罹患5年後に約25%、15年後に約80%がDRを発症するとされる。
主なリスク要因は以下の通りである1)。
血糖・血圧・脂質の最適化は網膜症の発症・進行を大幅に遅らせることができる1)。ただし長期罹患者では管理が良好でもDRが進行することがあるため、定期的な眼底検査は欠かせない。
初回スクリーニングの推奨時期は糖尿病の型と病状によって異なる1)。
初回診察では以下の検査を行う1)。
DR病期に応じた推奨フォローアップ間隔を以下に示す。
DR病期別の推奨受診間隔(ICO/ADA 2018準拠)は以下の通りである。
| DR病期 | 推奨間隔 |
|---|---|
| DR無し | 1〜2年ごと |
| 軽症非増殖糖尿病網膜症 | 6〜12ヶ月ごと |
| 中等症非増殖糖尿病網膜症 | 3〜6ヶ月ごと |
| 重症非増殖糖尿病網膜症 | 3ヶ月未満 |
| PDR | 1ヶ月未満 |
網膜症が検出されなかった場合でも、1〜2年ごとの定期検査が推奨される。糖尿病の罹患期間が延びるほどDR発症リスクは高まるため、無症状であっても継続的な受診が必要である。
スクリーニングで異常が発見された場合、病期に応じた治療・管理を行う。
DR進行抑制において最も重要な介入は全身管理の最適化である1)。
黄斑浮腫の治療選択は病態に応じて決定する。
糖尿病網膜症スクリーニングには従来の散瞳眼底検査に加え、さまざまな技術が活用されている。各手法の特性を把握することで、患者背景に応じた最適なスクリーニング戦略を選択できる。
代表的なスクリーニング技術の感度・特異度を以下に示す。
| 技術 | 感度 | 特異度 |
|---|---|---|
| テレレチナ | 78〜98% | 86〜90% |
| UWF眼底撮影 | 約94% | 高い |
| AI(従来型) | 87.0〜95.2% | 49.6〜68.8% |
テレレチナ
遠隔眼底読影システム:眼底写真を遠隔地の専門医が読影する方式。
感度78〜98%、特異度86〜90%:眼科専門医への物理的アクセスが困難な地域での有効性が実証されている。
費用対効果:スクリーニングプログラム実施により患者1人の生涯コストが127ドル節約されると試算されている。
超広角眼底撮影(UWF)
200度の広視野撮影:従来の標準眼底写真では見えない周辺部網膜まで一度に撮影できる。
感度約94%:周辺部の出血・新生血管検出に優れる。
散瞳不要(機種による):患者負担を軽減し、スクリーニングの受け入れやすさを向上させる。
AIスクリーニング
自律型AI(IDx-DR):2018年にFDAが承認した初の自律型AI眼底診断システム。
感度87.0〜95.2%、特異度49.6〜68.8%:医師なしで診断結果を提示できる点が画期的。
ディープラーニング改良後:感度96.8%・特異度87%への向上が報告されている。
スクリーニング受診率の向上は重要な公衆衛生課題である。
AIを用いたDRスクリーニングの研究が急速に進展している。
IDx-DRは2018年に米国FDAが承認した初の自律型AIスクリーニングシステムである。医師の解釈を介さずに診断結果を提示できる点で、一次医療現場での活用が期待されている。ディープラーニング技術の改良により、感度96.8%・特異度87%という従来型AIを上回る性能が報告されている。
AIの課題として、従来型では感度87.0〜95.2%に対して特異度49.6〜68.8%と偽陽性率が高い点が挙げられている。実臨床への導入には偽陽性の低減と汎化性能の向上が求められる。
AI技術を活用し、患者個々のリスク因子(HbA1c推移、罹患期間、腎機能など)に基づいて最適なスクリーニング間隔を算出する個別化スクリーニングの研究が進んでいる。一律の間隔設定ではなく、リスクに応じた効率的な資源配分の実現が目標とされる。
スマートフォンカメラに装着するアタッチメント型眼底撮影デバイスの開発が進んでいる。低〜中所得国を含む医療資源が限られた地域でのスクリーニング普及が期待されている。
AIスクリーニングは感度面では医師に近い性能を示しており、IDx-DRはFDA承認を取得している。しかし特異度が低く偽陽性が多い機種もあるため、AIで陽性と判定された場合は眼科専門医による確認が必要である。現時点では補助ツールとして位置づけるのが適切である。