非増殖糖尿病網膜症(NPDR)
非増殖糖尿病網膜症:軽症・中等症・重症の3段階に分類される。
軽症〜中等症:毛細血管瘤・硬性白斑・点状出血を認める。
重症:4象限の網膜内出血、静脈念珠状変化、網膜内微小血管異常(IRMA)のうち1つ以上。

糖尿病網膜症(Diabetic Retinopathy; DR)は、慢性高血糖に起因する網膜の微小血管障害を主体とした疾患である。糖尿病の最も重要な慢性合併症のひとつであり、先進国における成人視力障害の主要原因である。
従来は「微小血管疾患」と定義されてきたが、現在は**神経血管疾患(neurovascular disease)**として再定義されている。5) 血管病変が出現する以前に、OCTで網膜神経感覚構造の障害が検出されることが示されており、神経変性が血管病変に先行する可能性がある。5)
罹患率について、T1DMでは診断後20年以内に約90%、T2DMでは約60%にDRが生じるとされる。3) DRは以下の3つの主要な臨床病型に分類される。5)
非増殖糖尿病網膜症(NPDR)
非増殖糖尿病網膜症:軽症・中等症・重症の3段階に分類される。
軽症〜中等症:毛細血管瘤・硬性白斑・点状出血を認める。
重症:4象限の網膜内出血、静脈念珠状変化、網膜内微小血管異常(IRMA)のうち1つ以上。
増殖糖尿病網膜症(PDR)
増殖糖尿病網膜症:新生血管形成を特徴とする。
新生血管:網膜・視神経乳頭から発生し、硝子体内に伸展する。
線維化・牽引:新生血管が線維化し、牽引性網膜剥離をきたす。
糖尿病黄斑浮腫
糖尿病黄斑浮腫:非増殖糖尿病網膜症および増殖糖尿病網膜症のいずれの病期にも合併する。
血管透過性亢進:BRB(血液網膜関門)の破綻による。
視力低下:黄斑部への浮腫波及が直接の視力低下原因となる。
現在は神経血管疾患として再定義されており、血管病変の出現前から網膜神経感覚構造の障害がOCTで検出される。5) 詳細は「病態生理学」の項を参照。
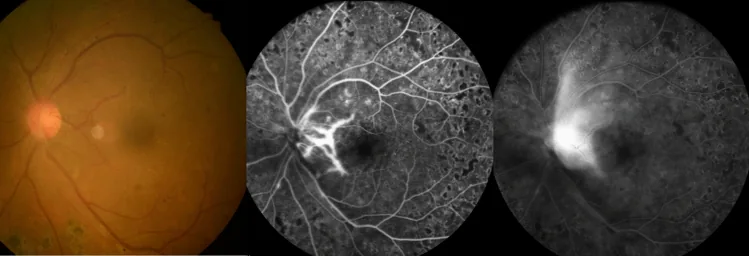
DRの初期は自覚症状に乏しい。病状の進行に伴い、以下の症状が現れる。
DRの病期分類(ICDR重症度分類)5)に応じた所見を示す。
| 病期 | 主な眼底所見 | 備考 |
|---|---|---|
| 軽症非増殖糖尿病網膜症 | 毛細血管瘤のみ | 最早期変化 |
| 中等症非増殖糖尿病網膜症 | 点状出血・硬性白斑 | 黄斑浮腫合併に注意 |
| 重症非増殖糖尿病網膜症 | 4象限出血・IRMA | 増殖糖尿病網膜症移行リスク高 |
| 増殖糖尿病網膜症 | 新生血管・硝子体出血 | 線維化・牽引剥離 |
DRに先行して神経変性が生じる。OCTでは、血管病変の出現より早期に神経感覚構造の菲薄化が検出される。5)
DRの発症・進行に関与する主なリスク要因を以下に示す。
血糖管理はDR予防に有効だが、一度高血糖に曝露された網膜細胞には「代謝記憶」と呼ばれるエピジェネティック変化が刻まれ、血糖を正常化した後も病変が進行しうる。3) 詳細は「代謝記憶」の項を参照。
DRの診断と病期評価には以下の検査が用いられる。5)
血糖・血圧・脂質の厳格な管理がDRの基本治療である。
眼内抗VEGF薬(ラニビズマブ・アフリベルセプト・ベバシズマブ)はDMEの第一選択治療である。増殖糖尿病網膜症に対する汎網膜光凝固の代替・補助としても使用される。
抗VEGF抵抗性を示すDMEが約40%存在し、その多くにRAAS活性化の関与が示唆されている。1)
**ファリシマブ(Faricimab)**はANG2とVEGF-Aを標的とした二重抗体であり、最大16週間隔の投与間隔延長が可能とされる。1)
網膜局所RAASの関与を標的とした治療として、以下の臨床試験結果が報告されている。1)
DIRECT試験では、T2DM患者においてcandesartanがDRの34%退縮をもたらすことが報告された。1)
Mauer(2009, NEJM)の報告では、enalaprilがDR進行を65%、losartanが70%抑制したことが示されている。1)
フィネレノン(非ステロイド性ミネラルコルチコイド受容体拮抗薬)は血液網膜関門(BRB)破綻・血管新生・炎症を軽減する効果が示されている。1)
メトホルミンはAMPK活性化を介して抗酸化・抗炎症・抗血管新生・神経保護の多面的作用を発揮する。4) 観察研究の主要結果は以下の通りである。
| 研究 | 比較 | 結果 |
|---|---|---|
| Li 2018(n=335)4) | 非使用 vs 使用 | 重症非増殖糖尿病網膜症/増殖糖尿病網膜症 47% vs 25% |
| Fan 2020(n=10,044)4) | 非使用 vs 使用 | STDR aHR=0.29 |
| 抗VEGF併用4) | 非使用 vs 使用 | 抵抗性45.3% vs 73.2% |
観察研究ではメトホルミン使用者でDR発症リスクおよび進行リスクの有意な低下が報告されている。4) しかし、眼科的適応としてのRCTデータは不十分であり、現時点では標準治療として確立されていない。内科的糖尿病管理の一環として処方されることが現実的である。
DRの病態は「高血糖」を起点とした複数の代謝経路の同時活性化から始まり、酸化ストレス・炎症・RAAS経路・BRB破綻・神経変性が複雑に絡み合う。
高血糖状態では以下の4つの代謝経路が同時に活性化される。3)
| 経路 | 主な産物/変化 | 主要な下流障害 |
|---|---|---|
| ポリオール経路 | ソルビトール蓄積 | NADPH枯渇・GSH低下 |
| AGEs形成 | RAGE活性化 | NF-κB↑・VEGF↑ |
| PKC活性化 | PKC-β活性化 | VEGF・Nox亢進 |
| ヘキソサミン経路 | UDP-GlcNAc過剰 | TGF-β・PAI-1増加 |
ポリオール経路では、グルコースがアルドース還元酵素によりソルビトールへ変換される際にNADPHが消費される。NADPHの枯渇はグルタチオン(GSH)合成を障害し、酸化ストレスを増幅させる。3)
**AGEs(終末糖化産物)**はRAGEを介してNF-κBを活性化し、周細胞のアポトーシスとVEGF発現増加を誘導する。3)
PKC-β活性化はジアシルグリセロール(DAG)蓄積を介して生じ、VEGFおよびNADPHオキシダーゼ(Nox)の亢進をもたらす。3)
ミトコンドリアの電子伝達系(ETC)はスーパーオキシド産生の主要源であり、高血糖下ではComplex IおよびIIIからの活性酸素種(ROS)産生が亢進する。3)
高血糖はDrp1/OPA1の不均衡を引き起こし、ミトコンドリアの過剰な断片化(fission亢進)をもたらす。3) さらに、Nox2由来のROSがミトコンドリア機能障害をさらに悪化させるフィードフォワードループが存在する。3)
He Wら(2025)は、粘膜類天疱瘡-9がミトコンドリアに移行して損傷を引き起こし、カスパーゼを介した毛細血管細胞アポトーシスを誘導することを報告している。3)
Nrf2/KEAP1経路は抗酸化応答の中心的制御因子であり、DR病態においてその機能が障害される。3)
SIRT1はNF-κBのp65サブユニットを脱アセチル化することでNF-κB活性を抑制し、p66Shcを介したミトコンドリアROS産生も制御する。3)
「代謝記憶(metabolic memory)」とは、一度高血糖に曝露された網膜細胞が血糖正常化後もエピジェネティック変化を保持し、病変が持続・進行する現象である。3)
主要なエピジェネティック変化として以下が報告されている。3)
網膜局所RAASには3つのシグナル経路が存在する。1)
古典的経路
ACE/AngII/AT1R軸:有害作用を担う主要経路。
周細胞アポトーシス:AngIIがインテグリンβ3/β1を介して誘導する。
白血球停滞:AngII→NADPH oxidase→ROS→ICAM-1↑のカスケードによる。
保護的経路
ACE2/Ang-(1-7)/Mas軸:古典的経路に拮抗する保護的経路。
抗炎症作用:Ang-(1-7)がMas受容体を介して炎症を抑制する。
血管保護:古典的経路の過剰活性化を均衡させる。
プロレニン経路
プロレニン/(P)RR軸:(P)RR(プロレニン受容体)を介する。
GPR91:高血糖→コハク酸蓄積→GPR91活性化→レニン放出のカスケード。
網膜特異性:局所でのRAAS活性化の起点となる。
AngIIはNADPHオキシダーゼ(Nox)を介してROSを産生し、ICAM-1発現を増強することで白血球の網膜血管への停滞(白血球停滞)を引き起こす。白血球停滞はDRの炎症性病態の中心的過程であり、ICAM-1が最も重要な接着分子とされる。1)
アルドステロンはミネラルコルチコイド受容体(MR)を介してMüller細胞の膨化を誘導し、BRB破綻に寄与する。1)
DRは炎症性疾患としての側面を持ち、白血球停滞・ミクログリア活性化・サイトカイン産生が病態を増幅する。5)
**フラクタルカイン(CX3CL1)**は膜結合型と可溶型の二重機能を持つケモカインである。2)
網膜神経節細胞がフラクタルカインの主産生源であり、ミクログリアのみがその受容体CX3CR1を発現する。2)
Lee CYら(2025)は、CX3CR1欠損マウスではミクログリアが過活性化し、神経細胞死・フィブリン漏出増加が生じることを報告している。2) また可溶性フラクタルカインはNF-κB阻害とNrf2増強を介してROS・炎症性サイトカインを減少させる。
増殖糖尿病網膜症患者の硝子体中では、VEGFとCX3CL1に正の相関が認められている。2)
BRBは内側BRB(iBRB:網膜血管内皮細胞)と外側BRB(oBRB:網膜色素上皮細胞)から構成される。DRではiBRBの破綻が主要な病態である。6)
主要なBRB破綻機序:6)
血管病変に先行して神経変性が生じることが、DRの神経血管疾患としての再定義の根拠である。5)
RAAS(レニン-アンジオテンシン-アルドステロン系)は血圧・電解質調節の全身システムだが、網膜には循環系から独立した局所RAASが存在し、全成分が発現している。1) 網膜内AngII濃度は循環中より高く、周細胞アポトーシス・白血球停滞・BRB破綻・VEGF産生を直接駆動する。
Lee CYら(2025)は、rAAV-sFKN(可溶性フラクタルカインを発現するアデノ随伴ウイルスベクター)の投与により、視力改善・フィブリン漏出減少・ミクログリアの正常化が得られることを報告している。2) この遺伝子治療アプローチは、抗VEGF療法とは異なる神経保護・抗炎症機序に基づく。
miRNAは複数の疾患関連遺伝子を同時に制御する「マスターレギュレーター」として注目されている。3)
経口投与では眼内移行が限られるメトホルミンについて、点眼製剤などの眼局所投与製剤の開発が進んでいる。4) AMPK活性化による網膜局所での抗血管新生・神経保護効果の発揮が期待される。
天然抗酸化化合物および抗酸化ナノ製剤に関する研究が進んでいる。3)
フィネレノンは非ステロイド性MR拮抗薬として心腎保護試験(FIDELIO-DKD・FIGARO-DKD)で評価されてきたが、網膜保護効果についても研究が進んでいる。1) BRB破綻・血管新生・炎症の軽減が前臨床モデルで示されており、DR独立した治療標的としてのMRの意義が注目されている。