眼球マッサージ
手技:眼球を5〜10分間間欠的に圧迫し、眼圧を低下させて塞栓の末梢移動を促す。
注意:発症早期(目安4時間以内)に行う。眼球マッサージ+前房穿刺の組み合わせは自然経過と比較して予後を改善しない可能性がある。

網膜動脈分枝閉塞症(Branch Retinal Artery Occlusion; BRAO)は、網膜中心動脈(CRA)から分岐した分枝血管が閉塞し、その支配領域の網膜に虚血性障害をきたす疾患である。網膜動脈閉塞症(RAO)全体の約38%を占める5)。
BRAOは閉塞の持続性により2つのサブタイプに分類される。
網膜動脈閉塞症の発生率は米国で年間人口10万人あたり約1.33例、韓国の65歳以上では1.8例と推定される5)。発症率は年齢とともに増加し、80歳前後でピークに達する。男性に多い傾向がある5)。
無症状の網膜塞栓は49歳以上の一般集団の約1.4%に認められるとされる(Blue Mountains Eye Study)5)。
2013年のAHA/ASA(米国心臓協会/脳卒中協会)改訂版脳卒中定義では、網膜虚血はCNS(中枢神経系)梗塞の一型として明示的に位置づけられた5)。新規RAO診断後の脳卒中リスクは最大25%に達する5)。
BRAOは脳卒中の眼所見として現れる場合があり、新規発症後の脳卒中リスクは最大25%とされる5)。AHA/ASAは網膜虚血をCNS梗塞に含めており、発症後は神経科・循環器科と連携した全身評価が不可欠である。頸動脈超音波・心エコーなどの塞栓源検索を迅速に行う必要がある。
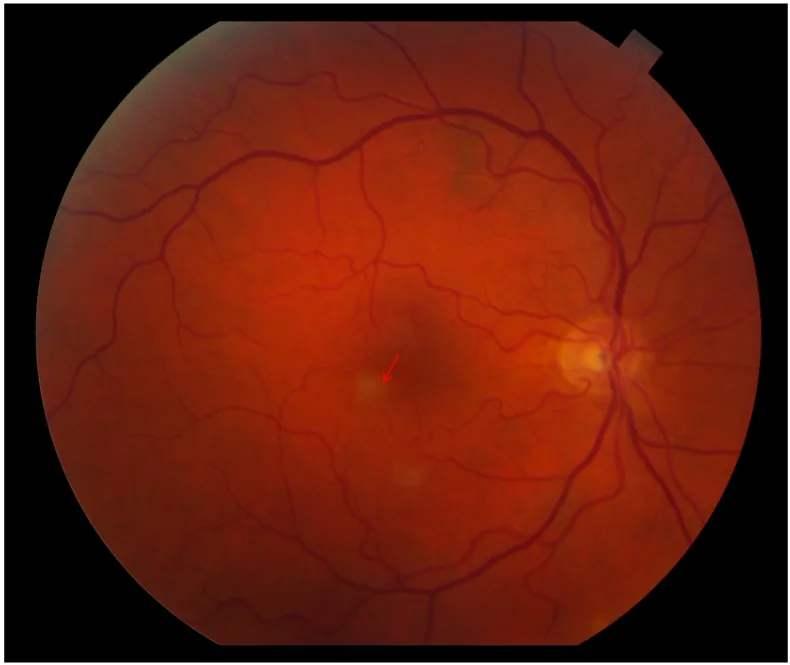
BRAOは典型的に以下の症状で発症する。
症例として、49歳女性がフェンテルミン内服中に急性無痛性視野欠損を訴えたが矯正視力は20/20に保たれていた1)。22歳男性ではレーザーポインター照射後にカーテン様の上方視野欠損が生じた3)。61歳男性では経皮的冠動脈形成術(PTCA)中に上方視野欠損を生じ、視力は6/36に低下した2)。
眼底所見・各種画像検査による主な所見を以下に示す。
BRAOの視力予後を下表に示す5)。
| 分類 | 初診時20/40以上 | 追跡時20/40以上 |
|---|---|---|
| 永久性BRAO | 74% | 89% |
| 一過性BRAO | 94% | 100% |
永久性BRAOでも追跡時に89%が矯正視力20/40以上を維持するとされる5)。一過性BRAOでは100%が20/40以上を保つ。ただし黄斑分枝の閉塞や治療の遅れがある場合は予後が悪化する可能性がある。発症4時間以内であれば回復が見込まれる。詳細は「標準的な治療法」の項を参照されたい。
BRAOの原因の大多数は頸動脈または心臓由来の塞栓である5)。主な塞栓の種類と由来を以下に示す。
| 塞栓の種類 | 主な由来 |
|---|---|
| コレステロール/フィブリン | 頸動脈・大動脈弓 |
| 石灰化塞栓 | 石灰化心臓弁 |
| 医原性塞栓 | PTCA・血管内治療 |
PTCAによる血栓塞栓症として発症した症例2)、神経血管内治療によるプラーク離開として発症した症例4)も報告されている。近年、美容目的の皮膚フィラー注入による網膜動脈閉塞が増加しており注目されている5)。
全身的なリスク因子として、喫煙・高血圧・高BMI・脂質異常症・糖尿病・心房細動が挙げられる5)。HDLコレステロール低値は独立したリスク因子とされる5)。
はい。フェンテルミン(食欲抑制薬)はノルエピネフリン再取り込み阻害作用により血管収縮・血管攣縮を引き起こし、BRAOを誘発した症例が報告されている1)。コカイン、シルデナフィル、フィラー注入なども原因となりうる5)。既往症や服用薬を眼科医・内科医に必ず伝えることが重要である。
BRAOの診断は眼底所見を基本とし、複数の画像検査と全身評価を組み合わせて行う。
各検査で得られる主な所見を以下に示す。
| 検査法 | 主な所見 |
|---|---|
| OCT | 急性期: 内層高反射・肥厚 |
| FA | 閉塞動脈の充盈遅延 |
| 網膜電図 | a波正常・b波減弱 |
急性症候性RAOは脳卒中センターへの緊急紹介が推奨される5)。主な全身評価を以下に示す。
一方、無症状のBRAOや偶発的に発見された網膜塞栓では、緊急の脳卒中評価を支持するエビデンスは現時点でないとされる5)。49歳女性のフェンテルミン関連BRAOでは全身検査がすべて陰性であった1)。
BRAOの治療では、脳卒中リスク評価を最優先に行う5)。一過性BRAOの多くは自然消退するが、永久性BRAOでも発症4時間以内の早期介入が予後に影響する2)。
眼球マッサージ
手技:眼球を5〜10分間間欠的に圧迫し、眼圧を低下させて塞栓の末梢移動を促す。
注意:発症早期(目安4時間以内)に行う。眼球マッサージ+前房穿刺の組み合わせは自然経過と比較して予後を改善しない可能性がある。
薬物療法
アセタゾラミド:500 mg静脈内投与により眼圧を低下させる。
ウロキナーゼ:6〜24万単位/日を約7日間投与。
オパルモン:5 μg錠を1日6錠(血流改善目的)。
亜硝酸アミル:0.25 mL吸入(血管拡張)。
全身評価・管理
塞栓源検索:頸動脈超音波・心エコー・凝固系検査などを緊急施行する。
脳卒中センター紹介:急性症候性RAOは脳卒中との関連が高く、神経科・循環器科との連携が必須である。
新生血管モニタリング:治療後も定期的な眼底検査を継続する。
発症4時間以内に前房穿刺(27G針で0.1〜0.4 mL除去)と眼球マッサージを行う。1症例では発症4時間以内に経口アセタゾラミドと眼球マッサージを施行して視力改善が得られた2)。血管攣縮が原因の場合にはカルシウム拮抗薬が有効な場合がある2)。
EAGLEスタディ(RCT)では、動脈内(IA)tPA対保存的治療において視力改善に有意差は認められず、頭蓋内出血(ICH)などの安全性上の懸念が示された4)。Schragのメタ解析では、静脈内(IV)tPAを発症4.5時間以内に投与した場合に視力回復率が約50%と報告されている4)。IA tPA 10.8 mgを投与した症例では眼内出血の合併症が生じたが、最終的に視力20/20を達成した4)。
閉塞後に虹彩新生血管・網膜新生血管が生じることがある。CRAOでは最大20%に虹彩新生血管が発生し、通常発症後30〜60日以内に出現する5)。汎網膜光凝固(PRP)が適応となる5)。
BRAOの約80%は矯正視力0.5以上を維持する。永久性BRAOでは追跡時に89%が20/40以上を保つ5)。発症4時間以内の治療介入で予後良好、7〜8時間を超えると回復は困難となる2)。
発症後約100分で網膜の虚血性変化が不可逆となり始めるとされ、4時間以内の介入が予後改善の目安である2)。7〜8時間を超えると視力回復は困難となる2)。また脳卒中リスクが最大25%あるため、症状出現後は直ちに眼科・救急を受診し、神経科との連携を取ることが重要である5)。
網膜動脈は内層網膜(神経線維層〜内顆粒層、内層2/3相当)を支配する。外層(光受容体層)は脈絡膜循環によって維持される。BRAOでは閉塞した分枝の支配域のみ内層網膜が虚血に陥り、外層は脈絡膜から酸素・栄養を受けて生存する。
毛様網膜動脈(cilioretinal artery)は全眼の約32%に存在し、脈絡膜循環から黄斑部の内層網膜に血流を供給する。網膜中心動脈完全閉塞でも毛様網膜動脈が温存されれば中心視力が保たれることがある。
実験的網膜動脈完全閉塞では97〜105分で重篤な網膜障害が生じる。慢性高血圧の状態では不可逆変化が生じるまでの時間が最大240分に延長するとの報告がある4)2)。OCTで観察される急性期の内層肥厚は細胞内浮腫(虚血性腫脹)を、慢性期の内層菲薄化はアポトーシスによる虚血性萎縮を反映する5)。閉塞血管は最終的に再疎通するが、視力は通常回復しない5)。
Hollenhorst plaqueはコレステロール結晶からなり、頸動脈や大動脈弓の動脈硬化プラークから遊離して網膜動脈の分岐部(bifurcation)に嵌頓する5)。フェンテルミンはノルエピネフリン再取り込みを阻害して交感神経系を賦活化し、血管収縮・血管攣縮を引き起こすと考えられる1)。レーザーポインターによるBRAOでは、熱的・光化学的・光機械的傷害が血管壁障害を引き起こす3)。
2013年のAHA/ASA改訂定義で網膜虚血がCNS梗塞として認定されたことにより5)、急性RAOに対する脳卒中プロトコールの適用を支持する動きが加速している。MacGroryら(2019)は61例のtPA投与患者を対象とした検討を報告しており4)、今後のRCTの基盤となりうる。
Schragのメタ解析では、発症4.5時間以内のIV tPA投与により視力回復率が約50%と報告された4)。ただし、EAGLEスタディではIA tPAの有効性は示されず安全性懸念も指摘されており、IV tPAに関しても十分なRCTエビデンスが不足している4)。
OCTA技術の進歩により、表層網膜の灌流欠如を発症後9年以上にわたって追跡可能となった1)。長期の微小血管変化の詳細な解明が期待される。
眼窩超音波で石灰化塞栓を検出する「スポットサイン」は感度83%・特異度100%と報告されており4)、非侵襲的な急性期診断補助として注目されている。
フェンジメトラジンなどフェンテルミン類似薬との網膜静脈閉塞症の関連も報告されており1)、薬剤性RAOの認識向上が課題である。神経保護薬(neuroprotective agents)の開発も進行中であるが、臨床での有効性は未確立である。
レーザーBRAO
世界初報告:450〜495 nmの青色レーザーポインターへの3秒間曝露によるBRAOが報告された3)。
機序:熱的・光化学的・光機械的傷害による血管壁障害と考えられる。
tPAの現状
EAGLE試験:IA tPAは保存的治療と比較して視力改善効果なく、ICHリスクあり4)。
IV tPA:発症4.5時間以内で約50%の視力回復率(メタ解析)だが、RCTエビデンス不十分4)。