
セマグルチドと関連する眼科的リスク
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. セマグルチドと関連する眼科的リスクとは
Section titled “1. セマグルチドと関連する眼科的リスクとは”セマグルチドはGLP-1受容体作動薬(GLP-1RA)であり、高血糖に応答してインスリン分泌を促進し血糖値を低下させる薬剤である。2017年12月にオゼンピック(Ozempic)として2型糖尿病(T2DM)治療でFDA承認され、2022年12月には肥満症治療薬ウゴービ(Wegovy)としても承認された。2021〜2023年に米国でのGLP-1RAの週間処方数は約60%増加しており、その使用拡大とともに眼科的副作用への関心が高まっている。
主に報告されている眼科的リスクは以下の2つである。
- 糖尿病網膜症(DR)の悪化:急速な血糖降下に伴うearly worsening(早期悪化)として生じる可能性がある。
- 非動脈炎性前部虚血性視神経症(NAION):視神経乳頭への血流低下によって急性・無痛性の視力低下を来す疾患で、虚血性視神経症の最も一般的な形態である。非動脈炎性前部虚血性視神経症の推定年間発生率は50歳以上で10万人あたり2.3〜10.2であり3)、有効な治療法がなく、半数以上で急性期後も視力改善が得られない。3)
黄斑浮腫も関連する所見として報告されているが、DR悪化の文脈で生じることが多い。
主に非動脈炎性前部虚血性視神経症(非動脈炎性前部虚血性視神経症)と糖尿病網膜症の悪化の2つが報告されている。黄斑浮腫も関連所見として挙げられる。いずれも因果関係が確立しているわけではなく、特に非動脈炎性前部虚血性視神経症については研究によって結論が異なる。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”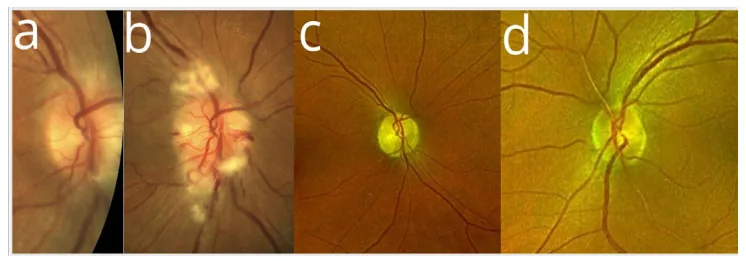
- 急性・無痛性の視力低下(非動脈炎性前部虚血性視神経症関連):片眼に突然発症する。非動脈炎性前部虚血性視神経症は通常痛みを伴わない。
- 視力低下・飛蚊症(DR悪化関連):セマグルチド開始後に既存の網膜症が進行することで生じる。硝子体出血では飛蚊症を訴えることもある。
- 中心視力の低下・歪視(黄斑浮腫関連):DR悪化に伴う黄斑浮腫では中心視力低下や変視を来す。
- 視神経乳頭浮腫(非動脈炎性前部虚血性視神経症急性期):急性期に乳頭浮腫が認められる。慢性期には視神経萎縮へ移行する。視野障害を伴う。
- 増殖糖尿病網膜症の進行(DR悪化):新生血管の出現、硝子体出血、牽引性網膜剥離等が生じる。
- 黄斑浮腫:DR悪化に伴い黄斑部に浮腫が生じる。
SUSTAIN-6試験では、セマグルチド群でプラセボ群と比較して網膜症関連合併症(失明、硝子体出血、光凝固術の必要性、硝子体内注射の使用)のリスクが有意に高かった(HR 1.76; 95% CI, 1.11–2.78; P = 0.02)。4)
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”セマグルチドによるDR悪化のメカニズム(推定)
Section titled “セマグルチドによるDR悪化のメカニズム(推定)”- 急速な血糖降下(early worsening):HbA1cの急速な低下が既存の網膜症を一時的に悪化させる可能性がある。これは厳格な血糖コントロール(DCCT試験)で既知の現象であり、セマグルチドにも同様の機序が働くと考えられている。
DR悪化のリスク因子
Section titled “DR悪化のリスク因子”23のRCTメタアナリシス(22,096例)では、セマグルチド群のDR発症リスク比はプラセボと比較してRR 1.24(95% CI, 1.03–1.50)であった。4)
特に以下の患者でDR悪化リスクが高い。
- 既存の糖尿病網膜症(特に重症例)
- 60歳以上(RR 1.27; 95% CI, 1.02–1.59)4)
- 糖尿病罹病期間10年以上(RR 1.28; 95% CI, 1.04–1.58)4)
非動脈炎性前部虚血性視神経症の一般的なリスク因子
Section titled “非動脈炎性前部虚血性視神経症の一般的なリスク因子”- 小さいcup-to-disc ratio(crowded disc):非動脈炎性前部虚血性視神経症の最も強いリスク因子であり、糖尿病等の全身リスク因子より重要とされる。2)
- 高血圧、高脂血症、糖尿病、閉塞性睡眠時無呼吸
- リスクを増加させうる薬剤:アミオダロン、ホスホジエステラーゼ阻害薬3)
セマグルチドと非動脈炎性前部虚血性視神経症の関連の仮説
Section titled “セマグルチドと非動脈炎性前部虚血性視神経症の関連の仮説”因果関係は確立していないが、以下の仮説が提唱されている。
- GLP-1RAが自律神経系を介して血管動態に影響し、全身血圧を低下させることで視神経乳頭灌流に影響する可能性2)
- ヒトの視神経にGLP-1受容体が存在し、GLP-1RAによる交感神経活動亢進が非動脈炎性前部虚血性視神経症感受性を高める可能性
- 一方でGLP-1RAには神経保護作用・虚血リスク低減作用も報告されており、メカニズムは不明である2)
非動脈炎性前部虚血性視神経症は稀な疾患であり(10万人年あたり14.5程度)、セマグルチド使用患者がすべて非動脈炎性前部虚血性視神経症を発症するわけではない。複数の大規模研究ではリスク増加は小さく、研究によっては有意差が認められなかったものもある。セマグルチドの血糖管理・心血管保護のベネフィットが非動脈炎性前部虚血性視神経症の潜在的リスクを上回る可能性が指摘されている。3)
4. 診断と検査方法
Section titled “4. 診断と検査方法”セマグルチド使用患者においては、以下のモニタリング・評価が重要である。
- 散瞳下眼底検査:セマグルチド開始前に実施を検討し、DR等の眼合併症の診断と治療を同時に行う。
- T2DM診断時のDRスクリーニング:T2DM診断時に眼底検査を行い、既存の網膜症の有無を確認する。
治療中のモニタリング
Section titled “治療中のモニタリング”- 定期的眼底検査:セマグルチド開始後、特に既存DR患者ではDR悪化の早期発見のため定期検査を行う。T2DM診断後は毎年スクリーニングを継続する。
- 非動脈炎性前部虚血性視神経症が疑われた場合:視力検査、視野検査、眼底検査(視神経乳頭浮腫の確認)、蛍光眼底造影を行う。
5. 臨床的推奨事項
Section titled “5. 臨床的推奨事項”DR関連の推奨事項
Section titled “DR関連の推奨事項”- セマグルチド療法開始前に散瞳下眼底検査を行い、併発するDRの診断・治療を同時に行う。
- 急激なDR悪化リスク軽減のため、インスリン療法の減量やスルホニル尿素薬の中止を検討する。
- 重症DRでは血糖降下療法の前または並行して網膜症治療を開始する(一過性の悪化が予想される)。
- DR管理ガイドラインは他の糖尿病治療薬使用患者と同様に適用する(抗VEGF薬、網膜光凝固術等)。
非動脈炎性前部虚血性視神経症関連の推奨事項
Section titled “非動脈炎性前部虚血性視神経症関連の推奨事項”- 非動脈炎性前部虚血性視神経症の既往・リスクがある患者には、セマグルチドと視力喪失の関連の可能性について事前に十分な説明を行う。
- インスリン治療の併用や疾患進行例では慎重なアプローチが必要である。
セマグルチド開始前に散瞳下眼底検査の実施が推奨される。既存のDRがある場合は診断と治療を同時に行い、重症DRがあれば血糖降下療法と並行して網膜症治療の開始を検討する。T2DM診断時および毎年の定期的なDRスクリーニングも重要である。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”セマグルチドの薬理作用
Section titled “セマグルチドの薬理作用”セマグルチドは長時間作用型GLP-1受容体作動薬である。
- 高血糖に応答してインスリン分泌を刺激する。
- グルカゴン放出を抑制し、肝臓での糖新生を抑制して血糖値を低下させる。
- 胃排泄遅延、空腹感・食物渇望の軽減を通じて体重減少を促進する。
- DPP-4による急速な分解に抵抗し、持続的治療効果をもたらす。
DR悪化の機序
Section titled “DR悪化の機序”DR悪化の主要な機序は急速な血糖降下に伴うearly worsening(早期悪化)である。
- SUSTAIN-6試験では、セマグルチド群で網膜症関連合併症のHR = 1.76(95% CI, 1.11–2.78)が報告された。4)
- 23のRCTメタアナリシス(22,096例)において、セマグルチド vs プラセボでDR発症RR 1.24(95% CI, 1.03–1.50)が示された。4)
- HbA1cの急速な低下が既存の網膜症血管に機能的・構造的変化をもたらすと推定されているが、詳細な機序は解明されていない。
非動脈炎性前部虚血性視神経症との関連の病態仮説
Section titled “非動脈炎性前部虚血性視神経症との関連の病態仮説”非動脈炎性前部虚血性視神経症は多因子性疾患であり、血管因子(視神経乳頭低灌流)と解剖学的因子(小さいcup-to-disc ratio、視神経乳頭ドルーゼン)が組み合わさって発症する。3)
- GLP-1RAが自律神経系を介して血管動態に影響し、全身血圧低下から視神経乳頭灌流への影響が生じる可能性がある。2)
- セマグルチドは脳卒中予防効果を有し(SUSTAIN 6 + PIONEER 6プール解析)、小血管閉塞に対して有効とされる。3)
- しかし、GLP-1RAと非動脈炎性前部虚血性視神経症の既知の機序的リンクは存在せず2)、神経保護作用・虚血リスク低減作用も報告されていることから、非動脈炎性前部虚血性視神経症発症への関与は不明である。
7. 最新の研究と今後の展望(研究段階の報告)
Section titled “7. 最新の研究と今後の展望(研究段階の報告)”セマグルチドと非動脈炎性前部虚血性視神経症の関連を検討した3つの主要研究があるが、結論は一致していない。以下に各研究の概要を示す。
Hathaway JTら(2024)は Massachusetts Eye and Ear での後方視的マッチドコホート研究(2017年12月〜2023年11月)を報告した1)。T2D群(セマグルチド194人 vs 非GLP-1RA 516人)では、36か月累積非動脈炎性前部虚血性視神経症発生率はセマグルチド群 8.9%(95% CI, 4.5%–13.1%)に対し非GLP-1RA群 1.8%(95% CI, 0%–3.5%)、HR 4.28(95% CI, 1.62–11.29; P < .001)であった。過体重/肥満群(セマグルチド361人 vs 非GLP-1RA 618人)でもHR 7.64(95% CI, 2.21–26.36; P < .001)と有意なリスク増加が認められた。リスクは処方後最初の1年以内に最も顕著であり、薬剤誘発性の可能性を示唆する。ただし単施設・専門施設での研究であり、HbA1c・BMI・インスリン使用が未調整という限界がある。
Cai CXら(2025)はOHDSI 14データベース(T2D患者3,710万人)を用いた大規模後方視的研究を報告した2)。セマグルチド新規使用者の非動脈炎性前部虚血性視神経症発生率は10万人年あたり14.5(sensitive定義)。コホート分析では他のGLP-1RAや非GLP-1RA薬との比較でいずれも有意差は認めなかった。自己対照症例シリーズ(SCCS)分析ではセマグルチド曝露中の非動脈炎性前部虚血性視神経症リスク増加(IRR 1.32; 95% CI, 1.14–1.54; P < .001、specific定義)が確認されたが、Hathaway研究より小さいリスクであった。デュラグルチドでは非動脈炎性前部虚血性視神経症リスク増加を認めず、セマグルチド特異的な可能性が示唆された。
Chou CCら(2025)はTriNetX(21か国、約2億人)を用いた多国籍人口ベースコホート研究を報告した3)。T2DMのみ・肥満のみ・T2DM+肥満の3群(計29万人超)に分けて解析した結果、いずれの群においても最大3年間の追跡で非動脈炎性前部虚血性視神経症リスクの有意な増加は認められなかった(T2DMのみ群の3年HR 1.51; 95% CI, 0.71–3.25)。BMI・HbA1c・インスリン使用を調整しており、一般人口ではセマグルチドと非動脈炎性前部虚血性視神経症の有意な関連を示さないと結論付けた。
3研究の結果をまとめると以下のようになる。
| 研究 | 対象規模 | 主な結果(NAION) | 結論 |
|---|---|---|---|
| Hathaway 20241) | 単施設 約1,700人 | T2D群 HR 4.28 | 有意なリスク増加 |
| Cai 20252) | OHDSI 3,710万人 | SCCS IRR 1.32 | 小さなリスク増加 |
| Chou 20253) | TriNetX 約30万人 | 3年 HR 1.51(ns) | 有意差なし |
今後の課題:因果関係を確認するための前向きコホート研究・臨床試験が必要である。3) 眼科的リスク因子(cup-to-disc ratio等)を含めた研究、用量依存性の評価も重要な課題である。2) 臨床医は非動脈炎性前部虚血性視神経症という稀だが失明の可能性がある疾患のリスクと、セマグルチドの多くの治療的ベネフィットを比較考量すべきである。2)
研究デザインの違いが主な原因である。Hathaway研究は単施設・専門施設での少数例コホートであり選択バイアスが懸念される。Cai研究は3,710万人の大規模データだが自己対照設計に限界がある。Chou研究は集団を3群に分けBMI・HbA1c・インスリン使用を調整した点が特徴であり、交絡因子の調整法の違いが結論に影響している。
8. 参考文献
Section titled “8. 参考文献”- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of Nonarteritic Anterior Ischemic Optic Neuropathy in Patients Prescribed Semaglutide. JAMA Ophthalmol. 2024;142(8):732-739.
- Cai CX, Mathioudakis N, Fan R, et al. Semaglutide and Nonarteritic Anterior Ischemic Optic Neuropathy. JAMA Ophthalmol. 2025;143(4):304-314.
- Chou CC, Pan SY, Sheen YJ, et al. Association between Semaglutide and Nonarteritic Anterior Ischemic Optic Neuropathy: A Multinational Population-Based Study. Ophthalmology. 2025;132(4):381-388.
- American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.
