COVID-19感染後に虚血性視神経 症(ION)と視神経炎 (ON)の2タイプの視神経症が報告されている。
IONには前部虚血性視神経症(AION)と後部虚血性視神経症 (PION)の両方が含まれる。
推定される発症機序は炎症性サイトカイン放出・凝固亢進・内皮障害・低酸素血症(ION)および自己免疫性脱髄(ON)である。
視神経炎にはメチルプレドニゾロンパルス療法が用いられ、適切な治療を行えば予後は一般的に良好である。
非動脈炎性AIONに対する確立された有効な治療法は存在しない。
COVID-19自体が炎症マーカーを上昇させるため、巨細胞性動脈炎 (GCA)との鑑別が難しくなる点に注意が必要である。
ワクチン接種後にもNAION ・ONの発症が報告されており、今後の研究が待たれる。
COVID-19後の視神経症は、SARS-CoV-2感染後に発症する視神経障害の総称である。主に2つのタイプが報告されている。
虚血性視神経症(ION) :視神経への血液供給の遮断による急性視力 低下。前部(AION)と後部(PION)に分類され、AIONはさらに動脈炎性(A-AION)と非動脈炎性(NA-AION)に分けられる。視神経炎(ON) :炎症により視神経が障害されて視機能が低下する疾患。乳頭炎型と球後視神経炎型の両方が報告されている。
成人における急性視神経症としては、非動脈炎性前部虚血性視神経症と視神経炎が最も一般的な2疾患とされる。COVID-19感染との時間的関連は、感染随伴性(感染中)と感染後(回復後数日〜数週間後)の両形態で報告されている。正確なメカニズムはいまだ不明であるが、炎症反応・凝固亢進状態・低酸素血症・自己免疫反応が関与すると考えられている。
Q COVID-19のワクチン接種でも視神経症は起こるのか?
A ワクチン接種後に非動脈炎性前部虚血性視神経症およびONの発症が報告されている。感染と接種の組み合わせが免疫反応を増強する可能性も示唆されており、詳細は「最新の研究と今後の展望」の項 を参照のこと。
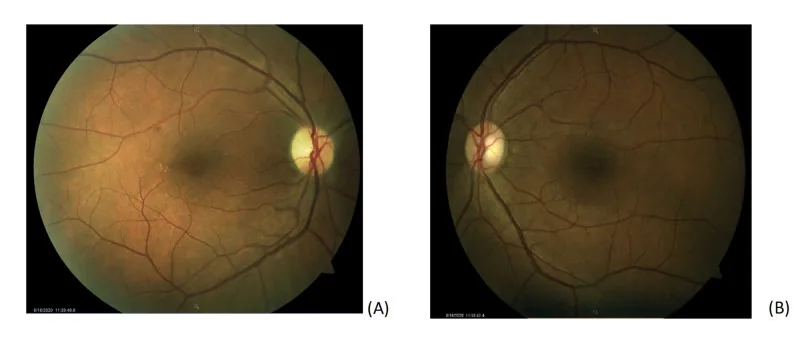
post covid optic neuropathy bilateral fundus A Case of Non-Arteritic Anterior Ischemic Optic Neuropathy with COVID-19. Cureus.; 12(12):e11950. Figure 1. PMCID: PMC7785499. License: CC BY.
Color fundus photography of both eyes. (A) Fundus photo of the right eye showing a small microaneurysm with exudates along the superotemporal arcade without subretinal fluid and temporal pallor of the optic nerve. (B) Fundus photo of the left eye is normal with a cup-to-disk ratio of 0.3.
IONの症状
発症様式 :突然の無痛性視力低下。朝の起床時に自覚することが多い。
発症時期 :COVID-19感染後数日〜数週間で発症。
視野異常 :水平半盲(特に下方)として自覚されることが多い。
罹患眼 :多くは片眼性。
ONの症状
発症様式 :急性の視力低下。眼球運動痛を約6割に認める。
発症時期 :COVID-19陽性判定後数日〜数ヶ月で発症。
色覚異常
罹患眼 :片眼性が多いが両眼例もある。
ION(NAION)の所見:
視神経乳頭腫脹 :びまん性または分節状の腫脹。乳頭周囲網膜 浅層の出血を伴う。対側眼の乳頭所見 :対側僚眼は小さな陥凹乳頭比(disc at risk)であることが多い。視野 :水平半盲(特に下方)が多い。RAPD
ION(PION)の所見:
急性期の眼底 :乳頭所見は正常。経過 :徐々に視神経萎縮 に転じ、乳頭蒼白化が出現する。
A-AION(GCA合併)の所見:
乳頭所見 :蒼白浮腫(pallid swelling)が特徴的。全身症状 :頭痛・顎跛行(jaw claudication)・前側頭部圧痛を伴う。
ONの所見:
乳頭炎型 :視神経乳頭の発赤腫脹・乳頭浮腫 。球後視神経炎型 :眼底所見は正常。視野 :中心暗点 ・盲中心暗点が多い(日本では約2割)。水平半盲は約1割。RAPD :陽性。眼窩 先端部症候群
Q IONと視神経炎の症状の違いは何か?
A IONは無痛性の急性視力低下が特徴であり、朝の起床時に気づくことが多い。一方、ONは眼球運動痛を約6割に伴い、色覚異常も認めやすい。視野パターンも、IONでは水平半盲、ONでは中心暗点が多いという違いがある。
構造的因子 :小さな陥凹乳頭比(disc at risk)。視神経乳頭の構造的な脆弱性がある。血管因子 :糖尿病・全身性高血圧・夜間低血圧・虚血性心疾患・貧血。COVID-19関連ION症例では糖尿病・高血圧の既往が多い。COVID-19特有の因子 :炎症性サイトカイン放出・凝固亢進状態・内皮障害・低酸素血症。これらが毛様血管の血栓症を介して視神経虚血を引き起こすと推測される。
神経親和性 :SARS-CoV-2が血液脳関門を通過し、感染白血球を介して中枢神経系に侵入する可能性がある。分子模倣(molecular mimicry) :ウイルス抗原が髄鞘タンパク質に対する自己免疫反応を誘発する。MOG-IgG抗体 :MOG抗体 産生によるMOGAD様の機序で脱髄が生じる症例が報告されている。発症時期との関係 :感染随伴性(無症状〜軽症時)と感染後(回復後数日〜数週間後)の両形態がある。
視力検査・視野検査 :Humphrey視野計を用いた定量的評価。視野パターンはIONとONの鑑別に有用。色覚検査 :ONでは赤色脱飽和などの色覚異常を認める。対光反射検査(RAPD) :視神経病変を強く示唆する所見。中心フリッカ値(CF F) :視神経疾患で低下する。眼底検査 光干渉断層計 (OCT)網膜神経線維層 の腫脹または菲薄化を評価する。
眼窩MRI :ONでは視神経の造影増強効果とSTIR画像での高信号を認める。冠状断脂肪抑制造影T1強調画像が有用。多発性硬化症 合併の評価にはFLAIR画像で側脳室周囲の脱髄斑を確認する。蛍光眼底造影 (FAG)
ESR・CRP :巨細胞動脈炎除外のために測定する。巨細胞動脈炎ではESR・CRP値が80%以上の症例で亢進し、CRPはESRより特異度が高い。ただし、COVID-19自体が炎症マーカーを上昇させるため、巨細胞動脈炎との鑑別が難しくなる点に注意が必要である。抗AQP4抗体 :ステロイド 抵抗性視神経炎の鑑別のために測定する。抗MOG抗体 :MOGAD様の機序が疑われる場合に測定する。血小板数 :凝固異常の評価として測定する。
以下の3疾患の鑑別ポイントを示す。
項目 非動脈炎性前部虚血性視神経症 動脈炎性前部虚血性視神経症 (巨細胞性動脈炎)視神経炎(ON) 年齢層 50歳以上 60歳以上 20〜40歳代が多い 眼痛 なし(無痛性) なし(無痛性) あり(眼球運動痛) 乳頭所見 淡い腫脹・出血 蒼白浮腫 発赤腫脹または正常 視野 水平半盲(下方) 重篤な下方欠損 中心暗点 MRI所見 通常異常なし 通常異常なし 視神経造影増強 ステロイド反応性 不良 良好(僚眼保護) 良好
非典型的視神経炎の判断基準として、以下のいずれかを満たす場合は視神経炎以外の疾患を鑑別する必要がある。
年齢が15〜45歳の範囲外
両眼同時発症
発症後2週間以降も進行
ステロイド依存性
全身症状の合併
非動脈炎性前部虚血性視神経症 vs A-AION の鑑別では、特に高齢者では側頭動脈生検が重要である。側頭動脈生検の感度・特異度はともに95%以上とされる。
Q COVID-19の炎症マーカー上昇が巨細胞動脈炎と間違われることはあるか?
A あり得る。COVID-19感染ではESRとCRPが著明に上昇することがあり、これが巨細胞動脈炎の所見と誤認される可能性がある。特に高齢のCOVID-19患者でAIONが生じた場合には、巨細胞動脈炎の偶発的な共存も念頭に置き、臨床症状・側頭動脈生検を含めた慎重な評価が必要である。
ステロイドパルス療法
メチルプレドニゾロン1,000mg/日 点滴静注、3日間施行する。
1回目で効果がなければ4〜5日あけて2回目を施行する。
パルス後はプレドニゾロン0.5mg/kg/日から内服を開始し、3〜4日ごとに5〜10mgずつ漸減する。
COVID-19関連ON症例でも同様のパルス療法+経口漸減プロトコルが用いられており、適切な治療を行えば予後は一般的に良好である。特発性視神経炎では無治療でも発症3週間以内に約8割で視力改善が始まり、9割以上で視力回復が期待できる。
小児例では体重換算で投与量を調整する(メチルプレドニゾロン15mg/kg/日 3日間→経口プレドニゾロン1mg/kg漸減)。
現時点では確立された有効な治療法は存在しない。抗凝固療法・血管拡張薬・ステロイド内服・視神経鞘減圧術 が試みられているが、有意な視力予後改善は証明されていない。
基礎疾患の管理 :血圧・糖尿病を含む動脈硬化リスク因子のコントロールが重要。血栓予防 :アスピリン等の抗血小板療法が推奨されることがある。自然予後 :COVID-19に関連しない非動脈炎性前部虚血性視神経症患者の約40%は視力がある程度自然回復する。発症後1〜2ヶ月で乳頭浮腫が消失し、ゆっくり視神経萎縮・蒼白化が進行する。安定期以降の視力低下の進行は非常にまれ。
確定または強く疑われた時点で、速やかにステロイド療法を開始する。治療が遅れると僚眼にも発症するリスクが高い(未治療では数日〜数週間内に約50%が僚眼発症)。
点滴療法 :メチルプレドニゾロン1g/日、3〜5日間。内服漸減 :プレドニゾロン1mg/kg/日から開始し、全身状態とESR値をみながら少なくとも4〜6ヶ月かけてゆっくり漸減する。症例により1年以上必要。予後 :罹患眼の視力改善はほとんど期待できないが、僚眼発症予防に効果あり。ステロイドで視機能が改善するのは4%のみ。ステロイド隔日投与は推奨されない。
ステロイドの単独内服療法は視神経炎の再発リスクを高めるため、ONに対してはパルス療法を行うこと。
ステロイド全身投与前にB型肝炎等の感染症を除外する必要がある。
ステロイドの長期投与では胃潰瘍・骨粗鬆症・高血糖・緑内障 ・白内障 などの副作用に注意する。
抗AQP4抗体陽性の視神経炎はステロイド抵抗性を示す場合があり(約1割)、別の治療戦略が必要となる。
Q 非動脈炎性前部虚血性視神経症に有効な治療法はないのか?
A 現時点では確立された有効な治療法は存在しない。動脈硬化リスク因子(血圧・血糖)のコントロールと、対側眼の発症予防が管理の中心となる。対側眼への発症率は年間15〜20%程度とされており、定期的な経過観察が重要である。
IONの機序
サイトカインストーム :SARS-CoV-2が炎症細胞(好中球・単球)と内皮細胞を活性化し、CRP・フェリチン・IL-2・TNF -αなどの炎症性サイトカインが血中で高値となる。
凝固亢進 :組織因子・フォン・ヴィレブランド因子の過剰産生により凝固促進状態が生じる。
補体 活性化
低酸素血症 :COVID-19による臨床的に重大な低酸素血症が毛様血管等の血栓症→視神経虚血を引き起こすとされる。
ONの機序
自己免疫反応 :SARS-CoV-2による分子模倣(molecular mimicry)が髄鞘タンパク質に対する自己抗体を誘発し、脱髄を引き起こす。
MOG-IgG抗体 :MOG抗体が産生されてオリゴデンドロサイトを標的とし、T細胞と補体結合が関与した脱髄が生じる。
神経親和性 :SARS-CoV-2は血液脳関門を通過し、感染白血球を介して中枢神経系に輸送される可能性がある。
発症様式 :感染随伴性(parainfectious)と感染後(postinfectious)があり、その区別は依然として不明確な部分がある。
COVID-19感染後に視神経周囲毛細血管網(放射状乳頭周囲毛細血管網:RPC P)の密度低下が認められたとする報告もあり、虚血の関与を示唆する所見として注目されている。なお、脳脊髄液(CSF)中のRT-PCR陰性でも中枢神経系感染を完全には排除できないことが知られている。
COVID-19関連視神経症の発症機序はいまだ完全に解明されておらず、特にIONにおけるCOVID-19の虚血性の起源はまだ確認されていない。さらなる研究が必要とされている。
現在、研究上の関心が高い領域を以下に示す。
ワクチン接種との関連 :COVID-19ワクチン接種後の非動脈炎性前部虚血性視神経症・ON症例が報告されており、感染とワクチン接種の組み合わせが免疫反応を増強する可能性が議論されている。機序の解明と頻度の把握が課題である。感染随伴性 vs 感染後ONの区別 :現時点でも両者の区別に明確な基準はなく、研究による整理が求められる。長期合併症の監視 :COVID-19後に他の神経学的合併症(ギラン・バレー症候群・急性横断性脊髄炎など)や将来的な脱髄疾患 (多発性硬化症など)が発症する可能性があり、長期フォローアップの体制が重要とされている。OCTを用いたバイオマーカー :RPCP密度の変化を含む視神経周囲の血流評価が、視神経虚血の早期検出指標として研究されている。
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください