急性HIT
血小板数:低下
機能的検査(SRA):陽性
免疫測定(ELISA):陽性
最もリスクが高い時期。すべてのヘパリンを即時中止し、非ヘパリン系抗凝固薬に切り替える。

ヘパリン起因性血小板減少症(Heparin-Induced Thrombocytopenia; HIT)は、ヘパリン投与に対して生じる免疫介在性反応である。血小板第4因子(PF4)とヘパリンの複合体に対するIgG抗体が産生され、血小板活性化を引き起こす。その結果、逆説的に血小板数が減少しながら血液が高凝固状態となる。
HITはI型とII型に分類される。HIT I型は一過性の血小板減少で自然軽快する。HIT II型は抗体介在性で、血栓塞栓合併症を伴う重篤な病態である。1)
眼科的合併症は、HITに伴う血栓・出血が眼の血管系に波及した際に生じる。HITによる全身管理と並行した眼科的対応が必要となる。
UFH投与患者では最大5%、LMWH投与患者ではその約1/10の発症率とされる。心臓手術後は0.1〜3%と一般集団より高く、致死率は最大10%に達する。2)
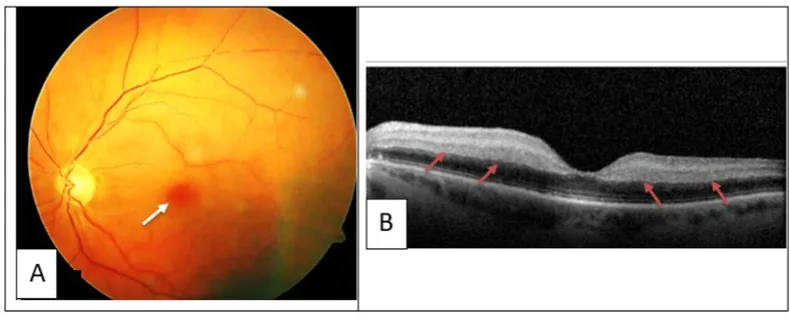
眼症状は血栓・出血の発生部位によって異なる。
HITの原因はヘパリン投与に対する免疫介在性反応である。主なリスク因子は以下の通りである。
LMWHでもHITは発症しうる。ただし発症率はUFHに比べて約1/10と低い。リスクが低いからといって血小板モニタリングを省略することはできない。
HITは除外診断である。ヘパリン投与後5〜14日の血栓症・血小板減少を認め、他の原因が否定された場合に疑う。
4Tスコアは4つの基準(Thrombocytopenia・Timing・Thrombosis・oTher causes)からなる臨床確率スコアである。各基準0〜2点で採点し、合計点で確率を分類する。
| 合計点 | 確率分類 |
|---|---|
| 6〜8点 | 高確率 |
| 4〜5点 | 中等度 |
| 0〜3点 | 低確率 |
4Tスコアの陽性的中率は中等度スコア4点で約10%、高確率スコア8点で約80%である。4)
心臓手術患者ではCPB後に血小板数が30〜50%低下するのが通常であり、さらにbiphasic pattern(二相性の血小板減少)を認める場合はHITに特徴的な所見として考慮する。3)1)
抗PF4/ヘパリン抗体(anti-PF4 ELISA)とセロトニン放出試験(SRA)が主要な検査法である。
ASHガイドラインは4Tスコア中等度以上の患者にanti-PF4 ELISAを推奨し、陽性ならSRAで確認する手順を示している。2)
anti-PF4 ELISA陰性かつSRA陽性という稀な乖離例(8,546例中16例、0.2%)も報告されており、臨床的にHITが強く疑われる場合は検査の乖離に注意が必要である。2)
HITの管理方針はフェーズによって異なる。3)
急性HIT
血小板数:低下
機能的検査(SRA):陽性
免疫測定(ELISA):陽性
最もリスクが高い時期。すべてのヘパリンを即時中止し、非ヘパリン系抗凝固薬に切り替える。
亜急性HIT A
血小板数:正常化
機能的検査(SRA):陽性
免疫測定(ELISA):陽性
血小板数は回復しているが機能的検査が陽性。心臓手術は可能なら延期する。
亜急性HIT B
血小板数:正常
機能的検査(SRA):陰性(中央値50日で陰転化)
免疫測定(ELISA):陽性
術中の短時間ヘパリン曝露は低リスク。術後はヘパリン回避を継続する。
Remote HIT
血小板数:正常
機能的検査(SRA):陰性
免疫測定(ELISA):陰性(中央値85日でPF4/H抗体消失)
再曝露時の短時間ヘパリン投与が可能な状態。
HITに続発する眼症状を認める患者では、他の全身症状がないか徹底的な病歴聴取と身体診察を行う。
血小板減少の程度(Thrombocytopenia)・発症時期(Timing)・血栓症の有無(Thrombosis)・他の原因の否定(oTher causes)の4基準でHITの臨床確率を評価するスコアである。合計0〜8点で、6点以上が高確率とされる。
HITと診断または強く疑われた時点で、以下を直ちに実施する。
アルガトロバン
分類:直接トロンビン阻害薬
半減期:39〜51分(正常肝機能)、肝障害時は181分まで延長
代謝:肝排泄型。腎障害例での使用に有利。
ビバリルジン
分類:直接トロンビン阻害薬
半減期:25分(正常〜軽度腎障害)
PCI用量:0.75 mg/kgボーラス + 1.75 mg/kg/h
CPB用量:1 mg/kgボーラス + 2.5 mg/kg/h(プライミング液に50 mg追加)3)
ASH 2018ガイドラインはPCIではビバリルジンを推奨している。PCIでの使用52例で処置成功率98%、重大出血1.9%が報告されている。3)
適切な非ヘパリン系抗凝固にもかかわらず血栓が進行する難治性HITでは以下を検討する。5)
急性HIT/亜急性HIT A患者に心臓手術が必要な場合は以下の3つの選択肢を考慮する。3)
網膜血管閉塞・眼窩出血などはHITの全身管理と並行して眼科的に対応する。
アルガトロバンまたはビバリルジンなどの直接トロンビン阻害薬に切り替える。いずれもヘパリンとは異なる機序でトロンビンを直接阻害するため、HIT抗体の影響を受けない。使用薬剤の選択は肝機能・腎機能・臨床状況によって決定する。
HITの発症は以下の段階で進行する。
Step 1:複合体形成と抗体産生
PF4(血小板第4因子)は巨核球由来の正に帯電したケモカインで、血小板α顆粒に貯蔵されている。PF4は負に帯電したヘパラン硫酸(血管内皮表面のGAG)やLPS(グラム陰性菌外膜)と複合体を形成する。これらの複合体が「危険信号」として機能し、IgG抗体の迅速な産生を可能にする。
Step 2:PF4-ヘパリン複合体の形成
ヘパリン投与によりPF4-ヘパリン複合体が形成される。ヘパリンはLPSやヘパラン硫酸と分子構造が類似しているため、既存のIgGが結合する。
Step 3:血小板活性化と凝固亢進
IgG-PF4-ヘパリン複合体が血小板上のFcγRII受容体(FcγRIIa)に結合し、血小板を活性化する。凝固カスケードの内因系経路が開始され、広範な血栓症と血小板消費による血小板減少が同時に生じる。これがHITの「逆説的」な病態の本質である。
通常のPF4以外にも、IL-8・プロタミン・NAP-2を標的とする抗体がHIT精査例の1%未満で検出される。2) また、ヘパリン非存在下でも血小板を活性化するanti-PF4抗体(ヘパリン非依存性HIT抗体)が難治性HIT・自己免疫性HITの病態に関与する可能性がある。5)
CPB後に最大50%の患者でPF4/H抗体のseroconversionが起こるが、臨床的HITに至るのは1〜2%のみである。1) CPB中のUFH高用量投与・組織因子放出・炎症がHIT抗体産生を促進すると考えられている。3)
マウスモノクローナルIgG2b型anti-PF4/H抗体KKOを脱グリコシル化した製剤である。FcγRIIa介在性結合をブロックすることで血小板活性化と補体活性化を抑制する。
マウスモデルでは血小板減少を改善し、血栓サイズを縮小したことが報告されている。5) 今後の臨床試験での評価が必要な段階である。
P2Y12阻害薬カングレロルを用いてCPB中にヘパリンを再投与する戦略が検討されている。
10例の症例集積では、VerifyNow P2Y12 PRUで投与量を調整しながら実施し、血栓合併症は報告されなかった。5) 確立されたプロトコールには至っていない。
TPEの有効性は認識されているが、統一されたプロトコールは確立されていない。
システマティックレビュー(30例)ではTPE平均4回施行・血漿交換量1.3 PVが報告されているが、エビデンスレベルは低く、今後の前向き研究が求められる。5)
Tugulan C, Chang DD, Bates MJ. Heparin-Induced Thrombocytopenia After Mitral Valve Replacement. Ochsner J. 2021;21(1):100-104.
Attah A, Peterson C, Jacobs M, et al. Anti-PF4 ELISA-Negative, SRA-Positive Heparin-Induced Thrombocytopenia. Hematol Rep. 2024;16(1):90-97.
Pishko AM, Cuker A. Heparin-induced thrombocytopenia and cardiovascular surgery. Hematology Am Soc Hematol Educ Program. 2021;2021(1):478-485.
Mele M, Iacoviello M, Casavecchia G, et al. Coronary thrombosis due to heparin-induced thrombocytopenia after percutaneous coronary intervention. Clin Case Rep. 2021;9(6):e04291.
Adeoye O, Zheng G, Onwuemene OA. Approaches to management of HIT in complex scenarios, including cardiac surgery. Hematology Am Soc Hematol Educ Program. 2024;2024(1):267-278.