特発性頭蓋内圧亢進症 (IIH)は、明らかな原因なく頭蓋内圧が上昇する症候群であり、偽脳腫瘍とも呼ばれる。患者の約90%が女性で、肥満が最大のリスク因子である。
頭痛・一過性視覚暗転・乳頭浮腫 が主要な臨床像であり、治療が遅れると不可逆的な視力 障害に至ることがある。
診断には修正Dandy基準(Friedman 2013基準)を用い、MRI/MRV正常・脳脊髄液開放圧 >25 cmH₂Oが必須要件となる。
第一選択薬はアセタゾラミド であり、体重管理との組み合わせが治療の中核をなす。
糖尿病患者では糖尿病性乳頭炎との鑑別や、硝子体出血 による眼底評価困難など、管理上の特有の課題がある。
GLP-1受容体作動薬はIIHのICP低下効果が報告されているが、中断後の急激な体重増加でIIH発症を招くリスクもある。
特発性頭蓋内圧亢進症(idiopathic intracranial hypertension; IIH)は、明らかな原因なく頭蓋内圧(ICP)が上昇する症候群である。偽脳腫瘍(pseudotumor cerebri)とも呼ばれる。1893年にQuinckeが偽脳腫瘍症候群(pseudotumor cerebri syndrome; PTCS)として初めて記述した5) 。
診断には修正Dandy基準(Friedman 2013基準)を用いる。構造的病変の除外(MRI/MRV)、脳脊髄液(CSF)成分正常、開放圧 >25 cmH₂O が必須要件である3) 。
IIHの発生率は10万人あたり1〜2人である。有病率は増加傾向にあり、2015年から2022年にかけて10万人あたり7.3人から9.9人に上昇した。米国での年間発生率は10万人あたり1.15(1997〜2016年)で、女性1.97に対し男性は0.36と女性に著しく多い。15〜44歳の肥満女性では10万人あたり22.0にのぼり、患者全体の約90%が女性である。人種別では黒人2.05、白人1.04、ヒスパニック0.67、アジア/太平洋諸島民0.16(/10万人)と差異がある。
肥満は2型糖尿病とIIHに共通するリスク因子である。修正Dandy基準は糖尿病の併存を除外しない。2型糖尿病はラットモデルでICP上昇と関連することが示されており、代謝調節不全がIIH発症に寄与する可能性が指摘されている。ただし、糖尿病患者でのIIH有病率を直接検討した疫学研究は現時点では乏しい。
Q 糖尿病があるとIIHになりやすいのか?
A 肥満が糖尿病とIIH双方の共通リスク因子であり、間接的な関連が生じやすい。動物実験では2型DMがICP上昇と関連するとの報告があるが、糖尿病患者を対象とした直接的な有病率データは十分に蓄積されていない。
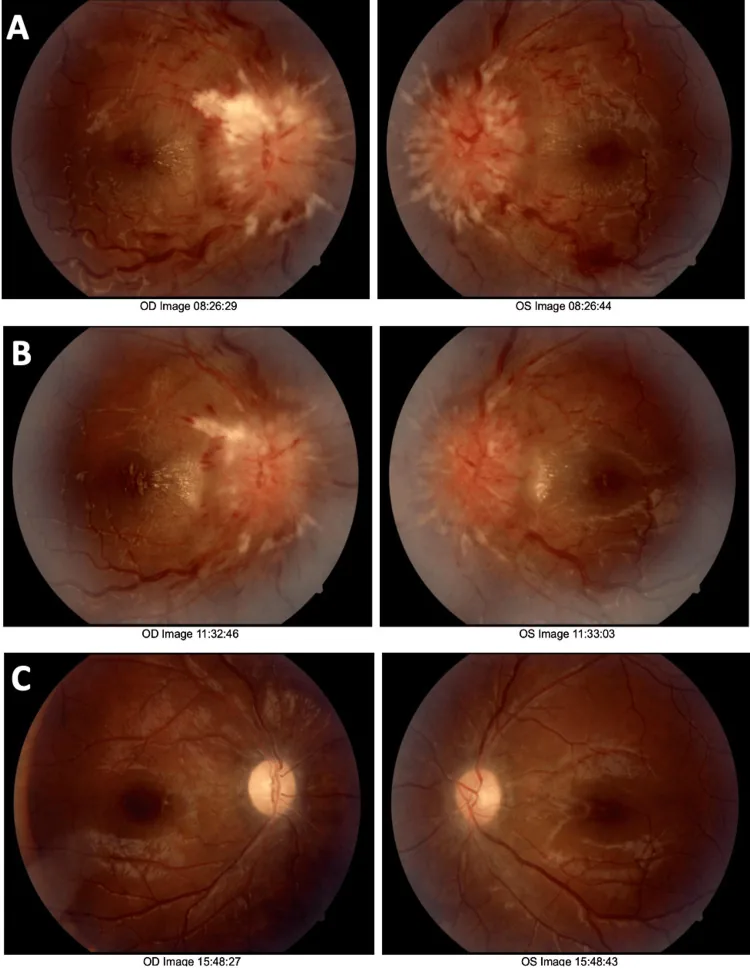
????????????????????? Sherilyn Nguyen, Nicholas Kato, Salomon D Salama. When One Tap Isn’t Enough: A Case of Pseudotumor Cerebri Requiring Venous Sinus Stenting. Cureus. 2025 Oct 17; 17(10):e94778. Figure 1. PMCID: PMC12619920. License: CC BY.
A????????????B?2?????????C?10???????????????????????????????????
頭痛 :最頻症状(約90%)。頭蓋内圧亢進型であり起床時に悪化しやすい。経過とともに慢性化し片頭痛 様に変化することがある。一過性視覚暗転(TVO) :68%に報告される。体位変換時などに生じる一過性の視覚消失を指す。拍動性耳鳴り :52%に認められる。背部痛 :53%に報告される。視力低下 :約33%で初発症状となる。乳頭浮腫に伴う視神経 障害が主因である。複視 劇症型特発性頭蓋内圧亢進症 視野欠損 を伴い、緊急対応を要する。
乳頭浮腫(papilledema) :IIHにおける視力障害の主因。重症度はFrisén分類で評価する4) 。外転神経(第6脳神経)麻痺 :IIH症例の9〜36%に認める1) 。視野障害 :盲点拡大・弓状暗点・周辺視野狭窄が典型的な所見である7) 。糖尿病性乳頭炎との鑑別 :糖尿病性乳頭炎は乳頭浮腫を模倣しうる。両側性の視神経乳頭浮腫を認めた場合は、IIHの可能性を検索する必要がある。硝子体出血(VH)による眼底評価困難 :増殖糖尿病網膜症 (PDR)に伴うVHが乳頭浮腫の評価を妨げることがある。
IIH発症に関わるリスク因子は代謝性要因と非代謝性要因に分類できる。
代謝性リスク因子
肥満 :最大のリスク因子。体格指数(BMI)30 kg/m²超でリスク増加。体格指数 >40 kg/m²では不可逆的視力障害リスクが顕著に増加する。
中心性肥満 :末梢性肥満よりICP上昇リスクが高い可能性がある。体幹脂肪と脳脊髄液圧の相関がDEXA scanningによる研究で示された2) 。
急激な体重増加 :GLP-1受容体作動薬(GLP-1RA)中断後に急速に体重が回復しIIHを発症した症例報告がある2) 。
2型糖尿病 :肥満を介した間接的関連が示唆される。代謝調節不全がIIHに寄与する可能性がある。
多嚢胞性卵巣症候群(PCOS) :IIHの認知された関連疾患である。
非代謝性リスク因子
女性・妊娠可能年齢 :患者の約90%が女性であり、発症の大部分を占める。
薬剤性 :テトラサイクリン系抗菌薬、ビタミンA誘導体(レチノイド)、成長ホルモン、リチウムが関連薬剤として知られる。
全身性エリテマトーデス (SLE)8) 。
閉塞性睡眠時無呼吸(OSA) :IIHの関連疾患として認識されている。
遺伝的素因 :家族性IIHの報告があり、染色体5・13・14に候補領域が特定されている。AQP1遺伝子多型がCSF産生増加に関与する可能性が示唆されている7) 。
感染・炎症との関連も報告されており、直近の感染または炎症性疾患でIIHリスクが約3倍に増加するとの疫学研究がある6) 。
体重管理が最も重要です。体重の3〜15%の減量でIIH寛解との関連が報告されています。
糖尿病患者では血糖コントロールと体重管理を並行して行うことが重要です。
GLP-1受容体作動薬を使用している場合は、医師の指示なく突然中断しないでください。急激な体重増加がIIH発症のリスクになります。
Q 急激な体重変動はIIHにどう影響するか?
A 急激な体重増加はIIH発症リスクを高める。GLP-1RAを中断した後にBMIが29から34へ急増しIIHを発症した症例が報告されている2) 。一方、体重減少はIIH寛解と関連し、治療の中核をなす。
IIHの確定診断には以下の基準をすべて満たす必要がある3) 5) 。
要件 内容 A 乳頭浮腫の存在 B 頭蓋神経異常以外の局所神経所見なし C MRI(±造影)で正常脳実質 D CSF成分正常 E LP開放圧 >25 cmH₂O(成人)
非典型例ではMRV(磁気共鳴静脈撮影)を追加する。
造影MRI + MRV :構造的病変および脳静脈洞血栓症 (CVST)の除外に必須。頭蓋内圧亢進の画像所見 :眼球後極部平坦化、視神経鞘内髄液貯留、空洞鞍(empty sella)、横静脈洞狭窄がみられる。糖尿病性腎症によるGd制限 :GFR低下例ではガドリニウム造影剤の使用が制限される場合がある。
側臥位で実施する。開放圧 >25 cmH₂Oが異常値であり、25〜30 cmH₂Oはグレーゾーンと判定される。CSF中の糖値は血清血糖値と対比させて評価することが重要である。
眼底検査 4) 。光干渉断層計 (OCT)網膜神経線維層 (RNFL)厚を定量評価し、偽乳頭浮腫との鑑別に有用である4) 。視野検査 (Humphrey 30-2)7) 。眼窩 超音波検査牽引性網膜剥離 の除外にも有用である。
脳静脈洞血栓症(CVST) :臨床像がIIHに酷似するため、MRVによる除外が必須4) 。糖尿病性乳頭炎 :乳頭浮腫を模倣する。両側性の場合はIIHの検索を行う。薬剤性頭蓋内圧亢進 :テトラサイクリン系・ビタミンA過剰・リチウムなどの服用歴を確認する。貧血 :乳頭浮腫患者の約10%に鉄欠乏性貧血が認められるとされ、スクリーニングを要する。
Q 硝子体出血がある場合、IIHはどう診断するか?
A 重度の硝子体出血は眼底観察を妨げ、乳頭浮腫の評価を困難にする。この場合、眼窩超音波検査で乳頭浮腫を検出できるほか、MRI/MRVで頭蓋内圧亢進の放射線学的所見を確認する方法が有用である。
主要な薬剤の特徴を以下に示す。
薬剤 機序 主な用量 アセタゾラミド 炭酸脱水酵素阻害 250〜500 mg×2/日、最大4 g/日 トピラマート 弱い炭酸脱水酵素阻害 個別調整 フロセミド ループ利尿 補助的使用
アセタゾラミド(第一選択) :脳脊髄液産生を減少させる炭酸脱水酵素阻害薬 。開始用量は250〜500 mg 1日2回とし、1日2〜4 gに漸増する。2014年のIIHTT(特発性頭蓋内圧亢進症 Treatment Trial)では、アセタゾラミド+体重減少療法が軽〜中等度の視野障害を有する特発性頭蓋内圧亢進症で有効であり、4 g/日まで安全性・忍容性が確認された。主な副作用は感覚異常・味覚障害(金属味)・悪心・嘔吐・倦怠感・腎結石である。トピラマート :弱い炭酸脱水酵素阻害作用を持ち、片頭痛様頭痛の併存治療にも有用。アセタゾラミド不耐時の代替として使用する3) 。フロセミド :ループ利尿薬として補助的に使用される3) 。
体重管理は特発性頭蓋内圧亢進症管理の中核をなす。体重の3〜15%減少で特発性頭蓋内圧亢進症寛解との関連が報告されている。頭蓋内圧正常化に必要な減量は体重の24%に相当するとされ、肥満外科手術でのみ達成可能な水準である。特発性頭蓋内圧亢進症 Weight Trial(IIHWT)では、体格指数 ≥35 kg/m²の特発性頭蓋内圧亢進症患者において肥満外科手術が2年間にわたる持続的なICP低下と体重減少をもたらすことが実証された。糖尿病合併例ではHbA1cの同時低下が期待でき、糖尿病寛解にも寄与しうる。
視神経鞘開窓術(ONSF) :乳頭浮腫による視力低下が主徴で頭痛が軽微な場合に推奨。視神経鞘に脳脊髄液排出用の開窓を作成する3) 。脳脊髄液シャント術 :脳室腹腔シャント(VPS)または腰椎腹腔シャント(LPS)。乳頭浮腫+視力低下の重症例に適応となる1) 。VP shunt後に随伴した三叉神経 痛が完全寛解した報告がある1) 。静脈洞ステント留置術 :横静脈洞狭窄を有するIIHに対し、頭痛・視力改善率が高い。内科治療抵抗例への外科的介入として認知度が上昇している。糖尿病患者固有の考慮 :PDR+VH合併例では硝子体 切除術(PPV )で後極部を観察可能にし、乳頭浮腫の評価・モニタリングを行う必要がある。
アセタゾラミド使用中は電解質(特にカリウム)の定期的なモニタリングを推奨する。慢性代償性代謝性アシドーシスを生じうる。
アセタゾラミドの認知機能への副作用が報告されており、長期使用時は注意を要する。
劇症型IIHでは治療遅延が不可逆的視力障害につながるため、緊急に対応する必要がある。
Q GLP-1受容体作動薬はIIHの治療に使えるか?
A GLP-1RAはIIH治療への応用が研究されており、エキセナチドがヒトで投与後2.5時間でICPをベースラインから5.7±2.9 cmH₂O低下させたとの報告がある。しかし現時点では標準治療として確立されておらず、研究段階の介入である。また、GLP-1RAを突然中断すると急激な体重増加を来してIIHを発症するリスクがあることに注意を要する2) 。
IIH発症に関する主要な病態仮説は以下の通りである。
CSF動態異常
CSF産生増加 :脈絡叢でのCSF産生が亢進する機序が提唱されている。
CSF排出障害 :くも膜顆粒での吸収障害がICP上昇の一因となる可能性がある。
レプチンの関与 :IIH患者のCSF中レプチン値が上昇している。脈絡叢にレプチン受容体が存在し、CSF産生に関与する可能性が示唆されている2) 。
GLP-1受容体 :脈絡叢にGLP-1受容体が存在し、GLP-1RAがCSF産生を減少させることがラットモデルで示されている2) 。
静脈還流障害
中心性肥満による機序 :腹腔内圧上昇→胸腔内圧上昇→脳静脈還流障害→頭蓋内静脈圧上昇というカスケードが提唱されている。
静脈洞狭窄 :横静脈洞の両側性狭窄と高い静脈圧勾配が病態に関与する1) 4) 。原因か結果かは議論が続いている。
限界 :この仮説は非肥満患者のIIHを説明できない。
内分泌・代謝機能障害 :CSF中のアンドロゲンレベルの異常が検出されており、PCOSなどの内分泌疾患がCSF分泌に影響する可能性がある。糖尿病との関連メカニズム :2型DMはラットモデルでICP上昇と関連する。内分泌・代謝調節不全がIIH発症に寄与しうる。遺伝的要因 :家族性IIHの報告がある。染色体5・13・14に候補領域が同定されており、AQP1遺伝子多型による脈絡叢でのCSF産生増加が仮説として提唱されている。常染色体優性遺伝 のパターンが示唆されている7) 。ビタミンA :過剰摂取との関連が示唆されているが、現時点では証明されていない。
エキセナチドはラットモデルおよびヒトでICPを低下させることが報告されている。
ヒトへの投与後2.5時間でICPがベースラインから5.7±2.9 cmH₂O低下した(P=0.048)。頭痛軽減効果も確認され、アセタゾラミド減量につながることが示唆されている。GLP-1RAはCSF産生減少・脂肪組織の脂肪分解・体重減少を通じてIIHを改善しうると考えられている2) 。
一方、GLP-1RAの突然中断によってICPが急上昇しIIHを発症するリスクがあることも示された。デュラグルチドを中断した後にBMIが急増してIIHを発症した症例では、GLP-1RAがIIHを抑制していた可能性が示唆されている2) 。
Sundholm(2020)らの疫学研究では、直近の感染または炎症性疾患によってIIHリスクが約3倍に増加することが報告された6) 。COVID-19感染後にIIHを新規発症した症例報告も蓄積されており6) 、感染・免疫応答がIIH発症に関与するメカニズムの解明が課題である。
家族性非肥満IIHの症例において、AQP1遺伝子多型が脈絡叢でのCSF産生増加に関与するという仮説のもと、研究が進行中である7) 。IIHにおける遺伝的素因の解明は、病態理解と新規治療標的の同定につながることが期待されている。
Ali A, Al-Sairafi A, Bida A, Attieh M, Al-Kandari A. Debilitating trigeminal neuralgia secondary to idiopathic intracranial hypertension: a case report and review of the literature. Heliyon. 2023;9(9):e19985.
Heckel B. Idiopathic intracranial hypertension after abrupt cessation of medication: a case report of abrupt GLP-1 receptor agonist cessation and review of the literature. Curr Pain Headache Rep. 2024;28(6):519-527.
Kwak M, Chaudhry MA, Weidler EM, Rouse B. Pseudotumor cerebri with blindness: a case report. Cureus. 2021;13(2):e13268.
Remolí Sargues L, Martínez-Costa L, Ruiz-Hernández C, Cervera-Taulet E. Incidental idiopathic intracranial hypertension in an older non-obese male. Rom J Ophthalmol. 2021;65(3):281-285.
Del Monte F, Iannella G, Russo FP, et al. Infantile idiopathic intracranial hypertension: case report and review of the literature. Ital J Pediatr. 2022;48(1):11.
Sriuoginys S, Haffar A, Joseph N. De novo presentation of idiopathic intracranial hypertension (IIH) associated with COVID-19 infection. Neurohospitalist. 2022;12(3):489-493.
Behbehani R, Almutairi A, Alroughani R, Alrashidi S, Alansari N. Familial non-obese idiopathic intracranial hypertension. Am J Ophthalmol Case Rep. 2022;27:101639.
Almalki A, Alsabah B, Aldhaheri W, et al. Idiopathic intracranial hypertension as the initial manifestation of systemic lupus erythematosus: a case report and literature review. Am J Case Rep. 2025;26:e946258.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください