VEP
視覚誘発電位(VEP):P100潜時の延長を検出する。エタンブトール服用患者の34.8%でP100が107 ms以上に延長したとの報告がある2)。潜在的な視神経損傷の検出に有用だが、EONに特異的ではない。

エタンブトール(EMB)はマイコバクテリウム属、特に結核菌(Mycobacterium tuberculosis)やマイコバクテリウム・アビウム・コンプレックス(MAC)などの非結核性抗酸菌症に対して使用される第一選択薬である。EMBの最も重大な副作用がエタンブトール視神経症(ethambutol optic neuropathy: EON)であり、薬物性視神経症のなかで発症頻度が常に上位を占める。
結核治療を受ける患者におけるEONの有病率は1〜2%と推定される。世界保健機関(WHO)によれば毎年約920万人の結核新規症例が報告されており、年間最大10万人のEON新規症例が発生する可能性がある。
EONのリスクは高度に用量依存的である。EMB投与量別の推定有病率を以下に示す。
| EMB投与量 | 推定有病率 |
|---|---|
| <15 mg/kg/日 | 1%未満 |
| 25 mg/kg/日 | 5〜6% |
| >35 mg/kg/日 | 18〜33% |
ただし、低用量(<15 mg/kg)であってもEONの発症は報告されている。日本の全国調査ではEON症例の52.2%が低用量で発症しており、真に「安全」な用量は存在しない3)。
2009年にWHOが結核治療の維持期にもEMBを含めるよう指針を改訂し、投与期間が延長された。この変更に伴いEON発症リスクの増大が懸念されている1)。
結核治療患者の約1〜2%に発症する。用量が高いほどリスクは上昇し、25 mg/kg/日で5〜6%、35 mg/kg/日超で18〜33%に達する。低用量でも発症しうるため、真に安全な用量は存在しない。詳細は「エタンブトール視神経症とは」の項を参照。
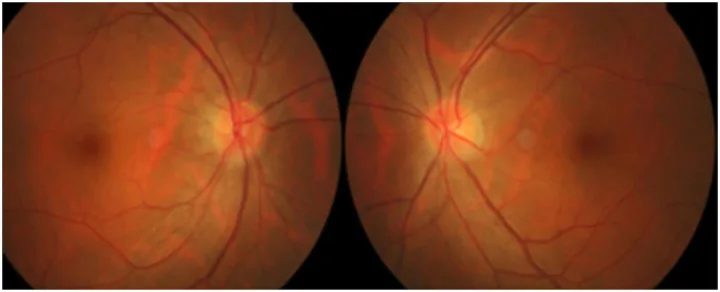
EONは他の中毒性視神経症とは異なり、治療開始後比較的短期間で発生しうる。発症時期は服用開始から1ヶ月〜36ヶ月と幅広いが、2ヶ月以内では起こりにくく平均7ヶ月である。
主な自覚症状は以下のとおりである。
色覚異常が最初の兆候となることがある。赤色が以前より鮮明に見えないといった自覚が手がかりとなる。両眼の視力低下は潜行性に進行するため、定期的な視力・色覚チェックが早期発見に重要である。
EMBの神経毒性の正確な機序は不明だが、金属キレート作用が主因と考えられている。EMBとその代謝物である2,2-エチレンジアミノジブチル酸(EDBA)はいずれもキレート物質であり、以下の経路で視神経障害を惹起するとされる2)。
動物実験では亜鉛欠乏が髄鞘の破壊とグリア細胞の増殖に関連することが示されている。ヒトにおいてもEMBの長期使用によるビタミンE・B1欠乏が視神経症を悪化させる可能性がある。
エタンブトール、リネゾリド、メサラジンなどの薬物性視神経症は後天性ミトコンドリア機能異常によるものと考えられており、遺伝性のLeber遺伝性視神経症と病態が類似する。
高用量・長期間の服用、65歳以上の高齢者、腎機能障害、高血圧、糖尿病、喫煙者、イソニアジド併用者がリスク因子として知られる。詳細は「原因とリスク要因」の項を参照。
EONの診断は臨床的に行われる。投与前のベースライン検査が不可欠であり、スクリーニングとしてEMB投与前に視力、視野検査、中心フリッカ値、色覚検査を施行し、投与中も1〜2ヶ月に1回チェックすることが望ましい。
VEP
視覚誘発電位(VEP):P100潜時の延長を検出する。エタンブトール服用患者の34.8%でP100が107 ms以上に延長したとの報告がある2)。潜在的な視神経損傷の検出に有用だが、EONに特異的ではない。
OCT
光干渉断層計(OCT):乳頭周囲網膜神経線維層(pRNFL)の菲薄化や神経節細胞層-内網状層(GCIPL)の変化を検出する。耳側優位の変化が特徴的で、20〜79%の減少が報告されている2)。視力予後の評価にも有用である。
EMBを中止しても視力低下が進行する場合は他の視神経症を考慮する必要がある。
EONに対する確立された治療法は存在しない。原因薬剤の中止に勝る治療法はなく、EONが疑われた場合は速やかにEMBを中止することが最も重要な対応である。眼科医はEMBを中止する前に処方医に直接連絡する必要がある。
EMB中止後も2〜3ヶ月程度は視力および視野障害が進行することがある。その後徐々に回復に向かうが、回復は半年〜2年と緩徐である。
喫煙はシンナー中毒やEONにおいても相加的な悪影響を及ぼすため中止させるべきである。高血圧や糖尿病など血流に影響を及ぼす基礎疾患がある場合は、内科と連携して治療を行う。
| 予後因子 | 影響 |
|---|---|
| 早期発見・早期中止 | 30〜64%で視力改善 |
| 60歳未満 | 回復率約80% |
| 60歳以上 | 回復率約20% |
視力が回復する患者ではスネレン視力表で平均2行分の改善がみられる2)。一方で、視力が完全に回復する患者もいれば、永久的な視機能障害が残る患者もいる。発症時に視神経乳頭蒼白が存在する場合は予後不良と関連する。
EMB中止後もRNFL厚の減少が持続するとの報告があり、不可逆的な視力喪失は綿密なモニタリングと速やかな薬剤中止にもかかわらず生じうる2)。
不可逆的な視神経萎縮が生じる前にEMBを中止すれば、30〜64%の患者で視機能が改善する。ただし完全回復は稀であり、平均的な改善はスネレン2行分である。中止後も2〜3ヶ月は症状が進行することがあるため、継続的なフォローアップが必要である。詳細は「標準的な治療法」の項を参照。
球後視神経症がEONの最も一般的な形態であり、発症時に視神経乳頭は正常に見える。
EMBとその代謝物EDBAはいずれも金属キレート物質として作用する。EDBAはエタンブトール自体より眼内クリアランスが低く、局所濃度が高くなるため毒性への寄与が大きいと推定されている2)。
障害の主な経路は以下のとおりである。
乳頭黄斑線維束(papillomacular bundle)を構成するparvo-cellular axonsは、ミトコンドリアのエネルギー需要が特に高い。このため中毒性・栄養障害性視神経症ではこれらの軸索が優先的に障害される2)。
網膜神経節細胞のなかでもATP消費の激しいp細胞が優位に障害されると推定されており、中心暗点の形成機序と一致する。一方、対光反応に関与するγ細胞は保存されるため、対光反応は比較的維持される。
動物実験ではEMBによる軸索性神経症は視交叉に起こりやすいとされ、臨床的に両耳側半盲を呈する症例の存在と合致する。
Sabhapanditら(2023)は2010〜2021年に発表された12研究(5818人、うち309人がEON)の系統的レビューを行い、2ヶ月を超えるEMBの延長使用が有意な視神経毒性をもたらすことを報告した1)。EMB中止後の視力改善は統計的に有意であった(P = 0.035)。色覚異常および視野異常の改善は有意水準に達しなかった。
Matsumotoら(2021)は、低用量EMB(12 mg/kg)・短期間(2.5ヶ月)の投与にもかかわらずEMB中止後に急激に視力が悪化し、不可逆的視力喪失に至った85歳男性の症例を報告した3)。中止前は20/17であった矯正視力が3週間で20/330(右眼)・20/1000(左眼)に低下した。この症例は、低用量であっても壊滅的な視力喪失が起こりうることを示している。
Peterson & Hawy(2022)は、MAC治療中に<15 mg/kg/日のEMBを3年間服用した82歳男性で遅発性EONを発症した症例を報告した4)。EMB中止後に視力は改善し、10ヶ月後も改善が持続した。発症の中央値は9ヶ月とされるが、3年以上経過してからの発症もありうることが示された。
Konanaら(2024)は、エタンブトール毒性による錐体機能障害の3症例を報告した5)。光過敏と視力低下を主訴とし、網膜電図でフリッカー応答の潜時遅延を認めた。エタンブトール毒性は視神経のみならず網膜細胞層にも影響を及ぼすことを示唆する報告である。
固定用量配合錠(FDC:1錠にイソニアジド、リファンピシン、ピラジナミド、エタンブトールを含有)の導入と投与期間延長により、EON発症の増加が予想されている2)。スクリーニング体制の整備、OCT・VEPの潜在性EON検出における有用性の検証、EONの発症機序の解明とリスク因子の特定が今後の重要な研究課題である。