暗所で顕著な不同
**交感神経障害(Horner症候群)**を示唆する。患眼側の瞳孔散大が不十分となり、暗所で健眼との差が拡大する。
散瞳遅延(dilation lag):暗室に入っても患眼側の瞳孔が遅れて広がる。
三徴:中等度縮瞳・軽度眼瞼下垂・見かけ上の眼球陥凹(瞼裂狭小)。対光反射は正常だが縮瞳後の散瞳が遅延する。
顔面発汗低下:節後性病変では患側の顔面・前額部の発汗が低下する。

瞳孔不同(Anisocoria)とは、左右の瞳孔径が異なる状態の総称である。瞳孔径の左右差が0.4mm以上の場合に定義されることもある5)。
正常人の約20%に生理的瞳孔不同が存在し、一般集団での有病率は約19%と報告されている4)。生理的瞳孔不同では左右差は通常1mm以下であり、明所・暗所の両条件で差がほぼ一定で、対光反射・輻湊反応は正常に保たれる。
原因の大分類として、以下の2系統が重要である。
瞳孔不同の原因は良性の生理的なものから、生命を脅かす脳動脈瘤・頸動脈解離・脳卒中まで多岐にわたるため、適切な鑑別が不可欠である。
正常人の約20%に生理的瞳孔不同があり、左右差が1mm以下で対光反射が正常なら多くは問題ない。しかし急性発症の場合や、頭痛・眼瞼下垂・複視・しびれ・脱力を伴う場合は緊急の精査が必要である。
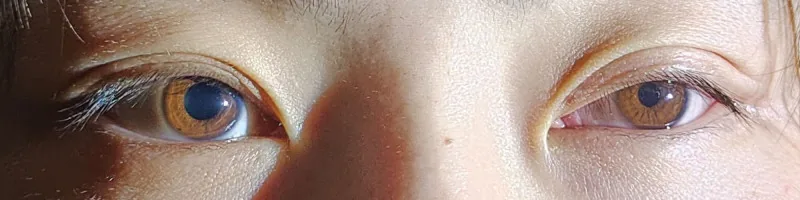
単独の瞳孔不同は無症状のことが多い。患者が気づく主な症状は以下の通りである。
明所・暗所での瞳孔径の変化が、障害部位の特定に不可欠である。
暗所で顕著な不同
**交感神経障害(Horner症候群)**を示唆する。患眼側の瞳孔散大が不十分となり、暗所で健眼との差が拡大する。
散瞳遅延(dilation lag):暗室に入っても患眼側の瞳孔が遅れて広がる。
三徴:中等度縮瞳・軽度眼瞼下垂・見かけ上の眼球陥凹(瞼裂狭小)。対光反射は正常だが縮瞳後の散瞳が遅延する。
顔面発汗低下:節後性病変では患側の顔面・前額部の発汗が低下する。
明所で顕著な不同
副交感神経障害を示唆する。患眼側が散瞳したままとなり、明所で健眼との差が拡大する。
Adie瞳孔:中等度散大・脱円。分節状の虹彩麻痺と虫様運動(vermiform movement)が特徴。対光反射は欠如または微弱だが、近見反応は緩徐に保存される(対光-近見反応解離)。
動眼神経麻痺:眼瞼下垂・外下方偏位・調節障害を伴うことが多い。瞳孔散大を伴う動眼神経麻痺では動脈瘤の頻度が高い。
薬剤性散瞳:散大・固定した瞳孔で高濃度ピロカルピン(1〜2%)に無反応。
薬剤が直接・間接的に眼に作用することで散瞳または縮瞳が生じる。外用薬・経口薬・経皮薬など投与経路を問わず起こりうる点が特徴である。
以下に主な薬剤とその特徴を示す。
| 薬剤 | 経路 | 特記事項 |
|---|---|---|
| グリコピロレート錠 | 経口(CL経由) | 微粒子がCLに付着し片眼に転移1)。散瞳は最大1週間持続 |
| Qbrexza(グリコピロニウム)ワイプ | 外用 | 不適切な手指衛生で眼に接触し瞳孔径8mm2) |
| スコポラミン経皮パッチ | 経皮 | 指を介し眼へ接触。散瞳効果は最大2週間持続4) |
| アゼラスチン0.5%点眼 | 局所 | H1抗ヒスタミン薬にもかかわらず散瞳。中止72時間で回復3) |
| イプラトロピウム臭化物ネブライザー | 吸入 | マスク不適切装着で眼へ暴露。中止12時間で回復7) |
| スコポラミン粉末(実験室) | 吸入・接触 | 散瞳+頻脈・めまい。ピロカルピン無効、5日で回復4) |
その他、アトロピン・トロピカミド・シクロペントラート・フェニレフリン・アドレナリンなどの点眼薬も散瞳を起こす。キダチチョウセンアサガオ(Angel’s trumpet;アトロピン・スコポラミン・ヒヨスチアミンを含有)は草刈り時の吸入暴露でも散瞳を起こしうる7)。縮瞳を起こす薬剤としてはピロカルピン・ブリモニジン・プロスタグランジン製剤・オピオイド・有機リン系殺虫剤などがある。
外傷性散瞳(虹彩根部離断)、急性閉塞隅角緑内障発作後の麻痺性散瞳、ぶどう膜炎による虹彩後癒着など。
抗ヒスタミン点眼薬(アゼラスチンなど)3)、乗り物酔い用スコポラミン経皮パッチ4)、多汗症治療用グリコピロニウムワイプ2)などで薬剤性散瞳が報告されている。いずれも原因薬剤を中止すれば自然回復するが、医師への申告が重要である。
明室と暗室の両条件での瞳孔径測定が最も重要な検査である。瞳孔の正常径は室内で平均4mm程度(2〜6mmと個人差がある)。乳幼児は2〜2.5mmと小さめで、高齢者は縮瞳気味である。
以下に主な薬剤試験の目的と判定を示す。
| 薬剤 | 目的 | 判定のポイント |
|---|---|---|
| アプラクロニジン(0.5〜1%) | Horner症候群の確認 | 健眼縮瞳・患眼散瞳→瞳孔不同逆転。感度88〜100%。若年児では禁忌 |
| コカイン(4〜10%) | Horner症候群の確認 | 正常眼散大・Horner眼不動→不同拡大 |
| ヒドロキシアムフェタミン(1%) | 節後性vs中枢・節前性の鑑別 | コカイン/アプラクロニジン施行48時間後に施行 |
| 低濃度ピロカルピン(0.1〜0.125%) | Adie瞳孔の確認 | 脱神経過敏性により縮瞳。正常瞳孔は不動 |
| 高濃度ピロカルピン(1〜2%) | 薬剤性散瞳vs動眼神経麻痺の鑑別 | 縮瞳→動眼神経麻痺、無反応→薬剤性散瞳1)4) |
| フェニレフリン(1%) | Horner症候群(節後性)の確認 | 脱神経過敏性により患眼のみ散瞳 |
虹彩括約筋裂傷・虹彩萎縮・ぶどう膜炎徴候の有無、Adie瞳孔の分節状虹彩麻痺・虫様運動を観察する。
薬剤試験が曖昧な場合、または動脈瘤・解離・腫瘍の臨床的疑いがある場合に施行する。急性Horner症候群では薬剤試験を省略して画像検査へ直接進むことが適切である。MRI/MRAはCT/CTAより頸動脈海綿静脈洞瘻検出に有用であり、3D time-of-flight MRAが静脈洞内の流速信号検出に優れる6)。
まず明所と暗所の両条件での瞳孔径計測が最重要である。次いで対光反射・近見反応を確認し、目的に応じた薬剤点眼試験(アプラクロニジン、ピロカルピンなど)で原因を絞り込む。動脈瘤・解離など緊急疾患が疑われる場合は薬剤試験を待たず頭部MRI/MRAを施行する。
治療の最優先事項は、後交通動脈瘤・頸動脈解離・急性閉塞隅角緑内障など緊急性の高い基礎疾患の除外と適切な治療である。
良性・生理的
生理的瞳孔不同:治療不要。経過観察のみ。
Adie瞳孔:良性で自然回復傾向あり(経過とともに縮瞳傾向)。羞明が強い場合は低濃度ピロカルピン(0.125〜0.25%)点眼や遮光眼鏡・虹彩付きコンタクトレンズを使用する。調節障害には近用眼鏡の装用が有用。
薬剤性瞳孔不同:原因薬剤の中止により自然消失。コンタクトレンズ使用者に抗コリン薬を処方する際は手指衛生の徹底を指導する1)2)。
神経疾患
Horner症候群:基礎疾患(頸動脈解離・パンコースト腫瘍等)の治療が優先。良性原因では経過観察。
動眼神経麻痺:後交通動脈瘤による圧迫性病変は緊急手術の適応。糖尿病性では糖尿病の治療が優先。良性原因は経過観察。
頸動脈海綿静脈洞瘻(硬膜動静脈瘻):経静脈的コイル塞栓術。後方ドレナージ型頸動脈海綿静脈洞瘻による動眼神経麻痺の自然回復は10〜73%で報告6)。
眼局所・構造
先天無虹彩症:虹彩付きカラーコンタクトレンズや遮光眼鏡で羞明を軽減。まれに人工虹彩移植術の適応となる。
機械的瞳孔不同:虹彩根部離断・ぶどう膜炎後癒着など。構造的欠陥の修正手術が必要な場合がある。
Adie瞳孔は良性疾患で自然回復傾向があるため、無症状なら経過観察のみでよい。羞明が強い場合は低濃度ピロカルピン点眼やサングラス・遮光眼鏡で症状を軽減できる。ただし、Adie瞳孔の背景にFisher症候群・神経梅毒など全身疾患が隠れていないかの確認は必要である。
交感神経は3次ニューロンで構成される。
副交感神経は対光反射に関わる求心路と遠心路からなる。
調節線維が瞳孔括約筋線維の95倍存在するという構造的非対称性が、毛様体神経節障害後の異常再支配と対光-近見反応解離の病態の基盤となる。
近見反応のEW核への核上性線維は対光反射の求心線維が通る中脳視蓋前域より腹側を走行するため、視蓋前域の障害では対光反射と近見反応の解離(Argyll Robertson瞳孔)が生じる。
毛様体神経節または短毛様体神経の損傷→異常再生→コリン受容体のアップレギュレーション(脱神経過敏性)が生じる。調節線維(95%)が瞳孔括約筋を異常再支配するため、近見刺激への反応は保存されるが対光反射は微弱となる(対光-近見反応解離)。また脱神経過敏性により、低濃度ピロカルピン(0.1〜0.125%)に対して正常瞳孔は反応しないが、Adie瞳孔は収縮する。
静脈叢圧上昇による海綿静脈洞外側壁への動眼神経圧迫・静脈うっ滞・血管盗血が複合的に関与する6)。動眼神経は海綿静脈洞外側壁に沿って走行するため静脈拡張による圧迫を受けやすく、三叉神経第1枝が動眼神経の神経上膜に沿って走行することで有痛性となる6)。
多汗症治療薬グリコピロレートには、従来錠に加えて口腔内崩壊錠(Dartisla ODT)が開発されている。
Adamkiewiczら(2024)は、口腔内崩壊錠は従来錠より速く崩壊するため、薬剤微粒子による眼への直接接触リスクがより高い可能性を指摘している1)。コンタクトレンズ装用者に経口抗コリン薬を処方する際の手指衛生指導の徹底が、薬剤性瞳孔不同の予防に重要との提言がなされている。
Qbrexza(グリコピロニウムトシル酸塩ワイプ)は2018年FDA承認の比較的新しい薬剤であり、医師間での認知不足が不要な神経画像検査の施行につながる可能性がある。
Sasherら(2024)は2症例を通じ、薬剤歴の詳細な聴取なしに瞳孔不同患者に神経画像検査を行うことで生じる患者負担・コスト・医療資源の不必要な消費を強調した2)。多汗症治療薬を使用している患者での突然発症の瞳孔不同では、まず薬剤性を疑うべきと提言している。
標準的な薬剤性散瞳の診断フローでは、高濃度ピロカルピン(1〜2%)に無反応であれば薬剤性散瞳を示唆するとされる。しかしスコポラミンによる散瞳では非典型的反応が報告されている。
Liら(2025)は、スコポラミン経皮パッチによる薬剤性散瞳例においてピロカルピン(1〜2%)点眼後に一時的な縮瞳が得られた後に再散瞳した症例を報告した4)。この知見は、薬剤性散瞳の診断においてピロカルピン試験が常に信頼できるわけではなく、詳細な薬剤歴聴取が不可欠であることを示唆する。
全身麻酔下では麻薬・筋弛緩薬などの薬剤効果により瞳孔所見の解釈が困難となる。
Haradaら(2023)は、術前に未診断だったAdie瞳孔が全身麻酔導入後に偶然発見され、脳血管障害疑いで手術が中止された症例を報告した5)。術前の全身評価に標準的な瞳孔検査を組み込むことで、麻酔下での不要な手術中止を防げる可能性があると提唱している。