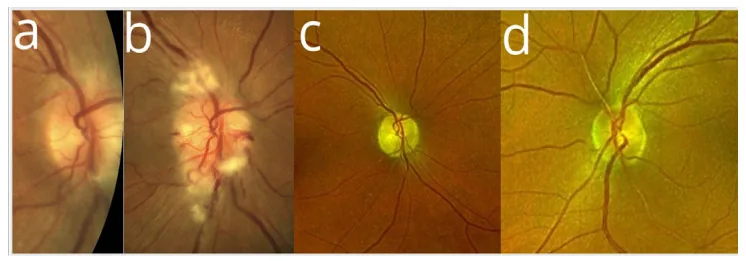
アミオダロン関連視神経症(AAO N)は抗不整脈薬アミオダロン服用中に発症する視神経 障害で、発生率は0.3〜2%と推定される。
最も一般的な眼副作用は渦状角膜 変性(70〜100%)だが、視神経症は最も深刻な眼副作用である。
潜行性の発症と遷延する乳頭浮腫 (中止後も最大15か月持続)が特徴で、非動脈炎性前部虚血性視神経症 (NAION)との鑑別が臨床上の最大の課題となる。
患者の約1/3は無症状であり、定期的な眼科モニタリングが重要である。
治療は被疑薬中止が原則だが、致死的不整脈の治療薬であるため循環器科との連携が必須となる。
アミオダロン中止後、視力 改善は58%にとどまり、21%はさらに悪化、20%は法的盲(20/200未満)に至る。
アミオダロンは1960年代に狭心症治療薬として開発されたジヨード化ベンゾフラン誘導体である。クラスIII抗不整脈薬として分類されるが、クラスI・II・IVの特性も併せ持つ1) 。心房細動・心室頻拍・心室細動に広く処方され、日本では商品名アンカロン(海外ではCordarone、Pacerone等)として知られる。
アミオダロンは経口バイオアベイラビリティ30〜80%、半減期20〜100日と極めて長い。脂溶性が高く脂肪組織に蓄積し1) 、肝CYP3A4/CYP2C8で代謝されて活性代謝物desethylamiodarone(DEA)を生成する1) 。
アミオダロンは複数の眼副作用を引き起こす。
渦状角膜変性(verticillate keratopathy) :最も一般的な眼副作用。角膜上皮 深層に褐色の渦状色素沈着として出現し、投与患者の2/3に発症する。投与量・投薬期間と相関し、高用量(400 mg/日)ではほぼ100%に出現する。Orlando分類grade I〜IVで評価される。渦状角膜変性のみであれば通常アミオダロン継続可能である。アミオダロン関連視神経症(AAON) :最も深刻な眼副作用。発生率は0.36〜2%と報告されている。その他 :前嚢下水晶体 混濁、多発性霰粒腫 、ドライアイ 等。
また、甲状腺機能障害・肺毒性(過敏性肺炎、致死的となりうる)・末梢神経障害・光線過敏症など多様な全身副作用も有する。
台湾国民健康保険データベースを用いたChengらのコホート研究(アミオダロン投与群6,175人 vs 対照24,700人)では、アミオダロン投与群の0.3%に視神経症が認められ、非投与群(0.1%)に対してハザード比2.09(95%CI 1.13〜3.85)と報告された1) 。
Q アミオダロンを服用するとどのくらいの確率で視神経症になるのか?
A 台湾のコホート研究ではアミオダロン服用者の0.3%に視神経症が認められ、非服用群と比較してハザード比2.09と報告されている1) 。後方視的報告では0.36〜2%の発生率が示されており、前向き二重盲検試験(1,600人超)での最大推定年間発生率は0.23〜0.74%であった1) 。
????????????????? Dina Lešin Gaćina et al. Is Semaglutide Linked to NAION? A Case Report on a Rare Ocular Complication. Reports. 2025 Aug 20; 8(3):149. Figure 1. PMCID: PMC12372079. License: CC BY.
???????????????????????????????????????????????????????????????????????????
視力低下 :急性または潜行性に発症する。単眼性・両眼性いずれも起こりうる。296例のレビューでは44%が潜行性発症であった。急性単眼性19%、潜行性単眼性26%、急性両眼性10%、潜行性両眼性14%の内訳が報告されている。無症状 :AAON患者の最大1/3は自覚症状がない。乳頭浮腫のみで発見されることも多い。色覚異常 (dyschromatopsia)
AAONの主要な臨床所見を以下に示す。
視神経乳頭浮腫 :症例の85%で認められ、2/3が両眼同時性である。乳頭浮腫はアミオダロン中止後も中央値3か月、最大15か月にわたり持続する。逐次性乳頭腫脹 :片眼発症後3〜48週で対側眼にも乳頭腫脹が出現する「sequential」パターンが報告されている1) 。渦状角膜沈着の併存 :視神経毒性と併発して高頻度に認められる。
Patelらは以下の5分類を提唱している2) 。
潜行性発症型
最も多い分類 :両側同時性乳頭浮腫を呈し、緩徐に進行する。自覚症状に乏しいことが多い。
非動脈炎性前部虚血性視神経症様型
2番目に多い分類 :急性片側性または両側性の視力喪失を呈し、非動脈炎性前部虚血性視神経症と臨床的に酷似する。
球後視神経症型
診断が最も困難 :正常眼底を呈し、画像検査・血液検査が診断に必要となる。
その他の型
頭蓋内圧亢進型 :髄液圧が200 mmH₂Oを超える。
遅延性進行型 :アミオダロン中止後数日〜数週で乳頭浮腫が出現する。
アミオダロン使用期間 :AAON発症までの平均期間は9か月(範囲1〜84か月)。中央値約4か月との報告もある2) 。治療期間の中央値41日を超えると視神経症リスクが3.5倍となる1) 。累積投与量 :日用量よりも累積投与量・投与期間がリスク評価に重要である1) 。視覚症状を呈した患者の用量中央値は200 mg/日(範囲57〜1,200 mg/日)。性別 :296例のレビューでは平均年齢66歳、74%が男性。男性は女性の約3倍のリスクを有する1) 。高血圧 :男性ではアミオダロン使用と高血圧が視神経症の有意なリスク因子である1) 。心血管リスク因子の併存 :アミオダロン服用患者の多くは心血管リスク因子を有し、非動脈炎性前部虚血性視神経症自体の発症リスクも高い。アミオダロン関連NA-AIONの特徴として、両側性・潜行性発症・全般性(非水平半盲型)視野欠損 ・乳頭腫脹が月単位で持続する点が挙げられる。
Q アミオダロンの用量を少なくすれば視神経症のリスクは減るのか?
A 日用量は有意なリスク因子ではなく、累積投与量と投与期間がより重要とされている1) 。治療期間中央値41日を超えるとリスクが3.5倍になるとの報告があり、短期間であっても経過観察は必要である。
AAONは臨床診断であり、確立された客観的診断基準は存在しない。
以下の所見が揃う場合にAAONが疑われる。
潜行性の発症
緩徐な進行
遷延する乳頭腫脹(アミオダロン中止後も数か月持続)
対側眼に大きな陥凹(disc at riskでない乳頭形態)
軽度の視神経機能障害(視力20/40以上、RAPD 0.9 logユニット以下)
全てのNA-AION患者にアミオダロン使用歴を確認し、陽性の場合は循環器科に報告すべきである。薬物性視神経症は服薬歴に注意し、まず疑うことが重要である。
AAONと非動脈炎性前部虚血性視神経症の鑑別は臨床上の最大の課題である。以下の表に主な鑑別点を示す。
鑑別点 非動脈炎性前部虚血性視神経症 AAON 発症様式 急性・数日〜数週 潜行性〜急性 乳頭形態 disc at risk(小乳頭) 特定の形態なし 乳頭浮腫の持続 2〜6週で消失 1〜15か月持続 側性 片側性が多い 両側性が多い
巨細胞性動脈炎 との鑑別にも注意を要する。アミオダロン使用中の72歳男性でAAON疑いとされたが、側頭動脈生検により巨細胞性動脈炎が確定した症例が報告されている3) 。巨細胞性動脈炎ではESR・CRP が正常であっても生検陽性となりうる3) 。また巨細胞性動脈炎ではMRIで視神経鞘の造影増強(optic perineuritis)が認められることがあり、AAONでは報告されていない所見である3) 。
フルオレセイン蛍光眼底造影 ハンフリー視野検査 :半側視野欠損〜中心暗点 を呈する。MRI :AAONでは通常正常であり、視神経の造影増強は認めない。巨細胞性動脈炎疑い例では視神経鞘増強(optic perineuritis)の有無を確認する3) 。
薬物性視神経症の治療原則として、被疑薬の中止が第一である。
アミオダロンは致死的不整脈の治療に使用されるため、中止は軽々しく行えない。以下の手順で対応する。
循環器科との緊急協議 :代替薬への変更またはカテーテルアブレーションの可否を循環器科と協議する。渦状角膜変性のみの場合 :通常はアミオダロン継続可能である。AAONを発症した場合 :薬剤継続のリスクとベネフィットを循環器科・眼科・患者の三者で慎重に協議する。既存の視神経疾患がある場合 :アミオダロン使用を避けることを推奨する専門家もいる。
中止後の視力転帰は以下の通りである。
視力改善:58%
不変:21%
さらなる視力低下:21%
法的盲(片眼以上で20/200未満):20%
AAONに対する確立された薬物療法は現在存在しない。
Q アミオダロンを中止すれば視力は回復するのか?
A アミオダロン中止後に視力が改善するのは58%にとどまり、21%は不変、21%はさらに悪化し、20%は法的盲(20/200未満)に至る。また半減期が20〜100日と長いため、中止後も薬剤が体内に残留し続ける点に注意が必要である1) 。
AAONの主な発症機序として、リン脂質症(phospholipidosis)に伴う軸索障害が中心的な役割を果たすと考えられている。
リソソーム機能障害 :アミオダロンがリソソーム・スフィンゴミエリナーゼを阻害し、リン脂質症を惹起する1) 。層板状封入体の蓄積 :視神経太い軸索の細胞質内に層板状封入体(intracytoplasmic lamellar inclusions)が選択的に蓄積する。これはアミオダロン誘発性末梢神経障害においても末梢神経の軸索・シュワン細胞に同様の変化が認められる。軸索流の障害 :層板状小体が軸索流(axoplasmic flow)を機械的・生化学的に減少させ、これが視神経損傷の機序と考えられる1) 。この乱れが乳頭浮腫の原因となりうる。酸化ストレス とアポトーシス 1) 。網膜神経節細胞 (RGC)への影響網膜電図 a波・b波の減少が確認されている1) 。
Q アミオダロンはどのようなメカニズムで視神経を障害するのか?
A アミオダロンがリソソーム・スフィンゴミエリナーゼを阻害してリン脂質症を惹起し、視神経軸索内に層板状封入体が蓄積する1) 。この蓄積が軸索流を障害して乳頭浮腫を引き起こすとともに、酸化ストレスによる細胞障害も加わることで視神経機能が低下すると考えられている。
Liaoら(2007)はRPE 細胞モデルで、IGF-1がPI3K/Akt経路を介してアミオダロン誘発性の酸化ストレスとアポトーシスからRPE細胞を保護することを示した1) 。RPE細胞の生存率はアミオダロンにより濃度依存的に低下し(LC50 = 50 μM)、IGF-1がこれを抑制した。MAPK経路の阻害は保護効果に影響しなかった1) 。
2017年のラット研究では、アミオダロンが網膜神経節細胞層に影響を及ぼし、IGF-1がこの効果を逆転させることが示された1) 。IGF-1の将来的なAAON治療への応用は今後の検討課題である。
Mindelら(2007)の前向き二重盲検試験(1,600人超、中央値45.5か月投与)では、両側性視力喪失の報告はなく、最大推定年間発生率は0.23〜0.74%であった1) 。これは従来の後方視的報告(0.36〜2%)と矛盾し、AAONが非動脈炎性前部虚血性視神経症とは臨床的に異なる独立した疾患実体であるかどうかの議論が続いている。
巨細胞性動脈炎症例のMRI所見として視神経鞘増強(optic perineuritis)が57〜78%で報告されており、AAONでは報告されていない所見である3) 。今後、AAON疑い例でのMRI所見の体系的評価が鑑別精度の向上に寄与しうる。
Mitchell R, Chacko J. Clinical and Mechanistic Review of Amiodarone-Associated Optic Neuropathy. Biomolecules. 2022;12:1298.
Patel S, Mahmood R. Amiodarone-Associated Optic Neuropathy in a Patient With Associated Arrhythmia. Cureus. 2024;16(3):e55819.
Tseng AM, Bindiganavile SH, Bhat N, Divatia MK, Lee AG. Optic Perineuritis Distinguishing Arteritic Ischaemic from Amiodarone-Associated Optic Neuropathy. Neuro-Ophthalmology. 2021;45(5):329-333.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください