アディー瞳孔
病巣:毛様体神経節(末梢)
瞳孔径:中等度散瞳、不整円
側性:片側性が多い(約80%)
緊張性:あり(縮瞳が長く続く)
ピロカルピン反応:低濃度で縮瞳

アディー緊張瞳孔(Adie tonic pupil)は、副交感神経の脱神経により、罹患瞳孔の対光反射が消失・減弱する一方、近接(近見)反応では良好かつ緊張性の縮瞳を示す疾患である。
疾患名はWilliam John Adieに由来し、1931年にAdie、Morgan、Symons、Holmesによりほぼ同時期に独立して報告された。有病率は人口1,000人あたり2人で、男女比2.6:1と女性に多く、平均発症年齢は32歳とされる。約80%が片側性であり、両側性への進展は年間4%の割合で生じる。
関連症候群として以下の2つが重要である。
約80%が片側性で発症する。ただし両側性への進展も年間4%の割合で生じるため、経過観察中に対側眼の瞳孔変化にも注意が必要である。
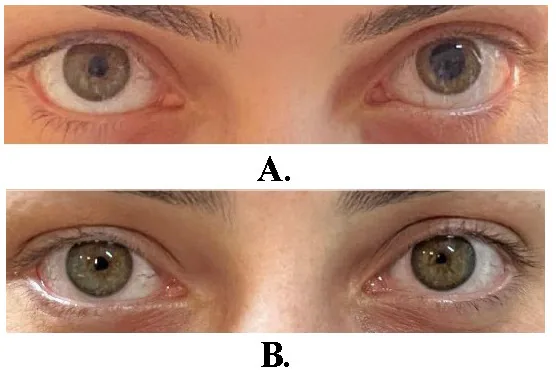
初期は罹患眼が散瞳して対側との瞳孔不同が顕著だが、慢性経過では罹患瞳孔が逆に縮小する傾向がある。これは毛様体由来の副交感神経線維が異常再生により瞳孔括約筋を支配するためと考えられている。
大部分は**特発性(原因不明)**であり、責任病巣は末梢の毛様体神経節および短後毛様体神経である。
特定できる原因として以下が報告されている。
ロス症候群の病因については、遺伝的素因に環境因子(ウイルス感染等)が加わるという説が提唱されている。一卵性双生児でのロス症候群の報告やサイトメガロウイルス感染後の発症例があり、遺伝的・感染性の両因子が関与する可能性がある3)。
COVID-19感染後の緊張性瞳孔については、COVID-19流行以降に免疫介在性機序による発症例が複数報告されており、感染後の神経眼科合併症として認識が広まっている1)2)。
典型的な症状(分節状麻痺、虫様運動、対光近見反射解離)が揃えば診断は容易である。
低濃度ピロカルピン点眼試験が最も広く用いられる。
対光近見反射解離を呈する疾患を中心に鑑別が必要である。
アディー瞳孔
病巣:毛様体神経節(末梢)
瞳孔径:中等度散瞳、不整円
側性:片側性が多い(約80%)
緊張性:あり(縮瞳が長く続く)
ピロカルピン反応:低濃度で縮瞳
Argyll Robertson瞳孔
病巣:中脳視蓋前域(梅毒)
瞳孔径:両側性の高度縮瞳
側性:両側性
緊張性:なし
ピロカルピン反応:低濃度では反応なし
視蓋瞳孔
病巣:中脳背側(松果体腫瘍等)
瞳孔径:中等度散瞳
側性:両側性
Parinaud症候群:合併が多い
緊張性:なし
その他の鑑別として、動眼神経麻痺後の神経異常再生、眼窩外傷・腫瘍、水痘帯状疱疹感染、フィッシャー症候群、シャルコー・マリー・トゥース病、神経サルコイドーシスが挙げられる。
梅毒血清反応(RPR)の検査、糖尿病・外傷・神経疾患の既往歴確認が診断の補助となる。ロス症候群が疑われる場合はMinor’s test(ヨウ素デンプン試験)で無汗領域を検出する3)。
否定はできない。急性期には脱神経過敏がまだ確立されていないため、陰性となる場合がある。臨床所見(虫様運動・分節状麻痺)が典型的であれば、試験陰性でも臨床的にアディー瞳孔と診断することが可能である。定期的に再検査することも有用である。
アディー瞳孔は良性の経過をたどる疾患であり、大多数の患者に対しては「良性疾患であること」を十分に説明し、経過観察が基本方針となる。
経過について:調節麻痺は数か月〜数年で改善することがある。一方、光に対する瞳孔反応(対光反射)は通常回復しない。
ロス症候群の代償性多汗症の治療:グリコピロレート外用、塩化アルミニウムクリーム、ボツリヌス毒素注射が使用される。重症で手術を望む患者には胸部交感神経切除術も選択肢となる3)。
調節麻痺による霧視や近見障害は数か月〜数年で改善することがある。しかし対光反射は通常回復しないため、光への瞳孔反応の正常化は期待できない。重篤な視力障害には至らないことが多く、安心して経過観察できる良性疾患である。
アディー瞳孔の発症機序には「脱神経過敏」と「異常再生」の2つが中心的な役割を果たす。
副交感神経解剖学的背景:動眼神経のEdingerWestphal(EW)核から出る副交感神経線維の95%が毛様体筋(調節に関与)へ、5%が瞳孔括約筋(対光反射に関与)へ至る。毛様神経節における対光反射と調節反応に関わる神経細胞の比は3:97とされており、対光反射に関わる線維が元々少数であることが特徴的である。
発症の経過は以下の順序で進行する。
対光近見反射解離の神経解剖学的説明:近見反応のEW核への核上性線維は、対光反射の求心線維が通る中脳視蓋前域や後交連より腹側を走行している。そのため、視蓋前域の障害(中枢性)でも同様の解離が生じるが、アディー瞳孔では病巣が毛様体神経節(末梢)にある点が鑑別の要となる。
COVID-19関連の機序:SARS-CoV-2感染後の緊張性瞳孔では、直接的なウイルスの神経侵入、内皮機能障害、過剰な炎症・サイトカイン放出による神経毒性の3つの機序が提唱されている1)。
ロス症候群の病態:後根神経節ニューロンと副交感神経系は神経堤細胞から共通の起源を持つとされており、この点がロス症候群における腱反射消失を説明する仮説として提唱されている3)。
COVID-19流行以降、感染後の神経眼科合併症として緊張性瞳孔の症例報告が相次いでいる。
Quijano-Nietoら(2021)は、36歳女性がCOVID-19感染(PCR陽性)の17日後に両側性緊張性瞳孔を発症した症例を報告した1)。脳MRI・血液検査・髄液検査はすべて正常。0.125%ピロカルピン点眼で両眼に強い縮瞳が確認された。免疫介在性機序が推定されている。
Gopalら(2021)は、37歳女性がCOVID-19感染3週間後に右眼の緊張性瞳孔を発症した症例を報告した2)。右眼瞳孔径5.5 mm、虫様運動と分節状収縮を確認。0.1%ピロカルピン点眼で縮瞳が確認された。MRI脳・眼窩に有意な所見なく、感染後免疫応答が原因として推察されている。
Ahmadら(2022)は同一施設で1か月以内に診断されたロス症候群2症例を報告した3)。症例1(24歳女性)は左緊張性瞳孔・右足首腱反射消失・T4レベルまでの分節性無汗の三徴を示した。症例2(42歳女性)は両側緊張性瞳孔・下肢腱反射消失・ホルネル症候群を合併した「Ross syndrome plus」であった。
ロス症候群がパーキンソン病・レビー小体型認知症・多系統萎縮症と同じシヌクレイノパチーである可能性が提唱されている3)。またロス症候群・ホームズ・アディー症候群・ハーレクイン症候群は同一疾患過程の異なる表現型である可能性も示唆されており、今後の疾患概念の統合が期待される。
Quijano-Nieto BA, Córdoba-Ortega CM. Tonic pupil after COVID-19 infection. Arch Soc Esp Oftalmol. 2021;96(7):353-355.
Gopal M, Ambika S, Padmalakshmi K. Tonic Pupil Following COVID-19. J Neuroophthalmol. 2021;41:e764-e766.
Ahmad R, Saurabh K. Two Cases of Tonic Pupil: Ross and Ross Syndrome Plus. Cureus. 2022;14(2):e22305.