保存的治療
局所ステロイド:炎症抑制が主目的。プレドニゾロン点眼を1日1〜4回1)。
散瞳薬:アトロピン1%を1日2回。血液房水関門の安定化と毛様体痙攣の緩和1)。
眼圧下降薬:房水産生抑制薬を最大2クラスまで。目標は症状緩和であり厳密な眼圧管理ではない1)。
人工涙液・眼軟膏:眼表面症状の緩和。防腐剤フリーが望ましい1)。
治療用コンタクトレンズ:水疱性角膜症の疼痛軽減に有効。

疼痛を伴う失明眼(painful blind eye; PBE)とは、視力が指数弁以下で機能回復の見込みがなく、4週間以上の慢性疼痛・不快感を伴う眼をいう1)。
失明者10人に1人がPBEを有するとされる1)2)。最も多い原因は血管新生緑内障を含む各種緑内障であり、外傷・角膜変性・慢性炎症・網膜剥離・眼内炎後遺症なども原因となる1)。多くの場合、初期治療に対して症状が難治性であり、患者のQOLを著しく低下させる1)。
現在のところPBE管理に関する統一されたガイドラインは存在せず、治療の多くが経験に基づいて行われている1)。
失明者のおよそ10人に1人がPBEを有するとされる1)2)。最も多い原因は緑内障であり、外傷・水疱性角膜症・慢性ぶどう膜炎などもPBEの原因となる。
PBEの主症状は慢性眼痛である。痛みの性状は鈍痛から激痛まで幅広い。
原因疾患に応じて多彩な所見を呈する。
PBEの原因疾患は多岐にわたる。
主な原因疾患を以下に示す。
| 分類 | 代表的原因 |
|---|---|
| 緑内障 | 血管新生緑内障、末期POAG |
| 角膜疾患 | 水疱性角膜症、帯状角膜変性 |
| 炎症性疾患 | 慢性ぶどう膜炎、眼内炎後 |
このほか、外傷後・慢性網膜剥離・角膜移植不全後なども原因となる1)。アフリカなどの発展途上地域では、伝統医療(TEM)による化学外傷や医療アクセスの制限がPBEの重要な要因である2)。
急性緑内障発作では急激な眼圧上昇により強い眼痛・頭痛・角膜浮腫が生じ3)、適切に管理されなければPBEに至ることがある。
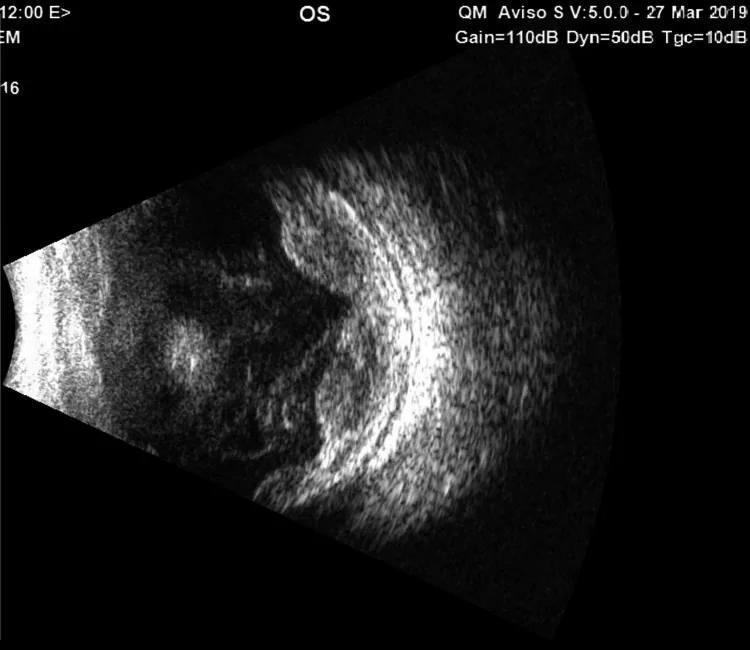
PBEの診断には、まず失明の原因疾患を特定し、疼痛の機序を理解することが重要である。
PBEの治療は段階的アプローチが基本である1)。保存的治療を第一選択とし、無効な場合に低侵襲治療、最終的に摘出術を検討する。
保存的治療
局所ステロイド:炎症抑制が主目的。プレドニゾロン点眼を1日1〜4回1)。
散瞳薬:アトロピン1%を1日2回。血液房水関門の安定化と毛様体痙攣の緩和1)。
眼圧下降薬:房水産生抑制薬を最大2クラスまで。目標は症状緩和であり厳密な眼圧管理ではない1)。
人工涙液・眼軟膏:眼表面症状の緩和。防腐剤フリーが望ましい1)。
治療用コンタクトレンズ:水疱性角膜症の疼痛軽減に有効。
低侵襲治療
毛様体光凝固(CPC):高眼圧が疼痛の主因である場合に選択。ダイオードレーザーによる経強膜CPCが主流1)。
球後注射:アルコールまたはクロルプロマジンを球後に注入し毛様体神経を遮断する1)。
硝子体内トリアムシノロン:炎症成分が強い場合に有効。初日から効果発現の報告あり1)。
ガンダーセン結膜弁:角膜表面の保護と疼痛軽減を図る1)。
高眼圧がPBEの疼痛に寄与している場合、毛様体破壊術が有効である。
Martinら(2001)は前向き研究で、経強膜ダイオードレーザーCPCがPBE 30眼中73%(22/30)で疼痛を軽減し、ベースラインからの眼圧30%以上低下が成功の最良予測因子であったと報告した(P = 0.0042)1)。
毛様体冷凍凝固術も有効であるが、低眼圧・眼球癆のリスクがCPCより高い1)。超音波毛様体形成術(UCP)は選択的凝固が可能な新しい手法であり、組織損傷の軽減が期待される1)。
点眼療法無効で摘出術を希望しない患者に対して選択される。
Galindo-Ferreiroら(2016)は前向きランダム化比較試験で、球後アルコール注射とクロルプロマジン注射を比較した。36週時点での有効率はアルコール43.7%(7/16)、クロルプロマジン37.5%(6/16)で両者に有意差を認めなかった(P = 0.6)。副作用はクロルプロマジンで一過性の眼窩刺激、アルコールで外眼筋不全麻痺が多かった1)。
PBEには角膜神経障害に起因する神経障害性疼痛の要素があるとされる1)。ガバペンチンは神経障害性疼痛の第一選択薬であり、PBEへの応用が報告されている。
Kavalieratosら(2008)は、毛様体破壊術でも疼痛コントロール不良であった緑内障性PBE患者にガバペンチン(最大2,400 mg/日)を投与し、投与初日から疼痛緩和が得られ6か月間効果が持続した症例を報告した1)。
角膜表面の障害が疼痛の主因である場合に選択される。
保存的・低侵襲治療に抵抗する場合、または眼球の変形・崩壊が高度な場合の最終手段である1)。
近年の研究では、眼球摘出術と内容除去術の疼痛軽減効果は同等であると結論されている1)。Nakraら(2006)は84例の観察研究で、義眼可動性は内容除去のほうが良好であった(正常の70% vs 54%)が、整容面・合併症に有意差はなかったと報告した1)。
摘出術前には超音波検査による眼内悪性腫瘍の除外が重要である1)。交感性眼炎のリスクは0.01〜0.3%とまれであるが、穿孔性外傷歴や複数回の内眼手術歴がある場合はリスクが高まる1)。
主にアルコール(100%)とクロルプロマジンが使用される。ランダム化比較試験では36週時点の有効率に有意差はなかった1)。副作用としてクロルプロマジンでは眼窩の一過性刺激、アルコールでは外眼筋不全麻痺が多い傾向にある。
両術式の疼痛軽減効果は同等と報告されている1)。内容除去は義眼の可動性に優れるとされるが、整容面や合併症に明らかな差はない。眼内腫瘍の可能性がある場合は眼球摘出が推奨される。患者の希望・全身状態・眼球の構造的保全度に応じて選択する。
PBEの疼痛は複数の機序が複合的に関与する。
持続的な眼圧上昇は角膜内皮障害を引き起こし、内皮のポンプ機能が閾値(おおむね500 cells/mm²以下)を下回ると角膜浮腫が不可逆性となる。上皮下に水疱(bullae)が形成され、これが破裂することで反復性の激しい疼痛が生じる。さらに進行すると角膜周辺部からの血管侵入と実質の瘢痕性混濁を生じる。
慢性ぶどう膜炎や眼虚血に伴う炎症メディエーターの持続的放出は、毛様体痙攣を誘発し疼痛の原因となる1)。ステロイド点眼と散瞳薬が有効であるのはこの機序に基づく。
PBEでは角膜神経の障害を介した末梢神経感作と、中枢レベルでの不適応的神経可塑性が関与するとされる1)。この機序はガバペンチノイドが有効である根拠となっている。
慢性炎症や眼球癆への進行過程で角膜実質にカルシウムが沈着し、帯状角膜変性を生じることがある。これ自体が異物感・疼痛の原因となる。EDTA塗布によるキレート除去や希塩酸による溶解が治療として用いられる。
最終的に毛様体機能が廃絶し房水産生が停止すると、眼球は萎縮・変形(phthisis bulbi)に至る2)。この段階でも疼痛が持続する場合があり、摘出術の適応となる。
PBE管理には統一されたガイドラインが存在しない。Parra-Tanouxら(2023)は利用可能なエビデンスに基づく段階的管理アルゴリズムを提案したが、多くの治療法でエビデンスが不足しており大規模研究の必要性を指摘している1)。
超音波毛様体形成術(UCP)は選択的凝固とマイクロパルス照射により組織損傷を最小化する手法であり1)、PBEへの応用が期待される。従来の経強膜CPCとの比較臨床試験が今後求められる。
Xavierら(2016)は、緑内障性PBE 6例に対して週1回×6セッションの星状神経節ブロックを施行し、1年後の追跡で4例中2例が無痛を維持、2例はガバペンチノイドの追加で疼痛管理が可能であったと報告した1)。
集学的疼痛管理チームとの連携が必要な手法であり、エビデンスの蓄積が待たれる。
アフリカではPBEの有病率が高い一方、眼科医の数が著しく不足している2)。CPCや球後注射などの低侵襲治療の普及と、プライマリケアレベルでの初期対応体制の構築が課題として挙げられている2)。