前眼部・眼表面
ドライアイ:最も頻度が高いirAE。PD-1/PD-L1阻害薬ではシェーグレン症候群様の涙液分泌低下を生じることがある。
前部ぶどう膜炎:前房内炎症細胞。ステロイド点眼に反応する症例が多い。
角膜びらん:ベーチェット病様症候群の一部として出現することがある。

免疫チェックポイント阻害薬(ICI)は、T細胞のブレーキ役であるチェックポイント分子を阻害し、がん細胞に対する免疫応答を増強するモノクローナル抗体である1)。がん治療に革命をもたらした一方、腫瘍以外の部位に非特異的な炎症を引き起こす免疫関連有害事象(irAE)が問題となる1)。
主な標的分子と代表的薬剤を以下に示す1)。
| 標的分子 | 代表的薬剤 |
|---|---|
| CTLA-4 | イピリムマブ、トレメリムマブ |
| PD-1 | ペムブロリズマブ、ニボルマブ、セミプリマブ |
| PD-L1 | アテゾリズマブ、アベルマブ、デュルバルマブ |
CTLA-4はT細胞表面の共刺激分子CD80/CD86との相互作用を介してT細胞活性化を抑制する1)。PD-1は活性化T細胞表面の受容体で、抗原提示細胞や腫瘍細胞上のPD-L1と結合すると免疫応答を抑制する1)。これらの阻害によりT細胞活性化と抗腫瘍免疫が促進されるが、同時に自己免疫反応も惹起されうる。
眼irAEの発生率は1〜3%であり、主に眼表面疾患(ドライアイ)と前部ぶどう膜炎として現れる1)。後眼部(網膜・脈絡膜)への炎症は全眼irAEの約5〜20%を占めるが、重篤度が高く、適切に対処しなければ永続的な視力障害に至る可能性がある1)。
眼の免疫関連有害事象(irAE)は1〜3%の頻度で生じる1)。大部分はドライアイや前部ぶどう膜炎であるが、後眼部炎症(5〜20%)は視力予後に影響する重篤な合併症となりうる。
部位と重症度によって多彩である。ドライアイでは乾燥感・異物感が主体である。ぶどう膜炎では充血・霧視・羞明を生じる。眼窩筋炎では複視・眼瞼下垂・眼球突出がみられる2)。後眼部炎症では視力低下・飛蚊症が出現する1)。
ICI関連眼irAEは眼のほぼ全領域に生じうる。部位別の主な病態を以下に示す。
前眼部・眼表面
ドライアイ:最も頻度が高いirAE。PD-1/PD-L1阻害薬ではシェーグレン症候群様の涙液分泌低下を生じることがある。
前部ぶどう膜炎:前房内炎症細胞。ステロイド点眼に反応する症例が多い。
角膜びらん:ベーチェット病様症候群の一部として出現することがある。
後眼部
眼窩
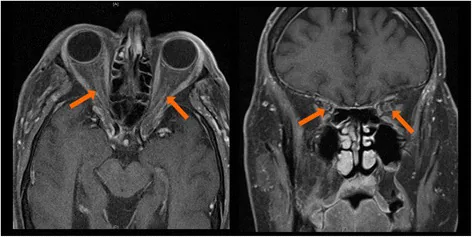
眼窩筋炎:両側性が多い。MRIで眼外筋腫大・造影増強を認める2)。
眼窩脂肪炎症:眼窩先端部・上眼窩裂まで波及することがある2)。
甲状腺眼症様炎症:甲状腺機能正常例でも出現する。
神経
眼窩炎症の発症時期は初回投与後2日〜2ヶ月と幅広い2)。全身症状(倦怠感・発熱・消化器症状・全身筋炎・心筋炎)を伴うことがある2)。
ICIによる眼irAEの根本原因は、T細胞の免疫チェックポイント解除に伴う自己免疫反応の惹起である1)。
ICIはT細胞の免疫チェックポイントを解除してがんを攻撃させるが、眼組織のPD-L1依存的免疫特権も同時に破綻させる1)。詳細は「病態生理学」の項で3つの主要メカニズムを解説する。
ICI関連眼irAEの診断は、ICI使用歴と眼所見の時間的関連性に基づく。以下の検査が用いられる。
| 部位 | 主な検査法 |
|---|---|
| 前眼部 | 細隙灯検査 |
| 後眼部 | OCT・FA・網膜電図 |
| 眼窩 | MRI |
ICI関連眼irAEは多彩な既知の眼疾患を模倣する。前部ぶどう膜炎では感染性・非感染性ぶどう膜炎との鑑別が必要である。VKH様反応は原発性VKHと臨床的に類似するが、メラノーマに対するICI使用歴が重要な手がかりとなる1)。眼窩筋炎では甲状腺眼症・IgG4関連疾患・特発性眼窩炎症との鑑別を要する2)。
治療は腫瘍内科医と眼科医の協議のもと、重症度に応じて個別化する。
ICIの中止が必要になることは稀である。多くの眼irAEはステロイド(点眼・局所注射・全身投与)により制御可能であり、ICI治療を継続しながら眼科的管理を行うことが一般的である。ただし重症例では腫瘍内科医との協議のもと中止を検討する。
眼は免疫特権臓器であり、以下の機構がT細胞による炎症を抑制している1)。
ICIはこれらのPD-1/PD-L1依存的な免疫特権機構を直接標的とするため、眼内T細胞活性化のリスクが生じる1)。
Haliyurら(2025)は、ICI誘発性後眼部irAEを以下の3型に分類することを提唱した1)。
Type 1
T細胞の交差反応・自己反応性拡大
Type 1a:抗腫瘍T細胞がメラニン含有細胞など眼組織と交差反応し、VKH様汎ぶどう膜炎を惹起する1)。メラノーマ患者のVKH様反応の5〜14%を占める。
Type 1b:既存の眼特異的組織常在メモリーT細胞がICIにより拡大・活性化される1)。自己免疫性網膜症を引き起こす。
Type 2
バイスタンダー効果による血管炎
ICI使用に伴う全身的な炎症増強が、非特異的に血液網膜関門を破綻させる1)。
CD4陽性T細胞による血管周囲リンパ形質細胞浸潤と接着分子の発現亢進が網膜血管炎・動静脈閉塞を引き起こす1)。
Type 3
自己抗体介在性炎症
PD-1はB細胞にも発現しており、ICIがB細胞系列の拡大と形質細胞からの組織特異的自己抗体産生を誘導する1)。
傍腫瘍症候群(MAR様網膜症など)の増悪にも関与する1)。
Haliyurら(2025)は、ICI誘発性後眼部irAEの3つのメカニズム分類を提唱した1)。Type 1ではT細胞の眼組織交差反応(1a)と自己反応性T細胞の拡大(1b)、Type 2ではバイスタンダー効果による網膜血管炎、Type 3では自己抗体介在性炎症が想定される。臨床所見は1つの機序に限定されず、複数の機序が重複することもある。
抗CTLA-4阻害薬(イピリムマブ)が最も高頻度に眼窩炎症を引き起こす2)。抗PD-1/PD-L1阻害薬でも同様の臨床像が報告されている2)。MRIでは眼外筋の腫大・造影増強と眼窩脂肪の炎症性変化を認め、両側性に出現する傾向がある2)。
ICI適応の急速な拡大により、今後数十年でICI関連眼irAEの症例数は増加すると予測される1)。
現時点では後眼部irAEの病態理解は主に症例報告・症例集積に基づいており、機序に関する実験的研究はわずかである1)。ICI関連VKH様反応に対する診断基準や治療ガイドラインは確立されていない。治療反応性の良好な例がある一方、遷延する滲出性網膜剥離やICI誘発性閉塞性網膜血管炎では永続的な視覚障害を生じうる1)。
今後の課題としては、後眼部irAEのメカニズム型別の治療戦略の確立、ICI投与前のベースライン眼科検査の標準化、および腫瘍内科・眼科間の連携プロトコールの整備が挙げられる。