眼所見
結膜下虫体移行:成虫が球結膜下を移行する様子が肉眼で観察される。本疾患の病徴的所見である。組織への永続的損傷は通常伴わない
眼瞼浮腫:成虫の眼周囲移行に伴い浮腫が生じる
眼瞼結膜炎:流涙・羞明の増加を伴う1)
眼内糸状虫症(稀):前房や硝子体内に虫体が侵入する。線維素膜形成・前房内細胞/フレア・角膜後面沈着物を認める。視力は6/24から光覚まで低下しうる

ロア糸状虫症(loiasis)は、フィラリア線虫であるロア糸状虫(Loa loa)がヒトの皮下・粘膜下組織に寄生することで生じる感染症である。成虫が球結膜下を移行する様子が肉眼で観察されるため「アフリカ眼虫(African Eye Worm)」とも呼ばれる。
ロア糸状虫はヒトと霊長類にのみ感染する1)。雄は約3cm、雌は5〜7cmの体長を有し、直径は0.4〜0.5mmである1)。成虫は20年以上生存可能であり、成熟した雌は1日に12,000〜39,000体のミクロフィラリアを産生する。
媒介ベクターはメマトイアブ属(Chrysops)の吸血性アブである。生息域は西部・中部赤道アフリカの森林地帯および沼沢地であり1)、アンゴラ、カメルーン、中央アフリカ共和国、コンゴ、ガボン、ナイジェリアなどが流行地域に含まれる。1,000万人以上が罹患し、1,400万人以上がハイリスク地域に居住している。
従来は良性疾患と考えられてきた。しかし近年、ミクロフィラリア血症に関連する死亡の人口寄与危険割合が14.5%であるとの報告があり、良性とする見解には疑問が呈されている。
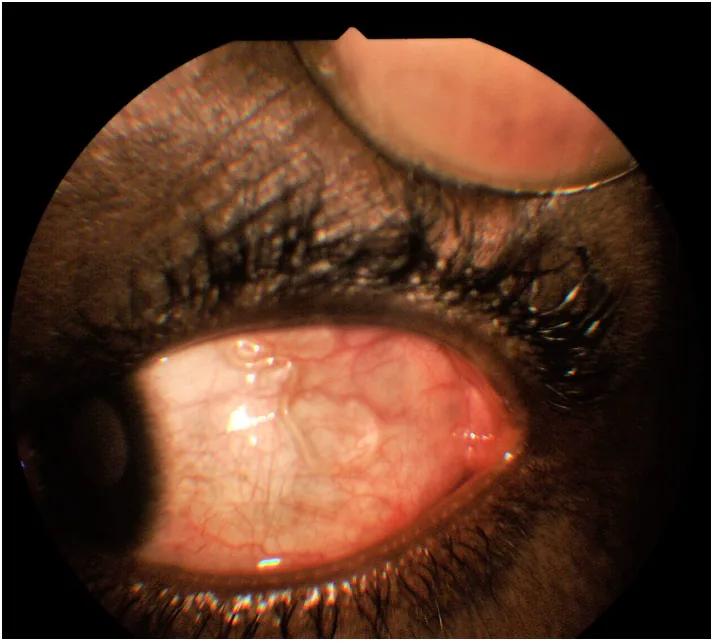
流行地域の永住者では多くの感染が無症状である。一方、旅行者や短期滞在者では「過敏反応症候群」として好酸球増多・血管性浮腫・全身性掻痒感・IgE上昇が顕著に現れやすい。眼症状としては異物感・不快感が多く報告される。眼内に虫体が侵入した場合は疼痛・羞明を呈する。
眼所見
結膜下虫体移行:成虫が球結膜下を移行する様子が肉眼で観察される。本疾患の病徴的所見である。組織への永続的損傷は通常伴わない
眼瞼浮腫:成虫の眼周囲移行に伴い浮腫が生じる
眼瞼結膜炎:流涙・羞明の増加を伴う1)
眼内糸状虫症(稀):前房や硝子体内に虫体が侵入する。線維素膜形成・前房内細胞/フレア・角膜後面沈着物を認める。視力は6/24から光覚まで低下しうる
全身所見
カラバル腫脹:患者の50%に出現する1)。四肢に好発する5〜20cmの非発赤性皮下浮腫であり、数時間〜2〜4日で自然退縮する1)。成虫の皮下移行に対する過敏反応による
好酸球増多:著明な末梢血好酸球増多を認める1)
その他:関節痛(免疫複合体沈着)1)、リンパ節炎1)、まれに髄膜脳炎1)・末梢神経障害1)・心筋線維化1)
結膜下を移行する虫体が見えた場合は、すぐに消えてしまう可能性があるため速やかに眼科を受診してください。結膜下の虫体は通常、局所麻酔下に小さな結膜切開を行い摘出できます。ただし、全身のミクロフィラリアが残存するため、虫体摘出後も抗寄生虫薬による全身治療が必要です。
ロア糸状虫症の原因はLoa loaの感染であり、メマトイアブ属(Chrysops)の雌アブが媒介する1)。アブは午前10時から午後2時に最も活発であり、昼行性パターンを示す。生息地は森林・沼沢地であり、雨季に最も多い1)。
感染経路:
ミクロフィラリアの昼間出現性:ミクロフィラリアは鞘に包まれ、正午にピークを迎える昼間出現性(diurnal periodicity)を示す1)。この周期性はメマトイアブの活動時間と一致する。
リスク要因:
はい、流行地域への旅行者も感染します。特に1か月を超える滞在で感染リスクが高まります。旅行者は流行地域の永住者と比較して症状がより強く現れる傾向があり、著明な好酸球増多・血管性浮腫・全身性掻痒感を呈する「過敏反応症候群」を発症しやすいとされています。
確定診断はミクロフィラリアの同定または成虫の直接確認に基づく。
確定診断法:
ミクロフィラリアの検出率は必ずしも高くない。非流行地域出身者では陰性のことが多い1)。ミクロフィラリアは不規則に末梢血中に放出されるため、異なる日に複数回の採血が必要となることがある1)。
血清学的検査・分子生物学的検査:
| 鑑別疾患 | 鑑別のポイント |
|---|---|
| 回旋糸状虫症 | 皮膚掻痒が顕著、河川盲目症 |
| リンパ系糸状虫症 | リンパ浮腫・象皮病 |
| 東洋眼虫症 | 結膜嚢内に虫体 |
回旋糸状虫(O. volvulus)との重複感染は臨床的に重要である。治療薬選択に直結するため、ロア糸状虫特異的な検査による鑑別が不可欠である。
薬物療法がロア糸状虫症の基本的治療であり、虫体摘出のみでは全身のミクロフィラリアを根絶できない。
薬物療法
ジエチルカルバマジン(DEC):第一選択薬。8〜10mg/kg 1日3回×3週間で投与する。成虫とミクロフィラリアの両方に有効である。予防投与にも使用可能。ミクロフィラリア血症≧2,500mf/mLでは脳症リスクがあり禁忌
アルベンダゾール:高ミクロフィラリア血症の前治療として使用する。成虫を標的とし、血中ミクロフィラリアを緩徐に減少させる。DECと比較して副作用が少ない
イベルメクチン:単回投与で1年以上ミクロフィラリアを減少させるが、成虫への活性はない。高負荷患者では脳症リスクがある。症例報告ではイベルメクチン200μg/kg/週×3週+アルベンダゾール800mg/日×1か月での治癒が報告されている1)
外科的治療
結膜下虫体摘出:虫体出現時に鉗子で把持し、エピネフリン含有リドカインの結膜下注射で麻酔・麻痺後、5mm以下の結膜切開で摘出する
前房洗浄:前房内糸状虫に対し前房洗浄を行い、ステロイド・抗菌薬の結膜下注射を追加する。線維素膜がある場合は切除が必要
硝子体切除術:硝子体内の糸状虫に対して行われるが、極めて稀な適応である
治療薬の主な懸念は、血中ミクロフィラリアが急速に死滅することで起こる脳症や網膜出血です。ミクロフィラリア量が少ない患者(2,500mf/mL未満)ではDECの安全性は比較的高いとされています。高負荷の場合はアルベンダゾールで前治療してからDECまたはイベルメクチンに切り替えます。症例報告ではミクロフィラリア陰性の患者にイベルメクチン+アルベンダゾールを投与し、軽度掻痒以外の副作用なく治癒しています1)。
ロア糸状虫の生活環はメマトイアブ(Chrysops)とヒト宿主の間で完結する。
感染サイクル:
カラバル腫脹の機序:成虫が皮下を移行する際に宿主の免疫系が反応し、IgE介在の過敏反応が生じる。一過性の局所浮腫として現れ、数時間〜数日で自然退縮する1)。
眼病変の機序:成虫が眼周囲組織を経て結膜下に移行する1)。結膜下の虫体移行は通常、永続的な組織損傷を来さない。しかし前房や硝子体に侵入した場合は、虫体に対する強い炎症反応(線維素膜形成、ぶどう膜炎)が視力喪失の原因となる。
ミクロフィラリア血症と臓器障害:循環器系内でのミクロフィラリアの閉塞性・炎症性プロセスが網膜血管病変(ロア糸状虫網膜症)や他臓器障害を引き起こすと推測されている。この機序は死亡リスク上昇(人口寄与危険割合14.5%)を説明する仮説として提唱されている。
ロア糸状虫症に関する研究は主に診断法の改良と安全な治療戦略の確立に向けて進展している。
新規診断法の開発:LISXP-1抗原を利用したイムノクロマト法が開発され、対照群に対して感度94%・特異度100%を達成している。LAMP法は高感度であり、イベルメクチン治療後の副作用リスク者の判別にも有用である。これらの検査法は流行地域での集団投薬プログラムの安全性向上に寄与する可能性がある。
集団投薬の課題:回旋糸状虫症に対するイベルメクチン集団投薬プログラムは、ロア糸状虫との重複感染地域で重篤な副作用のリスクにより制限されている。ミクロフィラリア量の迅速評価法の開発が進められており、安全な集団投薬の実現が期待される。
今後の課題:
- Lunardon L, Romagnuolo M, Cusini M, Veraldi S. A Case of Possible Loiasis Contracted in Cameroon and Diagnosed in Milan, Italy, and Review of Cases Published in Dermatological Journals. Case Rep Dermatol. 2021;13:389-393.