眼圧と視力
視力低下:軽度の低下から手動弁まで幅広い。症例報告では矯正視力20/80まで低下した例がある1)。
眼圧上昇:真の眼圧は上昇しているが、中央角膜のゴールドマン圧平眼圧計では偽低値を示すことがある2)。インターフェースの液体クッション効果により容易に圧縮されるためである1)。
周辺部測定:トノペンやダイナミック・コントア眼圧計で周辺部の眼圧を測定すべきである2)。

インターフェース液症候群(interface fluid syndrome:IFS)は、LASIK術後にフラップと角膜実質床の間(インターフェース)に液体が貯留する、稀ではあるが視機能を脅かす合併症である。Lyle & Jinが初めて報告し、Belinらが2002年に眼圧上昇に伴う層間実質角膜炎(pressure-induced interlamellar stromal keratitis:PISK)として記述した1)。
IFSの主要な原因はステロイド誘発性の眼圧上昇である1)3)。ステロイド誘発性眼圧上昇はインターフェースへの液体貯留を引き起こし、眼圧の過小評価にもつながる3)。術後早期(数日〜数週間)に発症することが多いが、LASIK後10年で発症した遅発性症例も報告されている1)。
LASIK以外にもSMILE(小切開角膜抽出術)や層状角膜移植術の後にも発生しうる。エジプトにおけるLASIK後のIFS発生率は2.9%と報告されているが、この研究では強力なステロイド(デキサメタゾン)を使用していたため、一般的な発生率はこれよりかなり低いと推測される。
LASIK術後数日〜数か月(ときに数年)後に霧視を主訴として来院する。疼痛や羞明を伴うこともある1)。典型的にはLASIK術後に長期間にわたり局所ステロイドを使用している患者に発症する1)。
眼圧と視力
視力低下:軽度の低下から手動弁まで幅広い。症例報告では矯正視力20/80まで低下した例がある1)。
眼圧上昇:真の眼圧は上昇しているが、中央角膜のゴールドマン圧平眼圧計では偽低値を示すことがある2)。インターフェースの液体クッション効果により容易に圧縮されるためである1)。
周辺部測定:トノペンやダイナミック・コントア眼圧計で周辺部の眼圧を測定すべきである2)。
角膜所見
インターフェース混濁:フラップと実質床の間にびまん性の混濁を認める1)。
液体貯留:細隙灯顕微鏡検査で明らかな液体層が確認できる場合がある。常に明瞭とは限らない。
角膜浮腫:上皮下浮腫やマイクロブラエ(微小水疱)を認めることがある1)。
OCT所見:前眼部OCTでインターフェースの液体貯留を明確に確認でき、診断確定に有用である1)2)。
IFSの原因は大きく2つに分類される。第一はステロイド誘発性の眼圧上昇であり、最も一般的な原因である1)3)。第二は角膜内皮機能不全である。
眼圧上昇をきたすあらゆる病態がIFSの原因となりうる。ぶどう膜炎、Posner-Schlossman症候群、サイトメガロウイルス内皮炎、前眼部毒性症候群(TASS)、外傷、感染性角膜炎などが報告されている。Fuchs角膜内皮変性症などの角膜内皮不全を有する患者も発症リスクが高い。
角膜実質とフラップの間に潜在的なスペースが生じる手術を受けた患者はすべてIFSのリスクがある。LASIK患者で最も多いが、SMILEや層状角膜移植術後にも認められる。
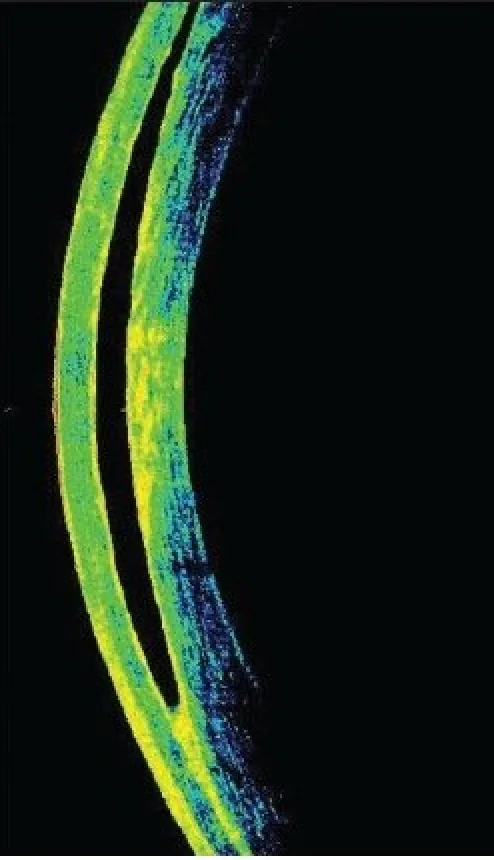
Dawsonらは2007年に以下の病期分類を提案した。
| 病期 | 所見 |
|---|---|
| Stage 0 | 正常なLASIK後角膜 |
| Stage 1 | 軽度〜中等度腫脹、混濁は最小限 |
| Stage 2 | 中等度〜重度腫脹、びまん性混濁と液体ポケット |
| Stage 3 | 癒合した大きな液体ポケット、散在性混濁 |
診断は臨床経過と細隙灯顕微鏡検査により行い、前眼部OCTで確定する1)。OCTではフラップと実質床のインターフェースにおける液体貯留を確認できる1)。角膜デンシトメトリー(Scheimpflug撮影による角膜輝度測定)もIFSの評価とグレーディングに有用である1)。
眼圧測定においては、ゴールドマン圧平眼圧計による中央測定では偽低値を示す可能性があるため注意が必要である2)。周辺部でのトノペン測定やダイナミック・コントア眼圧計が推奨される1)2)。
| 疾患 | 鑑別のポイント |
|---|---|
| DLK | 術後2〜5日発症、疼痛あり、眼圧正常 |
| 微生物性角膜炎 | 眼圧正常、浸潤を認める |
| 上皮迷入 | 眼圧正常、インターフェース液なし |
DLKとの鑑別は特に重要である。DLKの治療はステロイド投与であるが、IFSに対してステロイドを投与すると眼圧がさらに上昇し症状が悪化するためである1)。DLKでは炎症性単核球や顆粒球がみられるのに対し、IFSでは炎症細胞は認められない1)。
IFSの診断は、LASIK術後のステロイド使用歴、霧視の発症、細隙灯顕微鏡でのインターフェース混濁の確認に基づく。確定診断には前眼部OCTでフラップ-実質床間の液体貯留を確認する。眼圧は中央測定では偽低値を示す可能性があるため、周辺部での測定やダイナミック・コントア眼圧計を用いるべきである。DLK(びまん性層板状角膜炎)との鑑別が極めて重要であり、DLKは術後早期に疼痛を伴い眼圧は正常であるのに対し、IFSは眼圧上昇が本態である。
IFSの治療はステロイド中止と眼圧降下薬の開始が基本である1)。
β遮断薬(チモロール等)が第一選択であり、効果不十分な場合は炭酸脱水酵素阻害薬やα作動薬を併用する1)。症例報告ではブリモニジン0.2%、チモロール0.5%、ドルゾラミド2.0%の3剤併用で36時間後に視力改善が認められている1)。眼圧降下薬は1〜3か月間継続し、漸減中止する1)。
薬物療法で眼圧コントロールが不十分な場合は外科的介入が必要となることもある。Fuchs角膜内皮変性症に伴うIFSに対しDMEK(デスメ膜内皮移植術)で管理した報告がある。
上皮迷入を合併する場合は、フラップを挙上し機械的除去を行う1)。50%アルコールおよび0.02%マイトマイシンCの塗布を併用し、再発を予防する1)。
IFSの適時な診断は永久的な視力喪失を防ぐために極めて重要である。DLKと誤診してステロイドを投与するとIFSは悪化するため、両者の鑑別が治療方針を左右する。1)
IFS(インターフェース液症候群)とDLK(びまん性層板状角膜炎)はいずれもLASIK後のインターフェースに混濁を生じるが、病態と治療が異なる。DLKは術後2〜5日に発症する特発性のインターフェース炎症であり、疼痛を伴い眼圧は正常で、ステロイド点眼で改善する。一方IFSは眼圧上昇が本態であり、ステロイドによりむしろ悪化する。IFSでは炎症細胞は認められず、浮腫が主体である。治療はステロイド中止と眼圧降下薬投与が基本となる。
IFSの病態生理には主に2つのメカニズムが提唱されている。
第一のメカニズムは眼圧上昇による液体移動である。眼圧が上昇すると、角膜内皮を介して高圧域(前房側)から低圧域(インターフェースのスペース)へ液体が移動する。LASIKのフラップ作成により生じたインターフェースが低圧域となるため、液体がそこに貯留する。ステロイド誘発性眼圧上昇がこのメカニズムの最も一般的な誘因である1)3)。
第二のメカニズムは角膜内皮機能不全である。Fuchs角膜内皮変性症などで角膜内皮のポンプ機能が障害されると、角膜実質からの水分排出が不十分となり、インターフェースに液体が蓄積しやすくなる。
DLKでは炎症性単核球や顆粒球の集積が認められるのに対し、IFSでは炎症細胞は存在せず浮腫のみである1)。共焦点顕微鏡ではマイクロラクーナ(微小空隙)が観察され、これは実質浮腫の結果と考えられている1)。
遅発性IFSの機序として、上皮迷入が瘻孔を形成し、液体がインターフェースに流入するための「スペース」を提供するという仮説も提唱されている1)。
ステロイド誘発性眼圧上昇はインターフェースへの液体貯留を引き起こし、眼圧の過小評価にもつながる。眼圧を降下させることで炎症は消退する。3)
IFSでは実際には眼圧は上昇している。しかしゴールドマン圧平眼圧計で中央角膜を測定すると、インターフェースに貯留した液体のクッション効果により角膜が容易に圧縮されるため、眼圧が偽低値として測定される。このため、LASIK既往のある患者では周辺部での眼圧測定やダイナミック・コントア眼圧計の使用が推奨される。
IFSの臨床像は拡大している。従来は術後早期の合併症と考えられていたが、LASIK後10年で発症した遅発性PISK+上皮迷入の症例が報告された1)。この症例では上皮迷入が瘻孔を形成しインターフェースへの液体流入を促進したと推察されている1)。また、ぶどう膜炎の治療でステロイドを追加したことでLASIK後9年目にPISKが発症した症例も報告されている1)。
SMILEの普及に伴い、SMILE術後のIFSも鑑別診断として考慮すべき合併症となっている。従来の眼圧測定法の限界が認識されるようになり、前眼部OCTによるスクリーニングの重要性が強調されている2)。原因不明の視力低下や眼圧上昇を認めた場合はOCTの実施が推奨される1)。
IFSは通常術後1〜3日に発生するが、数年後に発生することもある。長期ステロイド使用中のLASIK既往患者では継続的な眼圧モニタリングが重要である。1)