術式の特徴
移植組織:デスメ膜+内皮細胞層のみ(約15μm)
接着方法:空気または20% SF6気体タンポナーデ
切開幅:2.2〜2.4mmの角膜小切開
視力回復:DSAEKより速く、術後20/25達成率が高い

デスメ膜角膜内皮移植術(DMEK: Descemet membrane endothelial keratoplasty)は、角膜内皮機能不全に対して行われる角膜内皮移植術の一種である。2006年にMellesらによって初めて報告された1)。ドナー角膜からデスメ膜と角膜内皮細胞層のみを分離し、レシピエントの病的デスメ膜を除去した角膜後面に気体タンポナーデで接着させる。グラフトの厚さは約15μmであり、実質を含むDSAEK(約50〜150μm)と比較してきわめて薄い1)。
術式の特徴
移植組織:デスメ膜+内皮細胞層のみ(約15μm)
接着方法:空気または20% SF6気体タンポナーデ
切開幅:2.2〜2.4mmの角膜小切開
視力回復:DSAEKより速く、術後20/25達成率が高い
DSAEKとの違い
DSAEK:後部実質(50〜150μm)+デスメ膜+内皮を移植
DMEK:デスメ膜+内皮のみを移植
遠視シフト:DMEKのほうが小さい1)
拒絶反応:DMEKのほうが低頻度1)
角膜内皮移植はDSAEKとDMEKが二大術式である。DMEKは実質を含まないため光学的に優れ、惹起乱視がわずかであり、拒絶反応もほぼ生じないとされる。一方、術中のグラフト操作が難しく、グラフト剥離のリスクがDSAEKより高い1)。
DMEKの利点として、技術的機材の要求が少なくDSAEKと比較してコスト削減が可能なこと、またsplit cornea transplantation(1つのドナー角膜をDMEKとDALKの2名に使用)が可能であることが挙げられる1)。
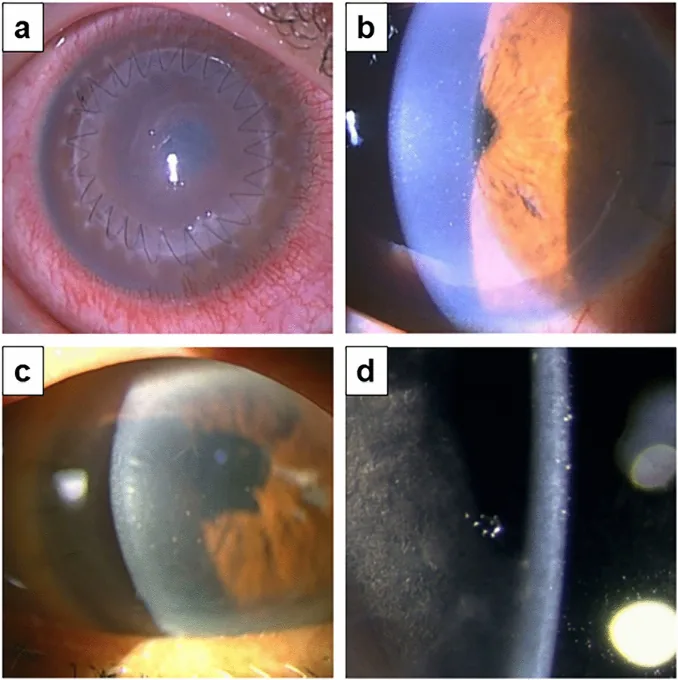
DMEKの主な適応は角膜内皮機能不全である。
角膜実質に瘢痕がある場合は、DMEKでは混濁や不正乱視が残るため全層角膜移植を考慮する。原則として偽水晶体眼であることが望ましい。
FECDの手術適応判断にはScheimpflugトモグラフィが有用である。以下の3所見はFECDの進行と角膜移植の必要性を強く予測する8)。
3所見すべてが存在する場合の5年進行率は約90%であり、いずれも認めない場合は約7%にとどまる。角膜厚640μm以下の患者は白内障術後1年以内に角膜移植を要しない確率が95%とされる8)。
COL8A2遺伝子変異(p.Leu450Trp)に伴う早期発症型Fuchs角膜内皮ジストロフィに対しても、DMEKは有効であり全眼20/20〜20/30の良好な視力を達成した報告がある7)。長期の角膜浮腫にもかかわらず、術後に角膜は透明化しうる7)。
以下の眼ではDMEKの適応はない。
前房操作が困難な症例(極度の水疱性角膜症、前房が非常に浅い場合など)ではDSAEKが選択される場合がある。
視力回復の速さと最終視力ではDMEKが優れています。ただし、無虹彩や広範な虹彩前癒着がある眼、硝子体切除術後の眼、前房の視認性が不良な眼ではDSAEKのほうが安全に施行できます。角膜実質の瘢痕が強い場合は、いずれの内皮移植でも視力改善が限られるため全層角膜移植を検討します。
SCUBA法(submerged cornea using backgrounds away technique)が広く用いられる。ドナー強角膜片の内皮面を上にして、シュレム管内側のデスメ膜をクレセントナイフまたはゴルフ刀で360°浅く切開する1)。その内側を無鈎鑷子でゆっくり持ち上げ、デスメ膜を剥離する。剥離されたデスメ膜は内皮細胞を外側にした筒状(scroll)を形成する。
0.06%トリパンブルーで染色し、患者に適した径にトレパンで円形切開してJonesチューブにセットする。デスメ膜の実質側に”S”や”F”のマークをトリパンブルーで記しておくと、前房内でグラフト表裏を誤認するリスクが減る。
球後麻酔またはテノン嚢麻酔で施行する。硝子体圧が高いと予想される症例ではホナンバルーンで術前に眼圧を下げる。
FECDは白内障と好発年齢が重複するため、以下の3つの方針を角膜の状態に応じて選択する8)。
Triple-DMEKでは以下に留意する。
BSS(balanced salt solution)または空気灌流下で、逆シンスキーフックを用いてレシピエント角膜のデスメ膜を円形に剥離する。剥離径は通常8.0mm前後である。
グラフト挿入
挿入器具:Jonesチューブ(ガラスチューブ)またはガラスインジェクター
切開幅:2.2〜2.4mmで十分
前置糸:10-0ナイロンを掛けておき、挿入後速やかに閉鎖
手順:実質側が上になる向きでグラフトを水流で前房内に流し込む
展開と気体注入
展開操作:角膜表面のタッピングとBSS注入・吸引を交互に行う1)
表裏確認:術中OCTまたはS/Fマークで確認
気体タンポナーデ:20% SF6ガスまたは空気を注入
術後体位:仰臥位を30〜60分維持
グラフト挿入後、サイドポートから前房水を少し抜いて低眼圧にし、グラフトの眼外脱出を防ぐ。10-0ナイロンで角膜切開創を縫合する。周辺虹彩切除は通常、グラフト展開と気体注入の後に施行する。
グラフト剥離とrebubbling:DMEKの最も頻度の高い合併症である。DMEKではDSAEKよりグラフト剥離の頻度が高い1)。メタアナリシスではrebubbling(再気泡注入)のオッズ比は2.76(95%CI 1.46-5.22)とDMEKで有意に高い2)。グラフト剥離が生じた場合、早期のrebubbling処置により多くは再接着が得られる。
術後眼圧上昇:角膜内皮移植後の20〜30%にみられる。ステロイド緑内障か術後炎症に伴う続発緑内障かの鑑別が重要である。前眼部OCTで虹彩前癒着の有無を評価する。
拒絶反応:DMEK後の拒絶反応は約1%と、DSAEK後(5〜10%)に比べ低い。5年拒絶エピソード率は2.6%と報告されている6)。角膜内皮移植後の拒絶反応は全層角膜移植と異なり、ステロイド点眼のみで寛解することが多い。
COVID-19ワクチン関連拒絶:BNT162b2 mRNAワクチン接種後に両側DMEK拒絶を発症した報告がある6)。94歳女性で接種2週後に両眼のグラフト拒絶が生じ、最終的にre-DMEKを要した6)。ワクチン接種前後のステロイド点眼増量が推奨されている6)。
嚢胞様黄斑浮腫(CME):DMEK後の約10〜13.8%に生じる4)。高頻度のステロイド点眼による予防が有効であるが、ヘルペスウイルス再活性化に伴う二次性CMEも報告されている4)。
ヘルペスウイルス再活性化と再発性グラフト不全:FECDに対するDMEK後に再発性のグラフト不全を呈し、前房穿刺PCRで単純ヘルペスウイルス-1陽性が判明した症例が報告されている4)。技術的原因のない再発性DMEK不全、ホスト+グラフト両方の角膜浮腫、軽微な前房反応+眼圧上昇を認めた場合はヘルペス性ぶどう膜炎を鑑別する4)。
術中前房フィブリン反応:DMEKの約3.7%に術中自発性フィブリン形成が生じうる5)。虹彩由来のフィブリン線維がグラフト展開を妨げ、80%のグラフト不全をもたらした5)。慢性的な血液房水関門(BAB)破綻が背景にあると考えられている5)。進行期FECDでは前房内サイトカイン高値が報告されており、虹彩の微小外傷がフィブリン形成のトリガーとなる5)。予防として術前NSAIDs点眼、術中triamcinolone acetonide、r-TPA(組換え型組織プラスミノゲン活性化因子)の使用が提案されている5)。
術後2〜3日おきに前眼部OCTで角膜厚の改善とグラフト接着を確認する。グラフトが接着して見えても浮腫が改善しない場合は、後日グラフト剥離が起きる可能性がある。
ステロイド点眼(ロテプレドノールまたはデキサメタゾン)を高頻度で開始し、段階的に漸減する。拒絶反応予防のため、漸減は非常にゆっくり行うことが重要である。グラフト感染は稀であるが、ドナー由来のことが多い。角膜保存液の培養検査でカンジダなどが検出された場合は抗真菌薬点眼を処方する。
グラフト剥離はDMEK後に比較的多い合併症です。術後早期に発見した場合、前房への再気泡注入(rebubbling)により多くは再接着が得られます。完全剥離で再接着が困難な場合は再DMEKが必要になることがあります。partial(部分的)剥離であれば経過観察で自然接着する場合もあります。
Dunkerらの多施設共同無作為化比較試験(54眼)では、術後12ヶ月の平均最高矯正視力(BCVA)(logMAR)はDMEK群0.08 vs UT-DSAEK群0.15であり有意差はなかった3)。しかし20/25以上の最高矯正視力達成率はDMEK群66% vs UT-DSAEK群33%と有意にDMEKが高かった(P=0.02)3)。内皮細胞密度(ECD)は12ヶ月後で両群間に有意差はなかった(DMEK 1870 cells/mm² vs UT-DSAEK 1612 cells/mm²)3)。
| 項目 | DMEK | UT-DSAEK |
|---|---|---|
| 20/25達成率 | 66%3) | 33%3) |
| 12ヶ月最高矯正視力 | 0.08 logMAR3) | 0.15 logMAR3) |
| 内皮細胞密度(12ヶ月) | 1870 cells/mm²3) | 1612 cells/mm²3) |
Selaらのメタアナリシス(8研究、376眼)では、12ヶ月最高矯正視力はDMEK群で有意に良好であった(平均差 −0.06 logMAR; 95%CI −0.10〜−0.02)2)。ただしrebubbling率はDMEK群で有意に高く(OR 2.76; 95%CI 1.46-5.22)、適切な患者選択が重要である2)。70μm未満の超薄DSAEKグラフトでは最高矯正視力に有意差がみられなかった2)。
両術式ともに軽度の遠視シフトを生じるが、DMEKのほうがシフト量は小さい(DMEK +0.22D vs UT-DSAEK +0.58D)3)。5年グラフト生存率および内皮細胞減少率は両術式で同等と報告されている1)。
COL8A2遺伝子変異(p.Leu450Trp)による早期発症型Fuchs角膜内皮ジストロフィの4眼(2患者)にDMEKが施行された7)。術前平均中心角膜厚(CCT)は713μmから術後1ヶ月で529μmに減少し、全眼が20/20〜20/30の最高矯正視力を達成した7)。ただし、術後初年に3〜3.6Dの屈折変動を認めたことから、COL8A2変異患者では屈折安定までに長期間を要する7)。
多くの患者で術後12ヶ月以内に20/25(0.8)以上の最高矯正視力が得られます。多施設RCTでは66%の眼が20/25以上を達成しました。ただし角膜実質の瘢痕や長期浮腫による不可逆的変化がある場合は回復に限界があります。
正常な角膜内皮細胞はNa⁺/K⁺-ATPaseポンプにより角膜実質から前房へ水を汲み出し、角膜の含水率を78%前後に維持している。FECDやPBKではこのポンプ機能が破綻し、角膜実質に過剰な水分が貯留して角膜浮腫・混濁を来す。
DMEKでは病的デスメ膜と機能不全内皮をDescemetorhexisで除去し、健常なドナーのデスメ膜+内皮複合体を移植することで角膜のポンプ機能が回復する。グラフトが角膜後面に接着すると、内皮細胞が水の排出を再開し、角膜浮腫は速やかに改善する。
内皮移植後のグラフト剥離やDescemetorhexis単独施行後に角膜が自然に透明化する症例が報告されている1)。この現象はFECDでは起きるが水疱性角膜症では起きないことから、FECDの周辺部に残存する内皮細胞が中央に遊走して機能を回復する可能性が示唆されている1)。
メタアナリシスにおいて、70μm未満の超薄角膜内皮移植術グラフトではDMEKとの視力差が消失する可能性が示唆されている2)。Nanothin DSAEK(50μm未満)はDMEKと同等の成績をもたらす可能性があるが、まだadditive(付加的)移植であり真のreplacement surgeryではない。
早期発症型Fuchs角膜内皮ジストロフィ(COL8A2 p.Leu450Trp変異)に対してDMEKが初めて施行され、全眼で良好な視力が得られた7)。術後の屈折変動が大きいため、眼内レンズ度数計算やフォローアップの戦略が今後の検討課題である7)。
COVID-19ワクチン接種後にDMEKグラフト拒絶が複数報告されている6)。ワクチン誘発性の免疫応答変化がグラフト拒絶を惹起する可能性があり、接種前後のステロイド点眼増量が推奨されている6)。
術中前房フィブリン形成はDMEKの約3.7%に生じ、高率にグラフト不全を引き起こす5)。術前NSAIDs点眼による予防、術中triamcinolone acetonideによるフィブリン検出、r-TPAによるフィブリン溶解が新しい管理戦略として提案されている5)。
DMEK後にワクチン接種(とくにmRNAワクチン)を受ける際は、拒絶反応のリスクに留意してください。接種前後にステロイド点眼(デキサメタゾン0.1%を1日2〜4回)を追加することが推奨されています。接種後に視力低下や充血を感じたら早急に受診してください。
Deng SX, Lee WB, Hammersmith KM, et al. Descemet membrane endothelial keratoplasty: safety and outcomes: a report by the American Academy of Ophthalmology. Annu Rev Vis Sci. 2019;5:303-328.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. BMJ Open Ophthalmol. 2023;8:e001397.
Dunker SL, Dickman MM, Wisse RPL, et al. Descemet membrane endothelial keratoplasty versus ultrathin Descemet stripping automated endothelial keratoplasty: a multicenter randomized controlled clinical trial. Ophthalmology. 2020;127(9):1152-1159.
Matar C, Seitz B, Daas L. Rezidivierendes DMEK-Versagen [Recurrent DMEK failure]. Ophthalmologe. 2021;118(7):719-723.
Trinh L, Bouheraoua N, Muraine M, Baudouin C. Anterior chamber fibrin reaction during Descemet membrane endothelial keratoplasty. Am J Ophthalmol Case Rep. 2022;25:101323.
Forshaw TRJ, Jørgensen C, Kyhn MC, Cabrerizo J. Acute bilateral Descemet membrane endothelial keratoplasty graft rejection after the BNT162b2 mRNA COVID-19 vaccine. Int Med Case Rep J. 2022;15:201-204.
Dzhaber D, Fliotsos MJ, Abousy M, et al. Descemet membrane endothelial keratoplasty in eyes with COL8A2-associated corneal dystrophy. Am J Ophthalmol Case Rep. 2022;26:101544.
Matthaei M, Hribek A, Clahsen T, et al. Fuchs endothelial corneal dystrophy: clinical, genetic, pathophysiologic, and therapeutic aspects. Annu Rev Vis Sci. 2019;5:151-175.