表層性血管新生

角膜新生血管(Corneal Neovascularization)
1. 角膜新生血管とは
Section titled “1. 角膜新生血管とは”角膜新生血管(corneal neovascularization; CoNV)は、本来無血管である角膜組織に輪部血管叢から新しい毛細血管が侵入する病態である1)。特定の疾患名ではなく、感染・炎症・低酸素・外傷など多様な病態に対する非特異的反応として生じる。
角膜は「血管新生特権(corneal angiogenic privilege; CAP)」を保持しており、血管新生抑制因子と促進因子の精密な均衡によって無血管状態が維持されている1)。この均衡が破綻すると、血管内皮細胞が増殖・遊走し、角膜実質に侵入する。
新生血管は解剖学的位置により2型に分類される。
深層性血管新生
前毛様動脈から角膜実質内に侵入する。
角膜実質炎(梅毒・結核)、実質型ヘルペス角膜炎、水疱性角膜症などの持続的な炎症・浮腫で生じる。
未熟な新生血管は脂質滲出・持続的炎症・瘢痕化を引き起こす1)。進行すると血管は成熟し、周皮細胞(pericyte)に被覆されて抗VEGF療法に抵抗性を示すようになる1)。角膜移植後の患者では、新生血管が拒絶反応のリスク因子となる。
放置すると新生血管が成熟して自然退縮しにくくなり、脂質角膜症(脂質の角膜内沈着)や角膜瘢痕を生じて永続的な視力低下の原因となります。また角膜移植が必要になった場合、新生血管の存在は移植片の拒絶反応リスクを高めます。早期の受診と原因治療が重要です。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”- 視力低下:新生血管やその続発症(脂質沈着・瘢痕)が視軸にかかった場合に生じる
- 充血:原因疾患に伴う結膜充血
- 無症状:視軸に病変が及ばない場合は自覚症状を欠くことが多い
臨床所見(医師が診察で確認する所見)
Section titled “臨床所見(医師が診察で確認する所見)”- 新生血管の形態:微細な網状パターンから、怒張した活動性血管、成熟した高密度血管まで多様
- 血管の位置と深さ:表層性か深層性かを細隙灯顕微鏡のスリット法・間接照明法で評価する
- ghost vessel:血流が途絶えた陳旧性の血管。治療の必要はない
- 結膜侵入(conjunctivalization):角膜上に結膜組織が被覆した状態。フルオレセイン染色のdelayed stainingで確認される
- 脂質角膜症(lipid keratopathy):新生血管から漏出した脂質が角膜実質に沈着した黄白色の混濁
- Vogtの角膜輪部柵(POV)の消失:輪部幹細胞の消失を示唆する重要な所見
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”- 単純ヘルペスウイルス(HSV-1):先進国における角膜新生血管の最も一般的な感染性原因1)。実質型角膜ヘルペスでは深層性血管新生を生じる
- 細菌性角膜炎:重症例では角膜潰瘍と瘢痕に伴い血管侵入が生じる
- 真菌性角膜炎:治療遷延例で新生血管を伴うことがある
- トラコーマ・オンコセルカ症:開発途上国における主要な感染性原因1)
低酸素(コンタクトレンズ関連)
Section titled “低酸素(コンタクトレンズ関連)”ソフトコンタクトレンズの不適切な装用(over-wearing)が主な原因である。従来型のHEMA素材SCL装用者の約80~90%に角膜上方からの血管侵入(10時~2時方向)が認められる。上皮障害が1か月以上遷延するとその部位に血管が侵入する。
アルカリ外傷は角膜実質深部まで浸透し、広範な輪部幹細胞障害と新生血管を引き起こす。角膜移植の成功率が著しく低い群の一つである。
輪部幹細胞欠乏症(LSCD)
Section titled “輪部幹細胞欠乏症(LSCD)”LSCDは角膜新生血管の主要な経路の一つである1)3)。先天性・化学外傷・CL over-wear・全身性炎症性疾患・医原性などにより輪部幹細胞が機能不全に陥ると、正常な上皮バリアが失われ血管侵入が生じる3)。軽症ではフルオレセイン染色で渦巻状上皮症が認められ、中等症で表層性新生血管とパンヌスが出現する3)。
その他の原因
Section titled “その他の原因”- 炎症性疾患:SJS/TEN、眼類天疱瘡、春季カタル、酒皶性角膜炎
- 角膜移植後:拒絶反応に伴う新生血管1)
- 変性疾患:Terrien辺縁角膜変性、膠様滴状角膜ジストロフィ
はい、予防できる場合が多いです。角膜新生血管の主な原因の一つはコンタクトレンズによる酸素不足です。装用時間を守ること、酸素透過性の高いレンズを使用すること、定期的な眼科検診を受けることで、リスクを大幅に低減できます。
4. 診断と検査方法
Section titled “4. 診断と検査方法”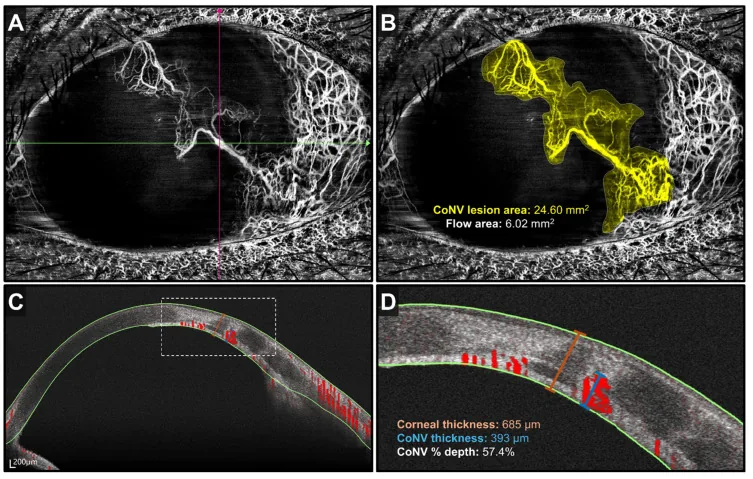
細隙灯顕微鏡検査
Section titled “細隙灯顕微鏡検査”角膜新生血管の診断において最も基本的な検査である。血管の位置(象限)、深さ(表層性/深層性)、活動性(血流の有無)、結膜侵入の有無を評価する。
- ディフューザー法:照射光幅を太くするか拡散板を介して観察すると新生血管を判別しやすい
- 間接照明法:虹彩や水晶体からの反射光で新生血管・角膜神経を観察する
- フルオレセイン染色:上皮欠損の有無、結膜侵入の評価に有用
蛍光造影検査
Section titled “蛍光造影検査”- フルオレセイン蛍光造影(FA):血管灌流と漏出を機能的に評価し、活動性血管と成熟血管を鑑別する1)
- インドシアニングリーン蛍光造影(ICGA):深層血管や輸入血管の描出に優れ、血管閉塞術のターゲティングに有用1)
- 前眼部OCT / OCT-A:非侵襲的に角膜血管網の深さと範囲を定量評価できる1)
- 生体内共焦点顕微鏡(IVCM):LSCDの診断において上皮基底細胞の定量が可能3)
| 検査法 | 主な評価項目 | 特徴 |
|---|---|---|
| 細隙灯顕微鏡 | 位置・深さ・活動性 | 第一選択の基本検査 |
| FA / ICGA | 灌流・漏出・輸入血管 | 治療計画に有用 |
| AS-OCT / OCT-A | 深度・定量的評価 | 非侵襲的 |
5. 標準的な治療法
Section titled “5. 標準的な治療法”角膜新生血管の治療は、原因治療と新生血管そのものへの介入の二本柱からなる2)。
- CL装用中止:低酸素性の場合は装用を中止し、酸素透過性の高いレンズへの変更を検討する。活動性血管か陳旧性(ghost vessel)かを見極める
- 感染治療:原因となる感染性角膜炎に対する抗菌薬・抗ウイルス薬・抗真菌薬の投与
- LSCD治療:輪部移植・羊膜移植などの手術治療
- ステロイド点眼:炎症性サイトカイン(IL-1、IL-6)の抑制、リンパ球のアポトーシス誘導、血管拡張抑制により血管新生を抑制する2)。第一選択だが、長期使用ではステロイド緑内障や感染感受性亢進に注意
- 抗VEGF療法:ベバシズマブ(点眼・結膜下注射・角膜実質内注射)が広く使用される1)2)。未熟な活動性血管に対して有効だが、成熟血管(周皮細胞に被覆された血管)に対する効果は限定的1)。新生血管の発症から2週間以内に周皮細胞被覆が80%に達するため、早期治療が重要である1)
- 免疫抑制薬:シクロスポリンA点眼はT細胞の活性化を抑制し、ステロイド節減効果がある2)。タクロリムス、シロリムス(mTOR阻害薬)も選択肢となる1)
- ドキシサイクリン:粘膜類天疱瘡阻害作用により角膜新生血管を抑制する2)
手術療法・手技的治療
Section titled “手術療法・手技的治療”- レーザー光凝固術:アルゴンまたはNd:YAGレーザーで血管を凝固・閉塞させる。角膜移植前の前処置や脂質角膜症の治療に使用される。角膜出血・菲薄化のリスクがあり、血管の再開通やシャント血管形成がしばしば認められる
- fine needle diathermy(FND):輪部の栄養血管に細い針を挿入し、電気的に凝固閉塞する。成熟した太い血管にも有効であり、アルゴンレーザーでは閉塞困難な輸入血管に対して施行される1)
- 光力学療法(PDT):光感受性物質を血管内に注入後、光照射により活性酸素種を生成し血管壁を破壊する。高い特異性を有するが、高コストと時間を要する
- MICE(MMC血管内化学塞栓術):33ゲージ針でマイトマイシンC(0.4 mg/mL)を栄養血管内に直接注入する手技6)。従来の治療に抵抗性の難治性角膜新生血管に対し、血管ゴースト化と脂質角膜症の改善が報告されている6)
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”血管新生特権(CAP)の維持機構
Section titled “血管新生特権(CAP)の維持機構”角膜の無血管状態は、複数の血管新生抑制機構が協調して維持している1)。
- 可溶性VEGF受容体1(sVEGFR1):角膜上皮・実質から恒常的に産生される。VEGF-Aを高親和性で捕捉し、膜結合型VEGFRへの結合を競合的に阻害する内因性VEGFトラップである1)
- トロンボスポンジン(TSP-1/TSP-2):角膜ECMに恒常的に発現する血管新生抑制性糖タンパク質。VEGFを隔離しVEGFR2シグナルを抑制する。CD36/CD47を介しVEC(血管内皮細胞)のアポトーシスを誘導する1)
- エンドスタチン:コラーゲンXVIIIのC末端フラグメント。VEGF・bFGF経路を阻害し、カスパーゼ3活性亢進によりVECのアポトーシスを促進する。リンパ管新生も抑制する1)
- 物理的バリア:輪部バリア、密なコラーゲン配列、角膜の相対的低温環境が血管侵入を制限する1)
血管新生促進因子と発症経路
Section titled “血管新生促進因子と発症経路”CAPの破綻は主に2つの経路で生じる1)2)。
経路1:炎症・低酸素による促進因子の産生亢進
角膜の損傷により、マクロファージ・上皮細胞・内皮細胞から3種の主要血管新生因子が放出される1)。
- VEGF-A:VEGFR-2を介してVECの増殖・遊走を促進し、粘膜類天疱瘡-2/粘膜類天疱瘡-9を誘導してECMリモデリングを促す1)。角膜新生血管において最も重要な促進因子
- bFGF(FGF-2):ERK/PI3K経路を介しVEGF産生を亢進させ、VE-カドヘリン結合を解離させてVECのスプラウティングを促進する1)
- PDGF:周皮細胞・平滑筋細胞をリクルートし、新生血管を安定化させる1)。PDGFによる血管成熟は抗VEGF療法への抵抗性をもたらす
経路2:輪部幹細胞欠乏症(LSCD)
輪部幹細胞の消失により角膜上皮の正常なバリア機能が失われ、結膜組織の角膜侵入と持続的炎症が新生血管を維持する1)3)。
リンパ管新生との関連
Section titled “リンパ管新生との関連”角膜新生血管(血管新生)とリンパ管新生は相互に関連しつつ独立した過程である4)。血管は免疫エフェクター細胞の輸出路(遠心路)として、リンパ管は抗原提示細胞の輸入路(求心路)として機能する4)。両者の同時進行は角膜移植における免疫特権の喪失と拒絶反応に関与する4)。VEGF-A/VEGFR-2が血管新生を、VEGF-C,D/VEGFR-3がリンパ管新生を主に駆動する4)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”AAVベクターによる遺伝子治療
Section titled “AAVベクターによる遺伝子治療”Xieら(2024)は、アデノ随伴ウイルス(AAV)ベクターを用いた持続的抗VEGF因子の発現による角膜新生血管治療を総説した5)。AAV2およびAAV8が角膜実質細胞の形質導入に最も効率的であり、角膜実質内注射が最も有効な投与経路とされる5)。AAV遺伝子治療は単回投与で長期間の抗VEGF効果を発揮しうるが、現時点では前臨床段階にとどまる5)。
MMC血管内化学塞栓術(MICE)
Section titled “MMC血管内化学塞栓術(MICE)”Addeenら(2023)は、角膜移植後の難治性新生血管に対するMICE(33ゲージ針でMMC 0.4 mg/mLを血管内注入)の2症例を報告した6)。術後早期から血管のゴースト化が認められ、疼痛軽減とQOL改善が得られた6)。有害事象は認められなかったが、長期安全性の確認が必要とされる。
アンチセンスオリゴヌクレオチド(Aganirsen)
Section titled “アンチセンスオリゴヌクレオチド(Aganirsen)”Mullerら(2026)の総説では、IRS-1を標的とするアンチセンスオリゴヌクレオチドAganirsenが角膜新生血管の退縮と寛解を前臨床モデルで示したことが報告されている1)。CRISPR/Cas9によるVEGF-A編集も有望な前臨床データを示している1)。
眼科用ナノシステム
Section titled “眼科用ナノシステム”Zhangら(2022)は、ナノ粒子・リポソーム・ミセルなどのナノキャリアが抗VEGF薬やステロイドの角膜内送達効率を改善し、持続放出・標的指向性・低刺激性を実現しうることを報告した7)。臨床応用はまだ限定的だが、頻回投与の負担軽減が期待される。
併用療法の重要性
Section titled “併用療法の重要性”角膜新生血管は多因子性の病態であるため、単一の治療法では十分な効果が得られないことが多い1)2)。VEGF、bFGF、PDGF、リンパ管新生など複数の経路を標的とする併用療法が、今後の治療戦略の中心となる可能性がある1)。
8. 参考文献
Section titled “8. 参考文献”- Muller E, Feinberg L, Woronkowicz M, Roberts HW. Corneal Neovascularization: Pathogenesis, Current Insights and Future Strategies. Biology. 2026;15(2):136.
- Wu D, Chan KE, Lim BXH, et al. Management of corneal neovascularization: Current and emerging therapeutic approaches. Indian J Ophthalmol. 2024;72(Suppl 3):S354-S371.
- Drzyzga L, Spiewak D, Dorecka M, Wygledowska-Promienska D. Available Therapeutic Options for Corneal Neovascularization: A Review. Int J Mol Sci. 2024;25(10):5479.
- Zhang Z, Zhao R, Wu X, Ma Y, He Y. Research progress on the correlation between corneal neovascularization and lymphangiogenesis. Mol Med Rep. 2025;31(2):47.
- Xie M, Wang L, Deng Y, et al. Sustained and Efficient Delivery of Antivascular Endothelial Growth Factor by AAV for Treatment of Corneal Neovascularization. J Ophthalmol. 2024;2024:5487973.
- Addeen SZ, Oyoun Z, Alfhaily H, Anbari A. Outcomes of mitomycin C intravascular chemoembolization (MICE) in refractory corneal neovascularization after failed keratoplasty. Digit J Ophthalmol. 2023;29(4).
- Zhang C, Yin Y, Zhao J, et al. An Update on Novel Ocular Nanosystems with Possible Benefits in the Treatment of Corneal Neovascularization. Int J Nanomedicine. 2022;17:4911-4931.
