上皮浮腫
微小嚢胞状浮腫:上皮細胞間に液体が貯留し、微細な嚢胞を形成する。スクレラルスキャター法で容易に観察可能。
上皮水疱:浮腫が進行すると上皮下に水疱が形成される。水疱の破裂は激しい疼痛と上皮欠損を引き起こす。
すりガラス状混濁:上皮・実質の浮腫によりびまん性の角膜混濁を呈する。

角膜浮腫(corneal edema)は、角膜の一層または複数層に過剰な水分が貯留した状態である。角膜厚が増大し、透明性が失われることで視機能の低下を来す。
角膜浮腫は障害される層に応じて以下のように分類される。
角膜内皮細胞は分裂能がきわめて乏しく、加齢や長期のコンタクトレンズ装用などで漸減する。何らかの病因により角膜内皮細胞密度が閾値(おおよそ500 cells/mm²以下)を下回ると、角膜実質の含水率を維持できなくなり水疱性角膜症に至る。主な病因には白内障手術・内眼手術、アルゴンレーザー虹彩切開術、Fuchs角膜内皮ジストロフィなどがある。
主な原因を片眼性・両眼性で分類すると以下のようになる。
| 原因 | 片眼性 | 両眼性 |
|---|---|---|
| Fuchs角膜内皮ジストロフィ | ○ | |
| PPCD・CHED | ○ | |
| 白内障手術後(偽水晶体眼) | ○ | ○ |
| 急性閉塞隅角緑内障 | ○ | |
| ICE症候群 | ○ | |
| 感染性角膜炎 | ○ | |
| 薬剤性(アマンタジン等) | ○ |
炎症性や眼圧上昇に伴う角膜浮腫は、原因の解消(消炎・降圧)により自然軽快することが多い。鉗子分娩によるDescemet膜破裂も自然治癒する。角膜内皮細胞の不可逆的な減少がある場合にのみ手術が検討される。詳細は「標準的な治療法」の項を参照。
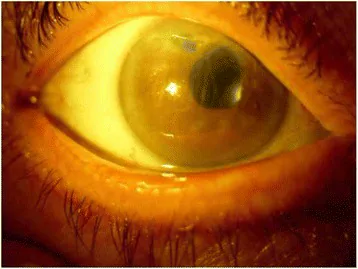
角膜浮腫の自覚症状は浮腫の程度と罹患層により異なる。
角膜浮腫の臨床所見は障害層によって異なる。
上皮浮腫
微小嚢胞状浮腫:上皮細胞間に液体が貯留し、微細な嚢胞を形成する。スクレラルスキャター法で容易に観察可能。
上皮水疱:浮腫が進行すると上皮下に水疱が形成される。水疱の破裂は激しい疼痛と上皮欠損を引き起こす。
すりガラス状混濁:上皮・実質の浮腫によりびまん性の角膜混濁を呈する。
実質浮腫・水疱性角膜症
Descemet膜皺襞:実質の膨潤に伴い角膜後面に皺襞を生じる。内皮障害の重要な指標。
角膜厚増大:正常角膜厚(約540μm前後)から著明に増大する。800μmを超える症例もある。
上皮下線維化:慢性例では水疱性角膜症に至り、上皮下に瘢痕組織が形成される。水疱の減少と疼痛の軽減につながる。
浮腫の分布パターンは原因の鑑別に有用である。
角膜内皮の機能が低下している場合、閉眼中(睡眠中)は涙液蒸散が減少し角膜浮腫が蓄積しやすくなる。日中は蒸散により改善するため、朝方に視力が低下し午後に回復する日内変動が生じる。このパターンはFuchs角膜内皮ジストロフィの初期症状として典型的である。
角膜浮腫の原因は多岐にわたり、内因性と外因性に大別される。
Vandevenneら(2024)は、進行性円錐角膜に対するカスタマイズクロスリンキング後4ヶ月で微小嚢胞状角膜浮腫を発症した症例を報告した3)。内皮細胞密度は2414→1514 cells/mm²と37%の喪失を認めたが、1ヶ月で自然消退した。UV-A照射時の角膜厚375μmは内皮障害の閾値(0.65 J/cm²)付近であった。
Safranら(2022)は、白内障術後20〜30年に石灰化Soemmering ring由来の微小粒子が角膜内皮に沈着し、炎症を伴わない限局性角膜浮腫を引き起こした3例を報告した7)。角膜内皮移植術と前房洗浄による治療が行われた。
Chuら(2021)は、角膜浮腫やぶどう膜炎の既往のない79歳女性がRhopressa開始5日後に重度の角膜浮腫を発症した症例を報告した4)。角膜厚は557→808μmに急増し視力は20/200に低下したが、中止と高張食塩水・ステロイド点眼により4ヶ月で完全回復した。
前眼部手術後に生じる非感染性の急性炎症反応である。
Ariciら(2022)は、合併症なく施行された翼状片手術後にびまん性角膜浮腫を発症した症例を報告した5)。PVP-Iの角膜内皮毒性が疑われ、集中的なデキサメタゾン点眼で2週間以内に消退した。ただし1年後の内皮細胞密度は1001 cells/mm²と高度に減少していた。
角膜浮腫の診断は臨床所見と補助検査の組み合わせにより行われる。原因の特定が治療方針を決定する上で最も重要である。
最も基本的な検査法である。
浮腫の定量的評価に不可欠な検査である。
| 検査法 | 特徴 | 留意点 |
|---|---|---|
| 超音波パキメトリ | 標準検査 | 同一部位の再現性に注意 |
| 前眼部OCT(AS-OCT) | 非接触、複数部位測定可 | 浮腫 > 650μmでも信頼性良好 |
| Scheimpflug撮影 | 角膜全体の厚さマップ | 高度浮腫では過大評価の可能性 |
超音波パキメトリは迅速かつ信頼性が高く、角膜厚測定の標準検査とされる2)。前眼部OCTやScheimpflug撮影は複数部位の測定と高い再現性を備える2)。
FECDの重症度評価では、角膜中心部と周辺部の厚さ比(central-to-peripheral thickness ratio)が発症前の基準値が不明な場合の客観的指標として提唱されている2)。
角膜内皮細胞密度・形態の評価に用いる。軽症例での術前評価に有用であるが、重度の角膜浮腫では正確な測定が困難になる。両眼間の内皮状態の比較にも役立つ。
Descemet膜剥離や細隙灯顕微鏡では確認困難な構造異常の可視化に有用である。角膜浮腫の評価における重要な補助検査として位置づけられる。
角膜浮腫の治療は原因の除去を基本とし、内皮障害の可逆性に応じて内科的治療または外科的治療を選択する。
角膜内皮の不可逆的な機能障害が確認された場合に適応となる。
バンデージコンタクトレンズは上皮水疱の疼痛を緩和する一時的な手段であり、長期的な解決策ではない。装用中は感染性角膜炎のリスクがあるため、定期的な眼科受診と予防的な抗菌薬点眼が必要となる。角膜内皮移植術が適応となる場合は、移植までのつなぎとして使用される。
角膜は約78%の含水率を維持することで透明性を保っている。この相対的な脱水状態(deturgescence)は以下の5因子の平衡により維持される。
角膜内皮の水分調節はMauriceが提唱した「pump-leak mechanism」に基づく1)。角膜内皮細胞は一次性および二次性の能動輸送機構を介して、角膜実質から前房側へのイオン移動(ネットイオンフラックス)を駆動し、浸透圧勾配を形成する。このポンプ機能は主にHCO₃⁻とCl⁻に依存し、Na⁺-K⁺ ATPaseが一次性能動輸送の中核を担う1)。
FECDでは、角膜内皮細胞の進行性の死により最終的にバリア機能とポンプ機能の両方が喪失し、角膜浮腫と有痛性の上皮水疱が形成される1)。
角膜厚が増大しているが上皮浮腫をまだ呈していないFECD患者では、角膜内皮の透過性亢進(バリア機能障害)が認められる一方、ポンプ速度には有意差がないことが示されている1)。この知見は、バリア機能の障害がポンプ機能の障害に先行する可能性を示唆する。
Toneら(2021)によれば、FECDの初期段階ではNa⁺-K⁺ ATPase密度の代償性増加が認められるが、病態の進行に伴いNa⁺-K⁺ ATPase密度は漸進的に低下する1)。リアルタイムPCRではFECDの角膜内皮細胞においてNa⁺-K⁺ ATPaseの有意なダウンレギュレーションが検出されており、MCT 1および4のダウンレギュレーションとともに内皮ポンプ機能の障害を裏付ける。
眼圧が約50 mmHgを超えると、前房水が前房圧により上皮層内に押し込まれ上皮浮腫を生じる。ただし、実質膨潤圧よりも前房圧のほうが高いため、この場合は実質浮腫を伴わない。
角膜内皮細胞密度が2000 cells/mm²を下回ると透過性は徐々に増加するが、代償的なポンプ機構により500 cells/mm²前後まではdeturgescenceが維持される。この閾値を下回ると水疱性角膜症に至る可能性が高い。ただし閾値には個人差が大きい。
おおよそ500 cells/mm²以下に減少すると水疱性角膜症に至る可能性が高い。ただし閾値には個人差が大きく、同じ細胞密度でも浮腫を生じる人とそうでない人がいる。角膜内皮細胞はヒトでは分裂・再生がきわめて困難であり、一度減少すると自然に元に戻ることはない。
EndoArt(EyeYon Medical社)は、角膜後面の曲率に適合する直径6.0 mm・厚さ50μmのドーム型人工内皮層である。親水性アクリル素材から成り、DMEKと同様の手技で前房内に挿入される。非生体材料であるため免疫抑制療法は不要であり、長期保存が可能である。
Auffarthら(2021)は、角膜内皮代償不全による慢性角膜浮腫の2例にEndoArtを移植した6)。角膜厚は症例1で730→526μm、症例2で761→457μmに減少し、17ヶ月時点で安定していた。両症例とも術後に脱落が生じたが再固定で回復した。米国FDAのBreakthrough Therapy Designationを取得しており、欧州で多施設前向き臨床試験が進行中である。
DSOは中心部のDescemet膜のみを除去し、周辺の健常な内皮細胞が中心部へ遊走・再生することで角膜浮腫の消退を図る術式である。従来はFECDが主な適応であったが、近年は術後合併症による限局性角膜浮腫への適応も報告されている。
Khan & Lin(2023)は、MIGS(Hydrus)挿入中止後のDescemet膜剥離に伴う角膜浮腫にDSOを施行した最初の症例を報告した8)。4×5 mmの偏心descemetorrhexisを行い、6週間で浮腫が消退した。中心部の角膜内皮細胞密度は検出不能から975 cells/mm²に回復した。ROCK阻害薬(リパスジル・ネタルスジル)の補助療法としての併用も検討されている。
培養したヒト角膜内皮細胞にROCK阻害薬を併用して前房内に注入する手法が報告されており、ドナー角膜を必要としない治療法として注目されている6)。
- Tone SO, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: the vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
- Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs endothelial corneal dystrophy: clinical, genetic, pathophysiologic, and therapeutic aspects. Annu Rev Vis Sci. 2019;5:151-175.
- Vandevenne MMS, Berendschot TTJM, Visser N, Dickman MM, Nuijts RMMA. Late-onset corneal edema after customized crosslinking for progressive keratoconus. Am J Ophthalmol Case Rep. 2024;35:102090.
- Chu MJ, Song M, Palmares T, Song A, Song J. Rhopressa-induced corneal edema: a case report. J Med Case Rep. 2021;15:182.
- Arici C, Mergen B, Kılıçarslan O, Ağaçhan A, Tülü Aygün B, Özdamar A. Diffuse corneal edema after uneventful pterygium surgery: toxic anterior segment syndrome or toxic keratopathy? Turk J Ophthalmol. 2022;52:69-71.
- Auffarth GU, Son HS, Koch M, et al. Implantation of an artificial endothelial layer for treatment of chronic corneal edema. Cornea. 2021;40:1633-1638.
- Safran JP, Nataneli N, Vazirani J, Eagle RC Jr, Milman T. Corneal edema associated with degenerating Soemmering ring cataract: clinical-pathologic correlation. Am J Ophthalmol Case Rep. 2022;28:101738.
- Khan NC, Lin CC. Descemet stripping only for Descemet’s membrane detachment and sectoral corneal edema. Am J Ophthalmol Case Rep. 2023;29:101784.